В условиях глобальной антропогенной нагрузки на компоненты природной среды значительное место занимают проблемы радиоактивного загрязнения. Низко интенсивному радиационному прессу подвергаются природные комплексы Восточно-Уральского радиоактивного следа (ВУРС, Свердловская обл.) и Тоцкого радиоактивного следа (ТРАС, Оренбургская обл.). где дозообразующими радионуклидами в современных условиях являются долгоживущие 90Sr и 137Cs [5, 6, 7, 9]. Полураспад и полное исчезновение основного загрязнителя 90Sr займет многие годы [9]. В связи с этим оценка влияния малых доз излучения на животный организм и его ответ на условия загрязненной среды является актуальной.
В качестве биоиндикаторов состояния природной среды часто используют мелких млекопитающих. В случае обитания животных в условиях повышенного радиоактивного загрязнения среды нет четкого представления о радиорезистентности организма млекопитающих. Ответ на воздействие поступающих в организм токсикантов зависит от концентрации, их состава, длительности действия, видовой специфики организмов и других факторов способных вызывать отклонение от нормы различных показателей. Действие малых доз радиационной или химической природы сложно оценить, но чрезвычайно важно, поскольку из неспецифических проявлений на начальном этапе поражения оно может изменить реактивное состояние организма и перейти в специфические. Оценить влияние на живой организм экологических факторов, его ответ на внешние воздействия позволяет изучение системы кроветворения, комплексная оценка количества, качества, состава клеток крови и кроветворных органов [4, 8].
Задача исследования – оценить по комплексу количественных и структурных показателей, клеточного состава крови и кроветворных органов мелких млекопитающих влияние низкого уровня радиационного загрязнения среды.
Материал и методы исследования
Объектом исследования служили достаточно однородные по репродуктивному статусу, отловленные в июле–августе 1993–1994 гг., Apodemus sylvaticus (19 особей, из них 13 самцов, 6самок) и Clethrionomys rutilus (9 особей: 5 самцов и 4 самки) из окрестностей озера Тыгиш, расположенного в буферной зоне ВУРСа [7] и Mus musculus (21 особь: 10 самцов и 11 самок) с территории пос. Старобогдановка, расположенной по осевой части ТРАСа [6]. Контрольные участки находились за пределами следа: Большая Грязнуха с ВУРСа (8 особей Ap. sylvaticus, из них 5 самцов и 3самки, 9 особей Cl. rutilus, 4 самца и 5 самок) и Кристалка с ТРАСа (14 особей M. musculus – 9 самцов и 5 самок).
У каждого животного определяли параметры крови (концентрацию и клеточный состав, гемоглобин, гематокрит, осмотическую резистентность эритроцитов в растворах 0,85–0,1 % NaCl и 16, 50 и 84 % гемолиз), параметры эритроцитов (средний диаметр, объем, содержание и концентрацию гемоглобина в эритроците, толщину, площадь поверхности эритроцитов, концентрацию гемоглобина на единицу площади поверхности), способность крови переносить кислород единицей объема. Определяли массу и клеточность селезенки, концентрацию и состав клеток костного мозга бедренной кости, пролиферативную активность, индексы созревания эритроцитов и гранулоцитов.
Определяли содержание радионуклидов в зольном остатке костно-мышечной ткани каждой тушки (с удаленными органами и черепом): суммарную бета-активность рассчитанную по 90Sr, содержание 137Cs и 90Sr для каждой выборки. Детально метод описан в работе [6].
Полученные данные анализировали с помощью “Statistica for Windows” (дисперсионный, ковариационный анализ), при оценке различий показателей использовали Tukey-тест для разного числа животных.
Результаты исследования и их обсуждение
Комплексное радиоэкологическое обследование территорий ВУРСа и ТРАСа выявило превышение уровней 137Cs и 90Sr контрольных участков, гамма-фон в зоне ТРАСа и ВУРСа соответствуют пределам колебаний в контрольном регионе, дозообразующими радионуклидами в современных условиях являются долгоживущие 90Sr и 137Cs [5, 6, 9]. Плотность загрязнения цезием почв ТРАСа превышала уровень глобальных выпадений (в 1,5–3 раза), стронцием – не отличалась от фоновых значений. Превышало уровень глобальных выпадений (в 1,5–5 раз) содержание плутония [5, 6]. Содержание 90Sr в костно-мышечной ткани домовых мышей опытной группы превышало значения контрольной группы (12 ± 1,2 против 4,9 ± 0,9 Бк/кг сухой массы), содержание 137Cs не различалось (18,5 ± 5 против 15 ± 5 Бк/кг), бета-активность составила 256,3 против 231,3 Бк/кг сухой массы в контроле.
Радиоэкологический мониторинг территорий ВУРСа [9] выявил пятнистую структуру загрязнений: при средней плотности 0,5–1 Ки/км2 найдены отдельные аномалии по 90Sr (2–3 Ки/км2) и 137Cs (до 0,5 Ки/км2). Более высокие концентрации 90Sr и 137Cs найдены в костно-мышечной ткани животных с опытного участка по сравнению с контрольным (137Cs в 1,5 раза у красной полевки и в 1,9 раза у лесной мыши, 90Sr в 6,1 у красной полевки и в 3,6 раза у лесной мыши), при этом у красной полевки содержание 90Sr и 137Cs больше (в 2,2 и в 1,3 раза), чем у лесной мыши [6]. Уровень бета-активности у лесной мыши с импактной территории составил 112 Бк/кг против 31 Бк/кг в контроле, у красной полевки – 248 и 41 Бк/кг сухой массы. У лесной мыши с ТРАСа уровень бета-активности составил 305,0 ± 7,6 Бк/кг, у красной полевки из окрестностей оз. Тыгиш и ТРАСа уровни были близки [6].
По данным ряда авторов столь незначительные загрязнения радионуклидами почвенно-растительного покрова не должны вызывать каких-либо изменений на уровне экосистем или клеток [2, 3]. Однако обнаружены изменения на растительных объектах [7], выявленные радионуклиды в тушках мышей и полевок с территорий ТРАСа и ВУРСа свидетельствуют о факте облучения организма и протекании жизнедеятельности животных в условиях радиоактивного загрязнения. С помощью ковариационного анализа мы установили влияние радионуклидов на показатели селезенки, диаметр эритроцитов, концентрацию гемоглобина и костного мозга у животных опытной группы, не найдено связи ни с одним из исследованных показателей в контрольной выборке. Исследование комплекса параметров системы крови мелких млекопитающих с применением многомерного дисперсионного анализа выявило влияние на изменчивость места обитания (R-Рао10,42 = 1,897, p < 0,07), вида животных (R-Рао20,84 = 2,634, p < 0,001) и взаимодействия факторов (R-Рао20,84 = 2,106, p < 0,01).
Концентрация эритроцитов, гемоглобина и гематокрит в крови, традиционно используемые при оценке состояния среды, у животных с загрязненной территории существенно не изменяются, лишь у красной полевки больше эритроцитов (11,9 против 8,4 млн/мкл в контроле, p < 0,01). Однако во всех выборках животных изменяется размерный состав, структура и свойства эритроцитов, что более важно в оценке патологических нарушений. Так, у домовых мышей с импактного участка (рисунок, а) кривая распределения эритроцитов сдвинута в сторону клеток большего диаметра (R-Рао14,11 = 57,185, р < 0,001), что указывает на появление в крови молодых клеточных форм. Эритроциты этих мышей бо́льшего диаметра и меньшей толщины (7,2 против 5,3 мкм и 1,3 против 2,4 мкм, р < 0,05), что делает их более стойкими в изотонических растворах, существенно возрастает (213 % от контроля) способность переносить кислород единицей объема крови.
У лесных мышей с ВУРСа отмечена тенденция к изменению параметров эритроцитов, увеличивается дисперсия размерного состава (рисунок а). У красной полевки при некотором сдвиге кривой в сторону клеток меньшего диаметра эритроциты меньшего (p < 0,05) объема (46 против 79 мкм3), с меньшим содержанием гемоглобина (15 против 22 пг) по сравнению контрольными животными и мышами (лесной и домовой), несколько меньше, чем у контрольных (p > 0,05) средний диаметр (5,7 против 6,2 мкм) и площадь поверхности (63 против 75 мкм2), меньше и диапазон 16, 50 и 84 % гемолиза эритроцитов (0,51–0,46 % против 0,57–0,41 % NaCl у лесной мыши). Можно полагать, что поддержание дыхательной функции крови у красной полевки при измененной структуре и функции клеток компенсирует возросшее число эритроцитов.
 б
б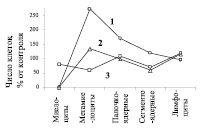
Клеточный состав (% от контроля) эритроцитов (а) и лейкоцитов (б) в крови мышей домовой (1), лесной (2) и красной полевки (3)
Концентрация лейкоцитов между контрольными и импактными выборками животных не различается, лишь у животных с импакта заметна тенденция к возрастанию. Однако в формуле крови отмечен сдвиг влево (рисунок б) и в большей мере у домовой мыши (юных 1,88 против 0,69 %, палочкоядерных нейтрофилов 5,38 против 3,18 %, р < 0,05), при этом возросло общее число нейтрофилов (23,6 против 17,2 %). У лесной мыши и красной полевки с импактной территории нейтрофилов в крови меньше, чем у контрольных животных (28,8 против 43 % и 21,9 против 29,4 %, соответственно).Для суждения о состоянии кроветворения более весомый лимфоцитарно-нейтрофильный показатель, чем общее число лейкоцитов в крови [2]. Величина его у домовых мышей с импакта ниже (2,43 против 3,52), у лесной мыши и красной полевки выше (1,1 против 2,0 и 2,0 против 3,1, соответственно), чем у контрольных особей, что можно связать с особенностями ответной реакции кроветворной системы у этих животных.
Исследуя параметры костного мозга и селезенки установлено, что кроветворная функция костного мозга зависит от места обитания (R-Рао24,15 = 2,55, р < 0,03) и вида животных (R-Рао24,15 = 6,33, р < 0,001). У домовых мышей с загрязненной территории концентрация клеток в костном мозге несколько выше (12,8 против 11,5 млн/бедро) и существенно выше в селезенке (123 против 65 млн/мг массы органа контрольных особей, р < 0,05), что, по-видимому, обусловлено активацией лейкопоэза и в большей мере эритропоэза (рисунок), в пользу которого свидетельствует снижение лейко-эритроцитарного профиля (2,4 против 3,5). У красной полевки в условиях загрязненной среды масса и клеточность селезенки составляют 58 % от контрольных значений, клеток костного мозга – 66 %, у лесной мыши соответственно 131, 119 и 117 %.
Исследование парциальной миелограммы выявило возрастание у лесных мышей (в 3 раза) и красной полевки (в 2 раза) с импактной территории митотической активности в эритроидном ряду (уровень ее у лесных мышей в 3 раза выше), у красной полевки в миелоидном ряду (в 1,6 раза). У лесных мышей с импактной территории больше, чем с контрольной (при p ≤ 0,05) базофильных нормобластов (в 2 раза) и миелобластов (в 1,4 раза), ретикулярных клеток (в 3 раза) способных регенерировать костный мозг, несколько выше (в 1,6 раза) индекс созревания эритроцитов (отношение орто– и поли– хроматофильных к базофильным нормобластам). У красной полевки в отличие от лесной мыши индекс созревания эритроцитов несколько ниже, чем в контрольной выборке (в 1,2 раза), но выше, чем у лесных мышей (p ≤ 0,05) индекс созревания нейтрофилов (отношение миелобластов, промиелоцитов, миелоцитов и метамиелоцитов к палочко- и сегменто- ядерным) за счет меньшего числа палочко- и сегменто-ядерных форм. Снижение лейко-эритроцитарного профиля у лесных мышей и красной полевки с импактной территории, и в большей мере у последней, свидетельствует о подавлении миелоидного ростка. При этом у красной полевки число лимфобластов превышает таковое у лесных мышей (2,21 против 0,88 %, p ≤ 0,05), что вероятно направлено на увеличение реактивности лимфоцитарного звена иммунной системы. Увеличение митотической активности и снижение числа зрелых клеток у лесной мыши и красной полевки с импактной територии указывает на задержку созревания нейтрофилов в костном мозге и снижение их в крови (28,8 против 43 % и 21,9 против 29,4 % контрольных, соответственно), у домовых мышей их выход в кровь (23,6 против 17,2 %), можно полагать, функционально неполноценных клеток.
Заключение
Наблюдаемые количественно-структурные изменения в крови и кроветворных органах у исследованных видов мелких млекопитающих даже в условиях столь низкого радиационного загрязнения среды можно расценивать как проявление компенсаторных возможностей кроветворной системы в ответ на возросшие функциональные нагрузки. Ответная реакция крови и кроветворных органов не одинакова: поддержание дыхательной функции крови у домовой мыши протекает по пути структурных изменений эритроцитов, у красной полевки за счет их количества, у лесной мыши поддерживается активное состояние кроветворения. Понять причину разной изменчивости параметров системы крови позволяет различная концентрация накопленных радионуклидов, у лесных мышей и красной полевки связанная скорее с различным типом их питания. Как более токсичный 90Sr по сравнению с 137Cs локализующийся в костной ткани и в бо́льших количествах у красной полевки, действует на костный мозг и подавляет радиочувствительную кроветворную ткань.
Работа выполнена при поддержке программы Президиума РАН, проект № 12-П-4-1068, № 12-С-4-1012.



