Комплексные соединения редкоземельных элементов (РЗЭ) вызывают большой научный интерес в плане их применения в современных технологиях и оптоэлектронике. Полимеризация комплексов позволяет получить новые полимеры и композиции на их основе, что приводит к улучшению многих свойств, присущих мономерам, и к получению новых перспективных характеристик. Способность соединений лантаноидов (III) образовывать разнообразные полимеры позволяет разрабатывать новые системы с заданными свойствами, отличающимися от свойств низкомолекулярных аналогов [2, 3].
Изучение структурных и электронных характеристик физико-химическими методами позволяет описать механизмы электронного возбуждения и фотохимических процессов в данных наноразмерных системах, что связано с необходимостью получения новых наноструктурированных оптических материалов для современных устройств контроля [6, 7]. Геометрическая и электронная структура и спектральные характеристики полимеров на основе комплексов РЗЭ изучены недостаточно, поэтому исследования строения кластеров комплексных соединений являются актуальными.
Целью настоящей работы является теоретическое физико-химическое исследование методом функционала плотности (DFT) реакционной способности и электронного строения наноструктурированного метакрилата иттрия (III) Y(Macr)3 (Macr – метакрилат-анион, CH2CH(CH3)COO–).
Материалы и методы исследования
Квантово-химические расчеты фрагментов Y2(Macr)6·(H2O)4 выполнены в вакуумном приближении методом DFT/TDDFT с функционалом PBE0 [1] с помощью программ GAMESS-US (версия 05.12.2014) [13] и FireFly 8.1.1 (b9295) [4]. Для атома иттрия использован Штутгартский псевдопотенциал и базис ECP28MWB(Y) [11], для других атомов взят базис 6-31G(d,p). При оптимизации геометрии в качестве начального приближения взята экспериментальная геометрия аналогичного комплекса лантана (III) [10], минимум энергии проверялся по гессиану. Дисперсионные поправки учтены по методу Гримме DFT-D3 [5]. Результаты расчетов визуализированы с помощью программы Chemcraft 1.8 (b486) [14].
Граничные молекулярные орбитали (МО), верхняя занятая МО (ВЗМО) и нижняя вакантная МО (НВМО), позволяют оценить реакционную способность и кинетическую устойчивость молекулы. ВЗМО связана со способностью системы отдать электрон, а НВМО – со способностью принять электрон. Индексы реакционной способности определяются соотношениями: I = –εВЗМО, A = –εНВМО, χ = (εВЗМО + εНВМО)/2, µ = –χ, η = (εНВМО – εВЗМО)/2, s = 1/(2η), w = µ2/(2η), где εВЗМО и εНВМО – энергии ВЗМО и НВМО, I – потенциал ионизации, A – сродство к электрону, χ – электроотрицательность, µ – химический потенциал, η – жесткость, s – мягкость, w – общий индекс электрофильности [9, 12]. Большая энергетическая щель ВЗМО–НВМО характеризует высокую химическую стабильность соединения. Химическая жесткость η молекулы определяется её сопротивлением деформации из-за электрического поля и эффекта химических реакций. Рост η связан с увеличением стабильности и снижением реакционной способности. Жесткое соединение имеет большую щель ВЗМО–НВМО, поэтому молекула с наименьшей щелью ВЗМО–НВМО имеет наибольшую реакционную способность. Большое значение химической мягкости s свидетельствует о высокой поляризуемости молекулы. Общий индекс электрофильности w соединения определяется энергией стабилизации при приеме дополнительной электронной плотности и характеризует электронный перенос и стабильность, поэтому он хорошо описывает общую реакционную способность соединения [12].
Результаты исследования и их обсуждение
Для квантово-химического моделирования наноструктурированного метакрилата иттрия (III) из экспериментальной структуры аналогичного комплекса лантана (III) (рис. 1) [10] было взято звено полимера – фрагмент, содержащий два иона РЗЭ, шесть метакрилат-анионов и четыре молекулы воды (рис. 2, а).
Метакрилат-анионы фрагмента Y2(Macr)6·(H2O)4 можно условно разделить на два типа: бидентантные, связанные с одним ионом РЗЭ (например, метакрилат-анион с атомами углерода C9–C10), и мостиковые, связанные с двумя ионами РЗЭ (C17–C18).
Звенья полимера связаны мостиковыми метакрилат-анионами и водородными связями между метакрилат-анионами и молекулами воды, полимерные цепочки в слое расположены параллельно и связаны водородными связями и межмолекулярным взаимодействием. Соседние слои также связаны водородными связями и межмолекулярным взаимодействием. Полимерные цепочки соседних слоев взаимно перпендикулярны. Оптимизированная геометрическая структура звена Y2(Macr)6·(H2O)4 показана на рис. 2, а.
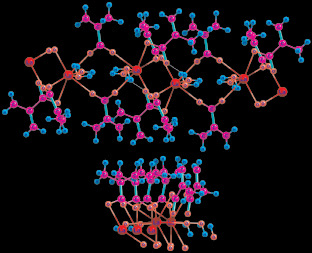
Рис. 1. Экспериментальная геометрическая структура Lan(Macr)m·(H2O)k [10]
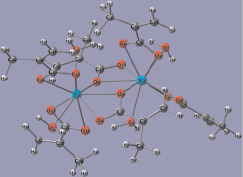
а
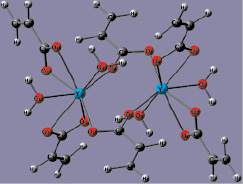
б
Рис. 2. Оптимизированный фрагмент Y2(Macr)6·(H2O)4 (а), Y2(Acr)6·(H2O)4 [8] (б)
Некоторые параметры его геометрии и электронного строения приведены в табл. 1. Для сравнения приведены данные для фрагмента Y2(Acr)6·(H2O)4 (Acr – акрилат-анион) (рис. 2, б, табл. 1) [8]. Согласно расчетам комплексов Y2(Macr)6·(H2O)4 и Y2(Acr)6·(H2O)4 (рис. 3, табл. 2), при переходе от акрилата к метакрилату иттрия (III) граничные МО дестабилизируются (ВЗМО – на 0,449 эВ, НВМО – на 0,164 эВ).
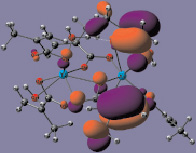
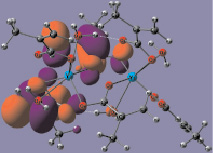
ВЗМО НВМО
Рис. 3. Граничные МО фрагмента Y2(Macr)6·(H2O)4
Таблица 1
Рассчитанные длины связей (Å), заряды на атомах (по Малликену), дипольный момент µ (Д) фрагментов Y2(Macr)6·(H2O)4 и Y2(Acr)6·(H2O)4
|
Y2(Mac)6·(H2O)4 |
Y2(Acr)6·(H2O)4 а |
|||||||
|
Длины связей |
Заряды на атомах |
Длины связей |
Заряды на атомах |
|||||
|
Связь |
Расчет |
Эксп.б |
Атом |
Заряд |
Связь |
Расчет |
Атом |
Заряд |
|
Y1–Y2 |
3,973 |
– |
Y1 |
0,88 |
Y1–Y2 |
3,940 |
Y1 |
0,89 |
|
Y1–O7 |
2,362 |
– |
Y2 |
0,85 |
Y1–O7 |
2,367 |
Y2 |
0,88 |
|
Y1–O8 |
2,422 |
– |
O7 |
–0,53 |
Y1–O8 |
2,477 |
O7 |
–0,54 |
|
O7–C9 |
1,257 |
1,254 |
O8 |
–0,63 |
O7–C1 |
1,265 |
O8 |
–0,59 |
|
O8–C9 |
1,284 |
1,260 |
C9 |
0,71 |
O8–C1 |
1,272 |
C1 |
0,65 |
|
C9–C10 |
1,492 |
1,507 |
C10 |
0,04 |
C1–C2 |
1,485 |
C2 |
–0,16 |
|
C10–C11 |
1,336 |
1,330 |
C11 |
–0,30 |
C2–C3 |
1,333 |
C3 |
–0,27 |
|
C10–C12 |
1,498 |
1,444 |
C12 |
–0,47 |
Y1–O3 |
2,375 |
O3 |
–0,53 |
|
Y1–O10 |
2,365 |
– |
O9 |
–0,60 |
Y1–O9 |
2,512 |
O9 |
–0,61 |
|
Y1–O9 |
2,514 |
– |
O10 |
–0,56 |
Y2–O9 |
2,292 |
C4 |
0,71 |
|
Y2–O9 |
2,421 |
– |
C17 |
0,69 |
O3–C4 |
1,251 |
C5 |
–0,16 |
|
O10–C17 |
1,265 |
1,245 |
C18 |
0,02 |
O9–C4 |
1,287 |
C6 |
–0,27 |
|
O9–C17 |
1,277 |
1,283 |
C19 |
–0,30 |
C4–C5 |
1,477 |
µ |
0,00 |
|
C17–C18 |
1,487 |
1,500 |
C20 |
–0,43 |
C5–C6 |
1,333 |
– |
– |
|
C18–C19 |
1,337 |
1,333 |
µ |
1,69 |
– |
– |
– |
– |
Примечание. а данные работы [8]; б данные для фрагмента La2(Macr)6·(H2O)4 [10].
Это свидетельствует о росте тенденции к отдаче электрона, а не к его присоединению. Щель ВЗМО–НВМО сужается на 0,285 эВ, приводя к снижению жесткости на 0,142 эВ, электрофильности на 0,282 эВ и к росту химического потенциала на 0,306 эВ, вызывая снижение стабильности и увеличение реакционной способности. Более высокая реакционная способность системы Y2(Macr)6·(H2O)4 относительно Y2(Acr)6·(H2O)4 также подтверждается искаженной геометрической структурой звена полимерной цепочки и ростом полярности системы (дипольный момент изменяется от 0 до 1,69 Д). Рост мягкости s на 0,007 эВ–1 также характеризует повышение поляризуемости системы при переходе акрилат → метакрилат.
Таблица 2
Рассчитанные энергии граничных МО εi, щель ВЗМО–НВМО Δε и параметры реакционной способности метакриловой кислоты и фрагментов Y2(Macr)6·(H2O)4 и Y2(Acr)6·(H2O)4
|
Параметры |
HMacr а |
Y2(Macr)6·(H2O)4 |
Y2(Acr)6·(H2O)4 б |
|
εВЗМО, эВ |
–7,589 |
–7,298 |
–7,747 |
|
εНВМО, эВ |
–0,933 |
–1,001 |
–1,165 |
|
Δε = εНВМО – εВЗМО, эВ |
6,656 |
6,297 |
6,582 |
|
I = – εВЗМО, эВ |
7,589 |
7,298 |
7,747 |
|
A = – εНВМО, эВ |
0,933 |
1,001 |
1,165 |
|
μ = –(I + A)/2, эВ |
–4,261 |
–4,150 |
–4,456 |
|
η = (I – A)/2, эВ |
3,328 |
3,149 |
3,291 |
|
s = 1/(2η), эВ–1 |
0,150 |
0,159 |
0,152 |
|
ω = µ2/(2η), эВ |
2,728 |
2,735 |
3,017 |
Примечание. а HMacr – метакриловая кислота, CH2CH(CH3)COOH; б [8].
Расчеты методом DFT колебательных спектров комплекса Y2(Macr)6·(H2O)4 показали, что колебания, связанные с ионом РЗЭ, лежат в области 50–250 см–1. Наличие кристаллической воды в полимерной структуре комплекса приводит к появлению в колебательных спектрах значительного числа полос, связанных с молекулами воды и водородными связями, что создает сложности при интерпретации спектров комплекса метакрилата иттрия (III).
Согласно расчетам методом TDDFT, в УФ спектрах Y2(Macr)6·(H2O)4 электронное поглощение, наблюдаемое в УФ области, близкой к вакуумной (215–232 нм), определяется синглет-синглетными переходами метакрилат-анионов, при этом энергии триплетных уровней анионов не соответствуют излучательным уровням ионов РЗЭ. Таким образом, метакрилат-анионы, обеспечивая полимерную структуру системы [2, 3], проявлять антенный эффект лишь для некоторых лантаноидов, соответствуя излучательным уровням ионов Ln3+. Благодаря полимерной сетке, комплекс метакрилата иттрия (III) может служить основой для получения новых материалов с перспективными функциональными свойствами.
Выводы
Метакрилат иттрия (III) имеет меньшую электрофильность и стабильность, большую поляризуемость и реакционную способность, чем акрилат иттрия (III). Метакрилат-анионы, обеспечивая полимерную структуру системы, проявляют антенный эффект лишь для некоторых ионов лантаноидов, соответствуя излучательным уровням ионов Ln3+. Благодаря полимерной сетке, метакрилат иттрия (III) может служить основой для получения материалов с перспективными функциональными свойствами.
Работа проводилась при финансовой поддержке Министерства образования и науки Российской Федерации в рамках государственного контракта № 2014/36 с Дальневосточным федеральным университетом (проект № 1137).
Библиографическая ссылка
Харченко В.И., Курбатов И.А., Чередниченко А.И., Алексейко Л.Н. РЕАКЦИОННАЯ СПОСОБНОСТЬ И ЭЛЕКТРОННОЕ СТРОЕНИЕ МЕТАКРИЛАТА ИТТРИЯ (III): ИССЛЕДОВАНИЕ МЕТОДОМ ФУНКЦИОНАЛА ПЛОТНОСТИ // Успехи современного естествознания. 2016. № 4. С. 62-66;URL: https://natural-sciences.ru/ru/article/view?id=35863 (дата обращения: 02.06.2026).



