Никель- и медьсодержащие сульфидные руды обычно перерабатываются флотацией с получением концентратов, которые затем подвергаются высокотемпературной обработке. Альтернативные технологии, такие как бактериально-химическое выщелачивание (биовыщелачивание), обладают потенциалом для снижения капитальных и эксплуатационных затрат на переработку подобного сырья. Необходимость получения экономически приемлемого концентрата для плавки часто приводит к значительным потерям ценных металлов в процессе флотации. Преимуществом процесса биовыщелачивания является то, что с его помощью могут быть эффективно переработаны более низкосортные флотоконцентраты и, соответственно, достигнуты более высокие показатели извлечения целевых металлов. Бедные руды и отвалы чаще всего выщелачивают кучным способом, для богатых руд и концентратов предпочтительно использование чанового (реакторного) биовыщелачивания.
За последние полвека были разработаны и усовершенствованы различные технологии биовыщелачивания разнообразного по составу сырья и извлечения из него таких ценных компонентов, как медь, никель, цинк, золото [1–3]. Они включают проекты, отработанные как на лабораторном, укрупненном лабораторном, так и на пилотном (полупромышленном) уровнях [4, 5]. Однако до промышленной реализации доходят немногие из них. Для успешного внедрения в промышленный процесс технология чанового биовыщелачивания должна обеспечивать максимум извлечения целевого компонента при минимуме времени, затрачиваемого на переработку руды или концентрата.
В то время как чановое биовыщелачивание никелевых и медных концентратов с использованием различных микробных культур изучено уже достаточно широко [4, 5], данных о биогидрометаллургической переработке полиметаллических медно-никелевых руд и концентратов относительно мало [6].
В Научно-исследовательском геотехнологическом центре Дальневосточного отделения Российской академии наук разрабатываются основы биогеотехнологии переработки сульфидных медно-никелевых руд с применением автохтонных сообществ хемолитотрофных ацидофильных микроорганизмов. В данной статье рассмотрены результаты исследования биовыщелачивания сульфидной кобальт-медно-никелевой руды месторождения Шануч в непрерывном режиме. Целью настоящей работы было определение оптимальной скорости протока пульпы в укрупненной биореакторной установке проточного типа в процессе бактериально-химического выщелачивания сульфидной кобальт-медно-никелевой руды в мезофильных условиях при плотности пульпы Т:Ж 1:5.
Материалы и методы исследования
В работе использована сульфидная кобальт-медно-никелевая руда месторождения Шануч степени измельчения 100 % – 125 мкм. Содержание рудных минералов в руде – 60–65 %, из которых на долю пирротина приходится 85–90 %, пентландита – 5–6 %, халькопирита – 2–5 %, виоларита – 0,2–0,5 %. Содержание металлов в руде: 4,79 % Ni; 0,75 % Cu; 0,12 % Co.
В качестве микробного инокулята использовали автохтонную мезофильную ассоциацию хемолитотрофных бактерий, выделенную авторами из зоны окисления месторождения Шануч, культивируемую в жидкой питательной среде Сильвермана и Люндгрена без железа 0К ((NH4)2SO4 – 3 г/л; KCl – 0,1 г/л; K2HPO4•3H2O – 0,65 г/л; MgSO4•7H2O – 0,5 г/л; CaNO3•4H2O – 0,01 г/л) при 30 °С и последовательно адаптированную к плотностям пульпы (Т:Ж) 1:20, 1:10, 1:5 в условиях реактора с механическим перемешиванием. Дополнительного внесения в питательную среду источника энергии для данной микробной культуры не требовалось, так как таким источником служили сульфидные соединения, содержащиеся в кобальт-медно-никелевой руде. По данным молекулярно-генетического анализа (ПЦР в реальном времени), в состав ассоциации входили преимущественно бактерии Acidithiobacillus ferrooxidans, Sulfobacillus spр.
Экспериментальные исследования процесса биовыщелачивания проводили на укрупненной биореакторной установке проточного типа, сконструированной и изготовленной научным сотрудником А.А. Балыковым. Схема установки представлена в работе [7]. В конструкции установки не использовались металлсодержащие материалы во избежание искажения результатов при проведении процессов биовыщелачивания. Установка состояла из контактного чана рабочим объемом 9 л, каскада из четырех последовательно соединенных биореакторов рабочим объемом 4,6 л каждый и приемной емкости для сбора пульпы на выходе из четвертого реактора. Контактный чан использовался для подготовки пульпы – смешивания твердой (измельченная сульфидная кобальт-медно-никелевая руда) и жидкой (питательная среда Сильвермана и Люндгрена 0К) фаз. В нем и биореакторах обеспечивалось механическое перемешивание пульпы мотор-редукторами, приводящими в движение двухлопастную мешалку, со скоростью 90–100 об/мин. В биореакторах поддерживалась температура 30 °С с помощью погруженных в пульпу терморегуляторов и аэрация пульпы со скоростью 2 л/мин с помощью воздушных компрессоров. Подача пульпы из контактного чана в первый реактор с регулируемой скоростью осуществлялась перистальтическим насосом переменной производительности. Перемещение пульпы из первого реактора в последующие происходило самотеком.
Перед запуском протока в первом реакторе вырастили бактериальную культуру. Для этого в него поместили 940 г руды и 4700 мл жидкой фазы, состоящей из 1175 мл инокулята (описанная выше автохтонная мезофильная ассоциация хемолитотрофных бактерий) и 3525 мл питательной среды 0К с рН 1,9. Таким образом, плотность пульпы Т:Ж составляла 1:5 по массе. Культивирование продолжали 20 сут.
На 21-е сутки в контактный чан поместили 1692 г руды и 8460 мл питательной среды 0К и запустили проток со скоростью 1,2 л/сут. Также в эксперименте использовали скорости протока пульпы 0,6 и 2,7 л/сут.
Результаты исследования и их обсуждение
Технология биовыщелачивания основана на окислительно-восстановительных процессах, протекающих в пульпе с участием хемолитотрофных (чаще всего ацидофильных) микроорганизмов – бактерий и архей. Источниками энергии для данных микроорганизмов служат двухвалентное (закисное) железо, элементарная сера и восстановленные соединения серы. Роль микроорганизмов в процессах биовыщелачивания заключается в окислении Fe2+ до Fe3+ (мощного окислителя сульфидов металлов), окислении элементной серы и восстановленных соединений серы, образовании серной кислоты, поддержании кислой реакции среды. В результате окисления соединений серы микроорганизмами высвобождаются протоны водорода, которые также способствуют извлечению металлов из кислоторастворимых сульфидов. Не растворимые в кислотах сульфиды подвергаются окислительному действию только ионов Fe3+ [8, 9].
Основными параметрами, отражающими кинетику биовыщелачивания, являются:
1) рН жидкой фазы пульпы;
2) окислительно-восстановительный потенциал (Eh) жидкой фазы пульпы как показатель интенсивности окислительно-восстановительных реакций, протекающих в пульпе;
3) концентрация клеток выщелачивающих микроорганизмов в 1 мл жидкой фазы пульпы как показатель роста биомассы;
4) концентрация окисного железа (Fe3+) в жидкой фазе пульпы – одного из основных окислителей сульфидных минералов;
5) концентрация суммарного железа (Feобщ) в жидкой фазе пульпы как показатель степени разрушения минералов;
6) концентрация целевого металла в жидкой фазе пульпы.
Значения перечисленных параметров в процессе биовыщелачивания сульфидной кобальт-медно-никелевой руды в непрерывном режиме при трех скоростях протока сведены в табл. 1. Из табл. 1 по динамике изменения рН и Eh в каскаде реакторов видно увеличение интенсивности окислительно-восстановительных процессов во втором и последующих реакторах по сравнению с первым. Количество бактериальных клеток в жидкой фазе пульпы при скоростях протока 0,6 и 1,2 л/сут постепенно увеличивается от первого к третьему реактору и снижается в четвертом. При скорости протока 2,7 л/сут прирост биомассы наблюдается только во втором реакторе. Вероятно, снижению концентрации бактерий в третьем и четвертом реакторах способствует вымывание клеток вследствие недостаточного времени нахождения пульпы в реакторах.
Наиболее интенсивный рост концентрации Fe3+ при скорости протока 0,6 л/сут происходит до третьего реактора. При 1,2 и 2,7 л/сут концентрация Fe3+ растет более равномерно, и при 2,7 л/сут она в среднем на 5 г/л ниже, чем при 1,2 л/сут. Очевидно, что при наименьшей плотности биомассы при 1,2 л/сут бактериальная культура обладала наибольшей железоокисляющей активностью, что способствовало и наибольшему извлечению никеля при данной скорости протока (рис. 1).
Из табл. 2 следует, что на выходе из четвертого реактора при скорости протока 1,2 л/сут продуктивный раствор имеет максимальную концентрацию никеля – 8,98 г/л, что соответствует максимальному извлечению данного металла – 93,6 %.
Динамика извлечения никеля представлена на рис. 1, на котором видно, что извлечение целевого металла при скорости протока 2,7 л/сут существенно ниже, чем при двух других исследованных скоростях. Разница в скоростях протока между 0,6 и 1,2 л/сут существенно влияет на извлечение никеля только в первом реакторе.
Таблица 1
Технологические параметры бактериально-химического выщелачивания сульфидной руды в непрерывном режиме при различных скоростях протока пульпы
|
Параметр |
Реактор |
Значения параметров при разных скоростях протока пульпы |
||
|
0,6 л/сут |
1,2 л/сут |
2,7 л/сут |
||
|
рН жидкой фазы пульпы |
I |
2,08 |
2,06 |
2,54 |
|
II |
1,75 |
1,73 |
2,14 |
|
|
III |
1,56 |
1,61 |
1,82 |
|
|
IV |
1,52 |
1,57 |
1,69 |
|
|
Среднее |
1,73 |
1,74 |
2,05 |
|
|
Eh жидкой фазы пульпы (мВ) |
I |
292 |
329 |
248 |
|
II |
367 |
397 |
317 |
|
|
III |
399 |
416 |
369 |
|
|
IV |
415 |
425 |
388 |
|
|
Среднее |
368 |
392 |
331 |
|
|
Концентрация бактериальных клеток в 1 мл |
I |
1,0×109 |
6,9×108 |
1,0×109 |
|
II |
1,5×109 |
1,1×109 |
1,8×109 |
|
|
III |
1,8×109 |
1,2×109 |
1,4×109 |
|
|
IV |
1,5×109 |
9,1×108 |
1,1×109 |
|
|
Среднее |
1,5×109 |
9,8×108 |
1,3×109 |
|
|
Концентрация Fe3+ (г/л) |
I |
1,06 |
4,94 |
0,50 |
|
II |
5,56 |
6,20 |
1,69 |
|
|
III |
10,49 |
8,44 |
3,60 |
|
|
IV |
11,70 |
10,91 |
5,16 |
|
|
Среднее |
7,20 |
7,62 |
2,74 |
|
|
Концентрация Feобщ (г/л) |
I |
3,93 |
5,57 |
1,06 |
|
II |
6,22 |
6,34 |
1,95 |
|
|
III |
10,76 |
8,54 |
3,68 |
|
|
IV |
11,87 |
10,97 |
5,18 |
|
|
Среднее |
8,20 |
7,86 |
2,97 |
|
|
Концентрация Ni2+ (г/л) |
I |
3,75 |
5,49 |
2,21 |
|
II |
6,27 |
6,56 |
3,67 |
|
|
III |
7,66 |
7,91 |
4,99 |
|
|
IV |
8,89 |
8,98 |
6,38 |
|
|
Среднее |
6,64 |
7,24 |
4,31 |
|
|
Пропускная способность (объем реактора/ч) |
0,005 |
0,011 |
0,024 |
|
|
Производительность по твердому (г/сут) |
100 |
200 |
450 |
|
|
Время нахождения пульпы в одном реакторе (сут) |
7,67 |
3,83 |
1,70 |
|
|
Время нахождения пульпы в каскаде реакторов (без контактного чана) (сут) |
30,67 |
15,33 |
6,81 |
|
Одним из основных параметров, определяющих экономическую рентабельность технологии бактериально-химической переработки руд и концентратов в реакторных установках проточного типа, является время нахождения пульпы в каскаде реакторов (residence time). Необходимо стремиться к увеличению скорости протока до такого значения, которое обеспечит максимальное извлечение целевого металла из выщелачиваемого сырья при минимальном residence time. На рис. 2 отображена зависимость извлечения никеля от residence time.
Выводы
Таким образом, скорость протока 0,6 л/сут соответствовала времени нахождения пульпы в каскаде реакторов 30,7 сут, 1,2 л/сут – 15,33 сут, 2,7 л/сут – 6,81 сут. По графику, представленному на рис. 2, очевидно, что оптимальная скорость протока пульпы для данной реакторной установки составляет 1,2 л/сут. При этом видно, что без существенной потери в степени извлечения никеля возможно сократить residence time до 13 сут, что будет соответствовать скорости протока 1,4 л/сут.
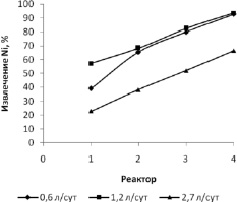
Рис. 1. Динамика извлечения никеля в процессе бактериально-химического выщелачивания сульфидной руды в непрерывном режиме при различных скоростях протока пульпы
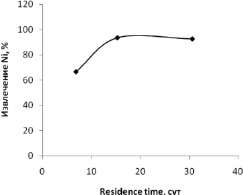
Рис. 2. Зависимость извлечения никеля от времени нахождения пульпы в каскаде реакторов (residence time)
Таблица 2
Извлечение никеля в процессе бактериально-химического выщелачивания сульфидной руды в непрерывном режиме при различных скоростях протока пульпы
|
Параметр |
Реактор I |
Реактор II |
Реактор III |
Реактор IV |
|
Скорость протока 0,6 л/сут |
||||
|
Концентрация Ni2+ (г/л) |
3,75 |
6,27 |
7,66 |
8,89 |
|
Извлечение Ni ( %) |
39,1 |
65,4 |
79,9 |
92,7 |
|
Скорость протока 1,2 л/сут |
||||
|
Концентрация Ni2+ (г/л) |
5,49 |
6,56 |
7,91 |
8,98 |
|
Извлечение Ni ( %) |
57,3 |
68,4 |
82,5 |
93,6 |
|
Скорость протока 2,7 л/сут |
||||
|
Концентрация Ni2+ (г/л) |
2,21 |
3,67 |
4,99 |
6,38 |
|
Извлечение Ni ( %) |
23,0 |
38,3 |
52,0 |
66,5 |
Можно выделить перспективные способы повышения эффективности биовыщелачивания сульфидной кобальт-медно-никелевой руды месторождения Шануч:
1) модернизация конструкции реакторов проточной установки в части улучшения массо- и газообмена путем оснащения реакторов вертикальными отбойниками пульпы (баффлами) на внутренних стенках, использования двойных мешалок в виде Раштон-турбин и увеличения скорости их вращения, а также перемещения точки подачи воздуха для аэрации пульпы под мешалку для более эффективного распределения пузырьков воздуха в пульпе;
2) использование умеренно термофильных и термофильных микроорганизмов, что позволит повысить температуру пульпы.
Библиографическая ссылка
Левенец О.О., Хайнасова Т.С., Балыков А.А. КИНЕТИКА БАКТЕРИАЛЬНО-ХИМИЧЕСКОГО ВЫЩЕЛАЧИВАНИЯ СУЛЬФИДНОЙ РУДЫ НА УКРУПНЕННОЙ БИОРЕАКТОРНОЙ УСТАНОВКЕ ПРОТОЧНОГО ТИПА ПРИ ТРЕХ РАЗЛИЧНЫХ СКОРОСТЯХ ПРОТОКА // Успехи современного естествознания. 2018. № 6. С. 96-101;URL: https://natural-sciences.ru/ru/article/view?id=36788 (дата обращения: 18.05.2026).
DOI: https://doi.org/10.17513/use.36788



