Введение
В 2021 г. в юго-восточной части Балтийского моря организована морская площадка карбонового полигона «Росянка» в рамках пилотного проекта Минобрнауки России (оператор – Балтийской федеральный университет им. И. Канта). Мониторинговые исследования направлены на оценку потоков парниковых газов в морской экосистеме в условиях региональных изменений климата. Данные о фотосинтетической способности фитопланктона необходимы для выявления влияния климатической и экологической изменчивости на фитопланктон и, как следствие, на скорость фотосинтетической фиксации углерода [1, 2]. Фотосинтетическая способность фитопланктона зависит от факторов среды, а также от внутриклеточных процессов, направленных на оптимизацию преобразования световой энергии в углеродную биомассу и предотвращение внутриклеточных повреждений [2]. Основным методом оценки фотосинтетической способности является измерение активной флуоресценции хлорофилла «а», позволяющее неинвазивно определять такие параметры, как максимальная квантовая эффективность фотосистемы II (Fv/Fm) и эффективная квантовая эффективность фотосистемы II (QY). Оба параметра характеризуют вероятность того, что поглощенный квант света инициирует реакцию, которая приводит к преобразованию энергии возбуждения/света в химическую энергию. Fv/Fm характеризует максимальную квантовую эффективность при оптимальных условиях, когда отсутствуют физиологические механизмы и внешние факторы, подавляющие фотосинтез, в то время как QY отражает фактическую квантовую эффективность при текущих условиях освещенности [3]. При благоприятных условиях и высокой активности фитопланктона значение QY будет максимально приближаться к значению Fv/Fm. Хорошо известно, что фотосинтетическая активность и светособирающие характеристики фитопланктона сильно различаются в зависимости от условий окружающей среды (в особенности фотосинтетически активной радиации (ФАР)) и сезонных циклов [3]. Поэтому физиологическое состояние фитопланктона является важнейшим фактором, регулирующим распределение фитопланктона и его первичную продуктивность в море. Предыдущие исследования показали, что Fv/Fm имеет ярко выраженную сезонную изменчивость [4, 5]. Однако лишь в немногих исследованиях измерялась QY [5, 6], а анализ соотношения Fv/Fm и QY для Балтийского моря не проводился.
Цель исследования – выявление сезонных особенностей и степени реализации фотосинтетической способности фитопланктона, а также анализ ее зависимости от факторов среды.
Материалы и методы исследования
Исследования выполнялись в период с 2022 по 2025 г. в российском секторе юго-восточной части Балтийского моря: в апреле 2025, мае 2023, июне 2024, июле 2022, июле 2025, августе 2024 и ноябре 2023. Количество проб для каждого месяца составляло от 6 до 15, максимальное количество проб отобрано в июле. Отбор проб воды осуществлялся гидрологическим комплексом MWS Slimline, оснащенным батометрами Нискина объемом 5 и 10 л. Данные по температуре (ºС), солености (ЕПС) и мутности (ЕМФ) были получены с помощью мультипараметрического зонда SAIV SD208. Концентрация хлорофилла «а» была получена с помощью погружного флуориметра Seapoint Chlorophyll Fluorometer, диапазон 0–75 мкг/л. ФАР (мкмоль фотонов/м2 в с) фиксировалась параллельно с измерениями активной флуоресценции подводным и надводным датчиками LI-190R и LI-192, и интегратора DataLogger LI-1500. Измерения параметров активной флуоресценции хлорофилла «а» проводились с помощью флуориметра WATER-PAM-II (Walz, Германия). Перед измерениями пробы выдерживались в темноте 20 мин [3]. QY и (Fv/Fm) являются безразмерными величинами и рассчитывались согласно методике, описанной в предыдущих работах [4, 7]. Степень реализации фотосинтетической способности фитопланктона в конкретных условиях рассчитывалась как отношение СРф = QY/(Fv/Fm). Анализ данных проводился для поверхностного слоя моря. Согласно проведенному нами тесту Шапиро – Уилка, показатели активной флуоресценции характеризуются ненормальным распределением, поэтому для анализа связи между переменными использовался метод корреляций Спирмена [8].
Результаты исследования и их обсуждение
Диапазон значений температуры воды в период исследований составил 5,3–21,3°C. Минимальные значения зафиксированы в апреле (5–8 °C), максимальные – в летний период (июнь – август: 16–21 °C). В ноябре значения температуры находились в пределах 8–11 °C. Значения солености в течение года изменялись незначительно с минимумом летом. Медианное значение составило 7,20 в диапазоне 6,65–7,67 ЕПС. Диапазон значений мутности составил 0,3–5,74 ЕМФ, медианное значение – 1,38 ЕМФ. Диапазон концентраций хлорофилла «а» составил 0,13–6,16, медианное значение – 0,945 мгк/л.
Сезонная динамика QY характеризовалась высокой вариабельностью (0,03–0,48; коэффициент вариации 15 %). Медианное значение составило 0,15. Наиболее низкие значения QY отмечены в апреле – мае, что могло быть связано с адаптацией фитопланктона к увеличению светового дня и низкой температурой воды, однако минимальное за период исследований значение отмечено в июне. Пик значений наблюдался в августе. Летом отмечен значительный разброс значений, который мог обуславливаться как оптимальными условиями освещения и температуры, так и периодическими стрессами (перегрев, сокращение концентрации/содержания биогенных веществ, угнетающий уровень ФАР). Более высокие значения были характерны для ноября, что могло быть связано с адаптацией фитопланктонного сообщества к низкой освещенности. Динамика Fv/Fm была схожа с динамикой QY, однако величины Fv/Fm были выше: медианное значение0,59, диапазон – 0,24–0,71. Максимум отмечен в апреле, повышенные значения установлены весной и осенью. В летние месяцы значения достигали минимума и в целом были ниже.
Степень реализации фотосинтетической способности (СРф) показала широкий диапазон значений (от 4 до 80 %) в различные месяцы (рисунок), что говорит о сезонной изменчивости способности фитопланктона реализовывать фотосинтетический потенциал.
Максимальная величина СРф (> 70 %) наблюдалась в ноябре при высоких значениях как Fv/Fm, так и QY. Однако известно, что количество первичной продукции, как и активного фитопланктона, минимально в этот период [9]. Очевидно, что, несмотря на высокую степень реализации квантовой эффективности, последующие этапы фотосинтеза были заторможены. Высокая фотосинтетическая активность также не отражает количество фитопланктона, поэтому не всегда определяет количество первичной продукции. Поэтому анализ реализации потенциала будет наиболее эффективным в случае комплексного рассмотрения с другими характеристиками фитопланктона. Летние месяцы характеризовались наименьшей величиной СРф (медианные значения 20–26 %), однако более широким диапазоном значений, что говорит о нестабильных для фитопланктона условиях в этот период. Низкая величина СРф летом определялась высоким Fv/Fm, но при этом крайне низким QY, что обуславливалось эффектом фотоингибирования под влиянием избыточной ФАР, а также лимитированием биогенных веществ [9]. Минимальное значение величины СРф было зафиксировано в мае (4 %), наименьшие медианные значения – в мае и августе (18–19 %).
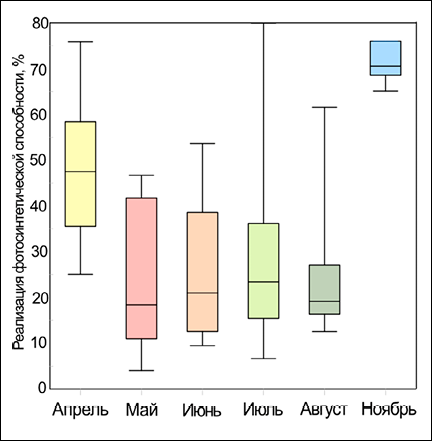
Распределение значений степени реализации фотосинтетической способности (СРф) в юго-восточной части Балтийского моря в 2022–2025 гг. с апреля по ноябрь: величина бара соответствует центральным 50 % значений, «усы» – минимальному и максимальному значениям, горизонтальная линия в баре – медианному значению Примечание: составлен авторами по результатам данного исследования
Примечателен высокий уровень величины СРф в апреле (медианные значения: 35–57 %). Оба параметра (QY и Fv/Fm) в этот месяц имели высокие значения, что говорит о высокой степени адаптации фитопланктона к условиям среды в этот период. Похожие результаты были получены для шельфовых вод Северной Атлантики, где QY достигал максимальных значений в апреле [5]. Авторы связывают это с «перезагрузкой» фотосинтетического аппарата после зимы: клетки имеют высокое содержание фотосинтетических пигментов и питательных веществ, что позволяет эффективнее использовать усиливающийся свет [6]. В исследовании пресноводного озера показано, что максимальные значения как Fv/Fm, так и QY также наблюдались в апреле: авторы предположили, что холодная вода способствует более высокой эффективности фотосинтетического аппарата, так как снижает метаболические затраты на «ремонт» и уменьшает тепловое рассеяние энергии. Весенние значения Fv/Fm были близки к теоретическому максимуму (0,7), подтверждая отсутствие значительного стресса [5]. Высокий уровень СРф в апреле подтверждается весенним пиком количества первичной продукции, который наблюдался в юго-восточной части Балтийского моря [9].
Для выявления влияния абиотических факторов на фотосинтетическую активность фитопланктона была проанализирована корреляция параметров активной флуоресценции с температурой поверхности воды, соленостью и ФАР (таблица).
Выявлена статистически значимая отрицательная корреляция между значениями Fv/Fm, QY и ФАР, что указывает на снижение параметров в случае избыточного освещения. Однако коэффициенты корреляции для Fv/Fm и QY значительно различались: так, эффект фотоингибирования слабо проявлялся в динамике Fv/Fm (корреляция с ФАР составила -0,3), однако был значительно заметен на изменении QY (корреляция с ФАР составила -0,8). Статистически значимая умеренная отрицательная корреляция была получена для значений QY и температуры (-0,38). Снижение QY на 0,37 при повышении температуры указывает на нарушение электронного транспорта при тепловом стрессе. Повышение тепловой диссипации избыточной энергии (до 80 вместо 5–10 % в оптимальных условиях) защищает фотосистемы, но снижает QY [10].
Выявлена также статистически значимая отрицательная корреляция между значениями Fv/Fm и мутности. Корреляция может быть объяснена хроническим стрессом клеток фитопланктона, которые могут испытывать резкие переходы между зонами высокой и низкой освещенности в турбулентных поверхностных мутных водах [10]. Высокая мутность также часто коррелирует с эвтрофикацией, поэтому снижение Fv/Fm при повышении мутности может свидетельствовать о хроническом стрессе фитопланктона из-за эвтрофикации: помимо уменьшения количества света изменяется спектральный состав освещения (увеличивается доля зеленого света, менее эффективного для фотосинтеза) [11]. Для прибрежных акваторий ранее было показано, что в эвтрофицированных водах высокая мутность коррелировала со снижением Fv/Fm на 30–50 % [12].
Значимой монотонной связи между параметрами флуоресценции и соленостью не обнаружено, что может быть связано с незначительной изменчивостью солености, не влияющей на фитопланктон в связи с осморегуляцией клеток. Высокая осмотическая толерантность многих морских микроводорослей, способных поддерживать фотосинтетическую активность, отмечалась ранее даже при значительных колебаниях солености [13]. Не обнаружено также связи хлорофилла «а» с параметрами активной флуоресценции. Таким образом, концентрация хлорофилла, получаемая с помощью зондового флуориметра, не дает информации о фотосинтетической активности, что может иметь как методологические, так и физиологические причины. Результаты согласуются с предыдущими комплексными исследованиями [14, 15], которые показали, что в смешанных фитопланктонных сообществах корреляция между хлорофиллом и фотосинтетическими параметрами часто слабая или отсутствует.
Коэффициенты корреляции Спирмена между фотосинтетическими параметрами и факторами среды
|
Параметр |
Температура, °C |
ФАР, мкмоль фот/м2 в с |
Соленость, ЕПС |
Мутность, ЕМФ |
Хл «а», мгк/л |
|
Fv/Fm |
-0,22; p = 0,06; n = 66 |
-0,33; p < 0,006; n = 66 |
0,13; p = 0,29; n = 66 |
-0,43; p = 0,003; n = 44 |
-0,076; p = 0,61; n = 44 |
|
QY |
-0,38, p = 0,0019; n = 66 |
-0,81; p < 0,0001; n = 66 |
0,06; p = 0,649; n = 66 |
-0,23; p = 0,116; n = 44 |
0,24; р = 0,102; n = 44 |
Примечание: составлен авторами на основе полученных данных в ходе исследования
Как показано в данной работе, мониторинг только Fv/Fm, являющегося консервативным показателем «здоровья» фотосинтетического аппарата фитопланктона, может не выявить текущего светового и теплового стресса. В то же время анализ только QY, значительно зависящий от мгновенного уровня ФАР, не дает информации об уровне адаптации фитопланктона к условиям среды. Таким образом, соотношение QY и Fv/Fm служит эффективным индикатором, позволяющим определить как кратковременное стрессовое воздействие среды, так и долговременную адаптацию фитопланктона к условиям обитания: высокие значения соотношения (> 60–80 %) указывают на эффективное использование поглощенной энергии, низкие значения (< 30–40 %) свидетельствуют о значительных потерях энергии на нефотохимическое тушение. Данный анализ позволяет оперативно оценить, в какой мере текущие условия среды позволяют фитопланктону реализовать свой фотосинтетический потенциал, что важно для понимания регуляции первичной продукции в юго-восточной Балтике, подверженной эвтрофированию и климатическим изменениям.
Заключение
В 2022–2025 гг. получены натурные данные о сезонной изменчивости фотосинтетической способности фитопланктона и степени ее реализации в юго-восточной части Балтийского моря, а также рассмотрены зависимости между параметрами фотосинтетической активности и абиотическими факторами. Установлено, что степень реализации фотосинтетической способности, выраженная через соотношение QY/Fv/Fm, была высокой в ноябре и апреле (медианные значения более 70 %), в периоды с умеренным уровнем ФАР, что связано с отсутствием теплового и светового стрессов. Низкий уровень реализации фотосинтетической способности отмечен в летние месяцы (медианные значения составили 20–26 %), что объясняется негативными эффектами эвтрофикации, истощением биогенных веществ, а также теплового и светового стрессов.
Значимых корреляций между параметрами флуоресценции, соленостью и хлорофиллом «а», измеренным с помощью погружного флуориметра, не было обнаружено. Однако установлена отрицательная зависимость значений Fv/Fm от значений мутности и температуры, что важно для оценки трофического статуса водоемов, так как данный параметр может стать эффективным индикатором «фонового здоровья» фитопланктона и подтверждать интенсивность эвтрофикации. Наиболее сильная отрицательная зависимость от ФАР была установлена для QY, что говорит о том, что показатель QY лучше отражает эффект фотоингибирования, чем Fv/Fm, что важно в рамках экологического мониторинга. Таким образом, для полноценного анализа состояния и продуктивности фитопланктона in situ необходимо одновременное использование обоих флуоресцентных параметров, а также сопоставление результатов с классическими методами измерения первичной продукции. Дальнейшей перспективой авторы также видят анализ влияния групп водорослей на показатели флуоресценции фитопланктона.
Конфликт интересов
Благодарности
Финансирование
Библиографическая ссылка
Боровкова К. А., Мошаров С. А. ИСПОЛЬЗОВАНИЕ АКТИВНОЙ ФЛУОРЕСЦЕНЦИИ ХЛОРОФИЛЛА «А» ДЛЯ ОЦЕНКИ РЕАЛИЗАЦИИ ФОТОСИНТЕТИЧЕСКОЙ СПОСОБНОСТИ ФИТОПЛАНКТОНА В ЮГО-ВОСТОЧНОЙ ЧАСТИ БАЛТИЙСКОГО МОРЯ // Успехи современного естествознания. 2026. № 3. С. 30-35;URL: https://natural-sciences.ru/ru/article/view?id=38486 (дата обращения: 14.05.2026).
DOI: https://doi.org/10.17513/use.38486



