Известно, что гуминовые соединения благодаря карбоксильным, карбонильным и ароматическим фрагментам обладают разносторонним связывающим потенциалом и вступают в ионные, донорно-акцепторные и гидрофобные взаимодействия. В работе [8] отмечено, что гуминовые кислоты в зависимости от рН среды и концентрации катионов вступают в разнообразные взаимодействия. Комплексообразование может протекать в двух режимах: первый режим предполагает связывание металлов фенольными гидроксилами и карбоксильными группами, а второй режим – только COOH-группами. В статье [7] исследованы сорбционные свойства двухвалентных Mе2+ (Cu, Pb и Zn) и трехвалентных катионов Mе3+ (Fe, Al) с гуминовыми кислотами из окисленных углей (Хазро, Турция) в водном растворе. Изучено влияние рН, концентрации ионов металлов и гуминовых кислот на процесс взаимодействие металла с гуминовыми кислотами. Установлена, что сорбционная способность гуминовых кислот возрастает с ростом рН и концентрации гуминовых кислот, уменьшается при повышении концентрации металлического иона. Авторами работы [1] изучена зависимость степени извлечения ионов Fe3+ , Cu2+ , Ni2+ и Zn2+ от расхода гуматов калия, натрия и аммония при рН 2–3 для различных концентрациях указанных солей и определены оптимальные расходы сорбента. Установлено, что при взаимодействии катионов железа с гуматами достигается высокая степень очистки воды (до 99 %), тогда как катионы меди, никеля и цинка связываются с гуматами слабее (до 80 %).
Таким образом, гуминовые соединения способны связывать различные классы экотоксикантов, они являются своеобразными посредниками, смягчающими действие токсинов на живые организмы. Поэтому изучение их комплексообразющих свойств с металлами вызывает несомненный интерес.
Цель исследования
Установить влияние нормы солей цинка на процесс комплексообразование в гетерогенной системе «сульфат цинка – гумат натрия».
Материалы и методы исследования
В работе использовался гумат натрия, следующего состава, мас. %: выход гуминовых кислот – 55,14; влажность – 19,15; зольность – 37,48; содержание карбоксильных групп – 0,8754 мг-экв, содержание фенольных гидроксильных групп – 1,9866 мг-экв. Опыты осуществляли при постоянном значении концентрации гумата натрия – 1,0 %, времени – 60 мин и температуры – 20ºС.
Запись инфракрасных спектров поглощения производили на двухлучевом спектрофотометре «Specord M-80» в области 200-4000 см-1. Выход гуминовых кислот в исследуемых образцах определяли по ГОСТ 9517-76, содержание функциональных групп – по методике [2].
Результаты исследования и их обсуждение
В ходе проведенных работ установлено (табл. 1), что повышение нормы сульфата цинка приводит к уменьшению выхода гуминовых веществ. Например, при температуре 20оС через 60 мин взаимодействия 1 % раствора гумата натрия с 0,5 г сульфата цинка выход гуминовых веществ составляет 52,12 %, а при взаимодействии с 2,5 г уменьшается до 29,02 %.
Наличие в макромолекуле гуминовых соединений множества атомных группировок и их взаимное расположение, а также большой набор различающихся по степени кислотности функциональных групп позволяет отнести гуминовых веществ к полидентатным лигандам [3–5]. Известно, что гуминовые соединения образуют комплексы с ионами d-переходных металлов [6]. Характерным для процесса комплексообразования является смещение рН в кислую сторону. Полученные результаты показали, что с увеличением нормы сульфата цинка происходит снижение рН от 7,23 до 6,84 (табл. 1). Это свидетельствуют об образовании комплексных соединений гуминовых веществ с ионами цинка.
Таблица 1
Влияние нормы сульфата цинка на характеристику полученных образцов
|
Норма сульфата цинка, г |
рН |
Выход гуминового вещества, % |
|
0,5 1,0 1,5 2,0 2,5 |
7,23 7,10 6,95 6,90 6,84 |
52,12 49,12 41,66 35,18 29,02 |
Экспериментальные данные свидетельствуют (рис. 1), что с ростом нормы сульфата цинка от 0,5 до 2,5 г количество связанного с гуминовой кислотой цинка увеличивается. Так, при взаимодействии 1 % раствора гумата натрия в течение 60 мин с сульфатом цинка при температуре 20 оС количество связанного цинка увеличивается от 6,09 до 10,18 г-экв.
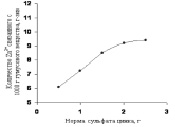
Рис. 1. Зависимость количества связанного с гуминовой кислотой цинка от нормы сульфата цинка
Как видно из табл. 2, увеличение нормы сульфата цинка приводит к уменьшению содержания связанных с цинком карбоксильных групп. Например, при взаимодействии гумата натрия с 0,5 г сульфата цинка количество связанных с цинком карбоксильных групп составляет 0,4371 мг-экв (49,93 %), а с 2,5 г – 0,1707 мг-экв на 100 г органической массы (19,50 %). В указанных условиях содержание замещенных цинком фенольных гидроксильных групп возрастает от 0,4449 до 0,7533 мг-экв на 100 г органической массы (от 22,39 до 37,92 %).
Результаты ИКС (рис. 2) свидетельствует, что с увеличением нормы сульфата цинка интенсивность полос поглощения исследуемых образцов усиливается. Широкие полосы поглощения в области 3420–3410 см–1 соответствуют валентным колебаниям гидроксильных групп, дублет в области 2920–2910 и 2810–2800 см-1 относятся к валентным колебаниям –СН3- , –СН2- и СН-групп алифатических структур, сильные колебания при 1590–1580 и 1390–1380 см-1 – валентным колебаниям карбоксилатных групп, при 1130–1120 и 1050–1040 см-1 – деформационным и валентным колебаниям С-О-групп спиртов. Широкие полосы средней интенсивности в области 3200 см-1 характерны для валентных колебаний ОН-групп в хелатных соединениях, а полосы при 830–820 и 620–605 см-1 подтверждает образование связи Ме-О в комплексах гуминовых соединений, их интенсивность с повышением нормы сульфата цинка увеличивается.
Таблица 2
Изменение содержания функциональных групп в зависимости от нормы сульфата цинка
|
Норма сульфата цинка, г |
Содержание кислых групп, мг-экв/г |
||
|
СООН |
ОНфен. |
СООН+ОНфен. |
|
|
0,5 1,0 1,5 2,0 2,5 |
0,4383 0,5007 0,5311 0,5647 0,7047 |
1,5417 1,4593 1,4189 1,3753 1,2333 |
1,9800 1,9600 1,9500 1,9400 1,9380 |
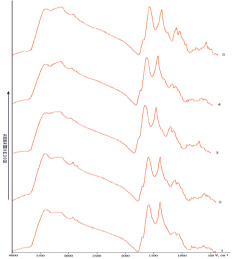
Рис. 2. ИК-спектры полученных образцов: продукты, полученные при разной норме сульфата цинка (II), г: 1 – 0,5; 2 – 1; 3 – 1,5; 4 – 2,0; 5 – 2,5
Выводы
Результаты проведенных работ свидетельствуют, что повышение нормы сульфата цинка способствуют уменьшению выхода гуминовых кислот и увеличению количества связанного с гуминовой кислотой цинка. Данные функционального анализа показывают, что увеличение нормы сульфата цинка приводит к снижению содержание связанных с цинком карбоксильных групп и к увеличению замещенных цинком фенольных гидроксилов. Методом ИКС подтверждено образование комплексных соединений гуминовых веществ с цинком.



