Интерес к использованию фитоэкистероидов, как адаптогенов растительного происхождения, с годами не только не снижается, а только возрастает. Адаптогены – это вещества, способствующие приспособлению, адаптации. Биорегуляторы в форме фитоэкдистероидов способствуют включению синтоксических программ адаптации с параводом клеточного метаболизма на более низкий уровень, определяющий экономичность обменных процессов, создавая условия для одновременного протекания анаэробного и аэробного окисления. Включение синтоксических адаптивных программ позволяет организму сопереживать с раздражителями внешней и внутренней среды путём активации холинореактивных структур гипоталамуса с дальнейшей активацией антиоксидантных и противосвёртывающх механизмов крови и явлениями иммуносупрессии. Недостаточное выделение синтоксинов в организме животных (АМФГФ, ТБГ и др.) сопровождается соответствующими патологическими процессами или к доминированию кататоксических программ адаптации, также оказывающих негативное влияние на организм, а введение синтоксинов нормализует баланс программ адаптаций и способствует нормализации всех процессов и возрастанию жизнеспособности организма в целом (5). В ходе научных экспериментов постоянно расширяется спектр положительного воздействия экдистероидов на организмы теплокровных.
Экдистероиды – это группа липофильных полигидроксилированных стероидов, участвующих в обмене веществ практически всех организмов (8). У насекомых они являются гормонами линьки, у человека – регулируют множество функций и оказывают различные эффекты: анаболический, ранозаживляющий, ноотропный, гипогликемический, иммуномодулирующий и др. (6). Важным представителем экдистероидов является экдистерон, обладающий основными эффектами, присущими данному классу соединений, и достаточно широко распространенный в растениях центральной полосы России. Например, экдистерон обладает выраженным актопротекторным эффектом, также отмечено его антигипоксическое и антиишемическое действие (7), позволяет добиться стихания воспалительного процесса в более ранние сроки по сравнению с традиционным лечением нагноительных заболеваний лёгких и плевры (3). Экдистероиды обнаружены у представителей более 100 семейств покрытосеменных растений, но лишь немногие виды экдистероидсодержащих растений пригодны в качестве сырья для получения фитоэкдистероидов (1).
Цель исследования – проанализировать химический состав ушанки мелкоцветковой (Otites parviflorus Grossh.) семейства гвоздичных (Caryophyllaceae Juss.) на наличие полифенольных и стероидных соединений, изучить актопротекторную активность экстракта ушанки мелкоцветковой как экдистероидсодержащего растения в сравнении с действием экдистерона.
Материалы и методы исследования
Сбор растений ушанки мелкоцветковой (Otites parviflorus Grossh.) семейства гвоздичных (Caryophyllaceae Juss.) в фазе цветения производили в Рязанской области (окрестности с. Заборье, на песках, Рязанский район), сушку сырья осуществляли воздушно-теневым способом.
Изучение качественного состава полифенольных и стероидных соединений проводили на высокоэффективном жидкостном хроматографе фирмы «GILSTON», модель 305, ФРАНЦИЯ; инжектор ручной, модель RHEODYNE 7125 USA, с последующей компьютерной обработкой результатов исследования с помощью программы Мультихром для «Windows».
В качестве неподвижной фазы была использована металлическая колонка размером 4,6х250 мм KROMASIL C18, размер частиц 5 микрон.
В качестве подвижной фазы – метанол: вода: фосфорная кислота (400:600:5). Анализ проводили при комнатной температуре. Скорость подачи элюента 0,8 мл/мин. Продолжительность анализа 60 мин. Детектирование проводилось с помощью УФ-детектора «GILSTON» UV/VIS модель 151, при длине волны 254 нм.
Для исследования сырьё измельчали до размера частиц, проходящих сквозь сито с диаметром отверстий 2 мм по (ГОСТ 214-83). Около 3,0 г лекарственного сырья помещали в колбу вместимостью 150 мл, прибавляли по 20 мл спирта этилового 70 %, присоединяли к обратному холодильнику и нагревали на кипящей водяной бане в течение 1 часа с момента закипания спиртоводной смеси в колбе. После охлаждения смесь фильтровали через бумажный фильтр в мерную колбу объёмом 25 мл и доводили спиртом этиловым 70 % до метки (исследуемый раствор).
Параллельно готовили серию 0,05 % растворов сравнения в 70 % спирте этиловом: рутина, кверцетина, лютеолина, лютеолин-7-гликозида, галловой кислоты, кофейной кислоты, хлорогеновой кислоты, гиперозида, геспередина, апигенина, кемпферола, феруловой кислоты, цикориевой кислоты, умбеллиферона, дигидрокумарина, скополетина, эскулетин, кумарина, дикумарин, дигидрокверцитина, катехина, эпикатехина, эпигаллокатехингаллата (ЭПГКГ), экдистерона, виценина, полиподина В. По 20 мкл исследуемых растворов и растворов сравнения вводили в хроматограф и хроматографировали в вышеприведенных условиях.
Для количественного определения виценина, полиподина В, экдистерона в траве ушанки мелко- цветковой методом ВЭЖХ сырьё измельчали до размера частиц, проходящих сквозь сито с диаметром отверстий 2 мм по ГОСТ 214-83. Около 3,0 г лекарственного сырья помещали в колбу вместимостью 150 мл, прибавляли по 20 мл спирта этилового 70 %, присоединяли к обратному холодильнику и нагревали на кипящей водяной бане в течение 1 часа с момента закипания спиртоводной смеси в колбе. После охлаждения смесь фильтровали через бумажный фильтр в мерную колбу объёмом 25 мл и доводили спиртом этиловым 70 % до метки (исследуемый раствор). Параллельно готовили растворы РСО виценина, полиподина в 70 % спирте этиловом. Для этого около 0,020 г (точная навеска) виценина, полиподина помещали в мерную колбу вместимостью 25 мл, прибавляли 20 мл спирта этилового 70 %, перемешивали до растворения и доводили объём до метки тем же растворителем. (РСО). По 20 мкл исследуемого раствора и растворов РСО вводили в хроматограф и хроматографировали по вышеприведенной методике.
Расчёт количественного содержания виценина, полиподина В, экдистерона производили методом абсолютной калибровки с помощью компьютерной программы «Мультихром» для «Windows» и с помощью формулы
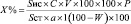 ,
,
где Sис –площадь пика виценина, полиподина В или экдистерона в исследуемом растворе; Sст – площадь пика стандартного раствора (РСО) виценина или полиподина В; X % – концентрация виценина или полиподина В в %; C – концентрация РСО виценина или полиподина В в г/мл; a – навеска исследуемого образца; W – потери в массе при высушивании в %; P – чистота стандартов виценина, полиподина В или экдистерона.
Актопротекторное действие изучалось на 24 беспородных белых крысах самцах средней массой 230 ± 20 г. Все животные были разделены на 4 серии. 1 серия – контроль – животные (n = 8), которым вводили воду очищенную, 2 серия – контроль препарата – животные (n = 8), которым вводили экдистерон (0,1 % раствор экдистерона, выделенный из смолёвки поникшей (Silene nutans L.) и смолёвки татарской (Silene tatarica (L.) Pers.), 3 серия – введение животным (n = 8) экстракта из – ушанки мелкоцветковой (Otites parviflorus Grossh.) семейства гвоздичные (Caryophyllaceae Juss.). Изучаемые вещества вводили per os 1 раз в день из расчета 5 мл/кг массы в течение 15 дней.
Перед началом эксперимента, на 5, 10 и 15 день исследования у крыс определяли физическую работоспособность. Её оценивали по времени плавания в ёмкости с водой при t 21 °С с грузом весом 15 % от массы тела у корня хвоста, до полного утопления, критерием которого служило 10-секундное погружение животного под воду (2,4). Фиксировали время первого плавания и время второго плавания (после 60-минутного отдыха), а затем также рассчитывали и общее время плавания.
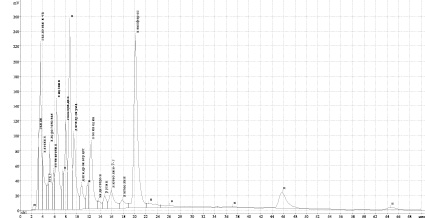
Рис. 1. Хроматограмма ВЭЖХ водно-спиртового извлечения (детектирование при длине волны 254 нм)
Таблица 1
Результаты идентификации некоторых полифенольных и стероидных соединений ушанки мелкоцветковой (водно-спиртовое извлечение, детектирование 254 нм)
|
№ п/п |
Время, мин |
Высота, mV |
Площадь, mV*сек |
ФО |
Конц. % |
Название соединения |
|
1 |
2,199 |
1,61 |
27,16 |
1,000 |
0,05 |
н |
|
2 |
3,13 |
104,29 |
1548,77 |
1,000 |
2,72 |
танин |
|
3 |
3,49 |
223,44 |
4378,49 |
1,000 |
7,69 |
галловая кислота |
|
4 |
3,93 |
72,98 |
2107,85 |
1,000 |
3,70 |
катехин |
|
5 |
4,755 |
33,73 |
412,56 |
1,000 |
0,72 |
эпгкг |
|
6 |
5,16 |
87,59 |
2221,23 |
1,000 |
93,90 |
хлорогеновая кислота |
|
7 |
5,866 |
53,20 |
1123,67 |
1,000 |
1,97 |
эпикатехин |
|
8 |
6,42 |
147,30 |
4771,34 |
1,000 |
8,37 |
виценин |
|
9 |
7,473 |
51,18 |
1057,37 |
1,000 |
1,86 |
н |
|
10 |
7,926 |
117,03 |
2964,13 |
1,000 |
5,20 |
гесперидин |
|
11 |
8,587 |
253,93 |
7017,13 |
1,000 |
12,32 |
н |
|
12 |
9,4 |
102,05 |
3575,02 |
1,000 |
6,28 |
дигидрокумарин |
|
13 |
10,66 |
34,01 |
1328,23 |
1,000 |
2,33 |
дигидрокверцетин |
|
14 |
11,71 |
33,00 |
844,17 |
1,000 |
1,48 |
н |
|
15 |
12,32 |
90,44 |
3850,82 |
1,000 |
6,76 |
полиподин В |
|
16 |
13,66 |
11,08 |
469,62 |
1,000 |
0,82 |
экдистерон |
|
17 |
14,7 |
17,24 |
755,47 |
1,000 |
1,33 |
рутин |
|
18 |
18,88 |
24,90 |
1630,67 |
1,000 |
2,86 |
лютеолин-7-гликозид |
|
19 |
17,79 |
11,73 |
890,85 |
1,000 |
1,56 |
лютеолин |
|
20 |
20,05 |
231,56 |
10936,14 |
1,000 |
19,20 |
кемпферол |
|
21 |
22,32 |
6,76 |
806,67 |
1,000 |
1,42 |
н |
|
22 |
26,17 |
4,01 |
1072,25 |
1,000 |
1,88 |
н |
|
23 |
37,01 |
1,12 |
201,64 |
1,000 |
0,35 |
н |
|
24 |
45,63 |
21,84 |
2431,06 |
1,000 |
4,27 |
н |
|
25 |
64,6 |
3,60 |
549,67 |
1,000 |
0,96 |
н |
|
25 |
70,51 |
1739,63 |
5671,98 |
0,050 |
100,00 |
Полученные результаты обрабатывали статистически с использованием программы «Statistica 7.0», при этом рассчитывали медиану и верхний и нижний квартили. Различия между сериями оценивали с помощью критерия Манна-Уитни, а различия внутри серий – с помощью критерия Вилкоксона. За уровень достоверности принята достоверность различий 95,0 % (р < 0,05).
Результаты исследования и их обсуждение
Приводим результаты ВЭЖХ-исследований некоторых полифенольных и стероидных соединений ушанки мелко-цветковой.
Ряд пиков остался неидентифицированым, что даёт повод продолжить изучение качественного состава травы ушанки мелкоцветковой.
Идентифицировано 14 полифенольных (танин, галловая кислота, катехин, эпигаллокатехингаллат, хлорогеновая кислота, эпикатехин, виценин, гесперидин, дигидрокумарин, дигидрокверцетин, рутин, лютеолин-7-гликозид, лютеолин, кемпферол) и 2 стероидных (экдистерон, полиподин В) соединений.
Таблица 2
Результаты количественного определения виценина, полиподина В и экдистерона в траве ушанки мелкоцветковой
|
виценин, % |
полиподин В, % |
экдистерон, % |
|
0,72 |
0,15 |
0,02 |
При анализе актопротекторного действия выяснено, что введение экспериментальным животным воды очищенной в течение 15 дней достоверно не влияло на время 1 плавания. Введение экдистерона (препарата сравнения) увеличивало время плавания животных с грузом через 10 дней введения на 6,8 % (р < 0,05), а через 15 дней – 19,2 % (р < 0,05). Применение водной вытяжки из ушанки приводило к повышению времени первого плавания на 10-й день исследования на 18,1 % (р = 0,05), а, на 15-й день опыта – на 45,1 (р < 0,05). На 15-й день эксперимента время плавания животных, получавших ушанку, превышало показатели контроля на 49,3 (p < 0,05).
У контрольных животных на 10-й день эксперимента происходило повышение времени второго плавания на 10,6 % (р < 0,05), на 15-й день – на 29,1 % (р < 0,05). Введение экдистерона (препарата сравнения) увеличивало время плавания животных с грузом через 5 дней на 16,4 % (р < 0,05), через 10 дней – на 23,9 % (р < 0,05). Однако время плавания животных, получавших экдистерон, было меньше показателей контроля на 15,9 % (р < 0,05). Применение водной вытяжки из ушанки приводило к повышению времени второго плавания на 15-й день исследования на 20,0 % (р < 0,05).
Влияние изучаемых веществ на суммарное время плавания представлено в табл. 3. У контрольных животных происходило повышение общего времени плавания – на 10,4 % (р < 0,05) только на 15-й день эксперимента. Введение экдистерона (препарата сравнения) увеличивало время плавания животных с грузом через 10 дней на 16,3 % (р < 0,05), а через 15 дней – на 21,3 % (р < 0,05). Применение водной вытяжки из ушанки приводило к повышению времени второго плавания на 5-й день эксперимента на 9,9 % (р < 0,05), на 10-й день – 16,2 % (р = 0,05), на 15-й день – на 31,0 % (p < 0,05).
Таблица 3
Показатели общей физической работоспособности крыс при введении экдистерона и экстракта из ушанки мелкоцветковой (суммарный показатель двойного плавания)
|
Сроки определения, продолжительность плавания, с Серии эксперимента |
Исходные данные, 1 день |
5 дней |
10 дней |
15 дней |
|
Вода очищенная |
139,0 (128,0; 147,0) |
145,5 (129,0; 162,5) |
142,0 (128,0; 187,0) |
153,5 (142,0; 178,0)* |
|
Экдистерон |
141,0 (138,0; 148,0) |
145,0 (139,0; 168,0) |
164,0 (158,0; 175,0)* |
171,0 (159,0; 172,0)* |
|
Ушанка |
142,0 (136,0; 149,0) |
156,0 (150,0; 194,0)* |
165,0 (154,0; 195,0)* |
186,0 (171,0; 199,0)* |
Примечание. * – р < 0,05 – достоверные различия с исходными данными.
Выводы
1. В траве ушанки мелкоцветковой (Otites parviflorus Grossh.) семейства гвоздичные (Caryophyllaceae Juss.) нами идентифицировано 14 полифенольных соединений, 2 экдистероида (экдистерон и полиподин В).
2. Определено количественное содержание экдистерона, полиподина В и виценина в траве ушанки мелкоцветковой, оно соответственно равно 0,02 %, 0,15 %, 0,72 %.
3. Экстракт из ушанки мелкоцветковой при введении per os в количестве 5 мл/кг массы обладает выраженным актопротекторным действием, превосходящим эффект экдистерона.
Библиографическая ссылка
Дармограй В.Н., Ерофеева Н.С., Дармограй С.В., Филиппова А.С., Морозова В.А., Дубоделова Г.В. КАЧЕСТВЕННОЕ И КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ЭКДИСТЕРОИДОВ И ПОЛИФЕНОЛЬНЫХ СОЕДИНЕНИЙ ТРАВЫ УШАНКИ МЕЛКОЦВЕТКОВОЙ (OTITES PARVIFLORUS GROSSH.) // Успехи современного естествознания. 2015. № 12. С. 21-25;URL: https://natural-sciences.ru/ru/article/view?id=35714 (дата обращения: 15.05.2026).



