Урал является крупнейшей колчеданной провинцией мира. Здесь более сотни месторождений и рудопроявлений, насчитывающих более 1,8 млрд тонн медных и медно-цинковых руд.
Южный Урал, являясь важнейшей составляющей Уральского промышленного региона, имеет наиболее явно выраженную техногеосферу, так как характеризуется чрезвычайно высокой концентрацией промышленного производства.
Медно-цинковый комплекс Южного Урала, представленный такими предприятиями, как ОАО «Гайский ГОК», ОАО «Учалинский ГОК», ОАО «Бурибаевский ГОК», ОАО «Башкирский медно-серный комбинат», ОАО «Александринская горнорудная компания» и др., занимается разработкой и переработкой медноколчеданных месторождений [10–12].
Горнодобывающая промышленность является источником образования большого количества отходов, не только твердых, но и жидких природно-техногенных. В результате деятельности ГОКов, помимо добычи и обогащения полезных ископаемых, происходит образование специфического сернокислого техногенного ландшафта, который приводит к загрязнению атмосферы, почвы, поверхностных и подземных вод, накапливанию твердых и жидких отходов [5]. Жидкие отходы характерно образуются из отработанных хвостов, карьеров, рудных отвалов [11, 12].
Сброс неочищенных техногенных стоков на земную поверхность приводит к накоплению в окружающих водных объектах тяжелых металлов, таких как медь, цинк, железо, марганец, кадмий, никель и др., многие из которых обладают кумулятивным действием, а также общетоксичными, эмбриотропными и мутагенными свойствами [10]. Значительное количество техногенных вод имеют высокую техногенную нагрузку.
Современная экологическая политика государства выводит на ведущие позиции решение вопросов переработки техногенных образований с целью снижения концентраций канцерогенных веществ в окружающей среде до норм ПДК. Значительные объемы вод и высокие концентрации в них металлов позволяют рассматривать этот вид отходов в качестве сырья для получения различных видов металлсодержащей продукции [2, 3, 5].
Переработка металлсодержащих природно-техногенных вод позволит более полно использовать природные ресурсы. В микрокомпонентном катионном составе подотвальных и рудничных вод горных предприятий Южного Урала преобладают железо, медь и цинк. В макрокомпонентном анионном составе преобладает сульфат-ион. Концентрация ионов железа достигает 2100 мг/дм3.
Анализ техногенных водных объектов, формирующихся на территории ГОКов Южного Урала, показал, что концентрация основных металлов в рудничных кислых водах составила (в среднем): по Cu 541,5 мг/дм3, по Fe 880,4 мг/дм3, по Zn 687,5 мг/дм3 и по Мn 187,9 мг/дм3, что естественным образом негативно сказалось на качестве воды прилегающих поверхностных водоемов [5–7].
Таким образом, очевиден вывод о необходимости вовлечения кислых рудничных вод в переработку и разработки новых инновационных технологий извлечения катионных форм металлов из техногенного гидроминерального сырья, обеспечивающих предотвращение сброса токсичных гидроминеральных стоков в природные водоемы.
В работе представлены результаты исследований процесса извлечения ионов железа (II, III) из кислых рудничных вод ЗАО «Бурибаевский ГОК» методом кислотноосновного осаждения.
На начальном этапе исследования процесса кислотно-основного осаждения железа проводились на модельных растворах с исходной концентрацией ионов Fe3+: 300, 500, 750 мг/дм3 и ионов Fe2+: 300, 400, 650 мг/дм3 (исходные концентрации железа были смоделированы на растворах кислых подотвальных вод Бурибаевского ГОКа). В качестве реагента-осадителя использовали раствор известкового молока. Процесс осаждения железа проводили в изотермических условиях при перемешивании в течение 20 минут. Известковое молоко вводили дозировано в виде 1 % водной суспензии, контролируя значения рН обрабатываемого раствора до и после введения. По истечении 20 минут определяли остаточное содержание ионов Fe2+ и Fe3+ фотометрическим методом с использованием сульфосалициловой кислоты. Полученные результаты эксперимента представлены на рис. 1.
Согласно полученным зависимостям (рис. 1) осаждение ионов Fe3+ наблюдается после рН от 2,5 до 4,1. Показатели извлечения железа в виде гидроксида Fe (ОН)3 в зависимости от исходной концентрации ионов железа изменяются в диапазоне 94,9–96,4 %. При этом уменьшение исходной концентрации ионов Fe3+ в растворах приводит к увеличению рН начала осаждения его в виде Fe(ОН)3. Изменение интервала осаждения ионов Fe3+ при разных исходных концентрациях может объясняться явлением соосаждения, а именно: поверхности образующегося гидроксида железа (III) обладают хорошими сорбционными свойствами, вследствие чего хлопья Fe(ОН)3 улавливают более мелкие коллоидные частицы, агрегируют их на своей поверхности, усиливая тем самым процесс осаждения образующихся коллоидных взвесей [1, 3, 4, 9].
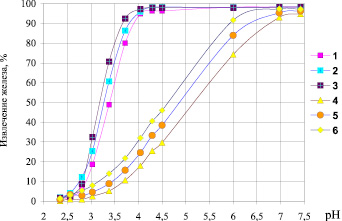
Рис. 1. Влияние рН раствора на извлечение ионов Fe2+ и Fe3+ из кислых вод методом кислотно-основного осаждения: 1 – исходная концентрация Fe3+ = 300 мг/дм3; 2 – исходная концентрация Fe3+ = 500 мг/дм3; 3 – исходная концентрация Fe3+ = 750 мг/дм3; 4 – исходная концентрация Fe2+ = 300 мг/дм3; 5 – исходная концентрация Fe2+ = 500 мг/дм3; 6 – исходная концентрация Fe2+ = 650 мг/дм3
Максимальные показатели извлечения Fe2+ в виде гидроксида Fe (ОН)2 (91,5–96,9 %) в зависимости от Сисх. Fe2+ в воде, наблюдаются в диапазоне рН 7,1–7,5. Увеличение исходной концентрации ионов Fe2+ в обрабатываемых растворах приводит к уменьшению рН начала осаждения Fe (II).
Из вышеизложенного следует, что селективное извлечение таких металлов, как медь, марганец и цинк (методом кислотно-основного осаждения), в присутствии ионов Fe2+ невозможно ввиду того, что осаждение Fe(II) в виде осадка Fe(ОН)2 наблюдается в интервале рН 3,4 – 7,5, что совпадает с оптимальным диапазоном рН осаждения ионов меди, цинка и марганца [2, 4, 8, 9]. При этом существует возможность селективного разделения ионов Mn2+, Zn2+ и Fe3+, т.к. в интервале рН от 2,5 до 4,1 трехвалентное железо осаждается практически полностью в виде осадка Fe (ОН)3.
Следовательно, для селективного извлечения меди, цинка и марганца из кислых рудничных вод необходимо предварительно проводить процесс окисления ионов Fe2+ до Fe3+ с последующим осаждением его в виде нерастворимого гидроксида Fe(ОН)3. В качестве окислителя возможно использование: молекулярного кислорода (в случае предварительной аэрации растворов), озона, хлорсодержащих окислителей и др [3, 4, 8].
Основные процессы, протекающие в растворах, содержащих ионы Fe2+ и Fe3+ при проведении процесса окислительного осаждения, отображены в реакциях ниже [5, 7, 10]:
Fe2+ + О2 + H2SO4 > Fe 2 (SO4)3 + 2Н2О,
Fe3+ + H2SO4 > Fe 2 (SO4)3 + 2Н2О,
Fe 2 (SO4)3 + 2Н2О > Fe (ОН)3 + H2SO4.
Полученные кинетические зависимости процесса окислительного осаждения ионов железа в виде осадка из технических растворов показали, что максимальное извлечение железа (в виде гидроксида железа (III)) возможно после 10–15 минут протекания процесса, в зависимости от Сисх Fe3+ (рис. 2). В качестве окислителя использовали раствор хлорной извести (рН = 9,4).
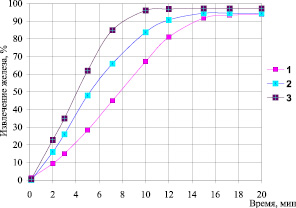
Рис. 2. Кинетика процесса окислительного осаждения Fe (II,III) из технических растворов, при введении раствора хлорной извести (рНисх. 3,1), (рНкон. 6,7): 1 – исходная концентрация Feобщ. 300 мг/дм3; 2 – исходная концентрация Feобщ. 500 мг/дм3; 3 – исходная концентрация Feобщ. 750 мг/дм3
Отмечено, что с увеличением концентрации железа в системе значительно сокращается время протекания процесса осаждения. Данный факт можно объяснить тем, что образующиеся хлопья гидроксида железа характеризуются большой гидравлической крупностью, поэтому быстро оседают под действием силы тяжести, что способствует интенсификации процесса коагуляции.
Следовательно, максимальные показатели извлечения железа (II и III) из кислых растворов в виде дисперсной фазы Fe(OH)3 достигаются при проведении процесса окислительного осаждения в диапазоне рН от 3,7 до 4,1, продолжительность обработки растворов 10–15 минут (Сисх Feобщ. 300–750 мг/дм3) с использованием в качестве реагента-осадителя водных растворов хлорной извести.
В работе были проведены исследования химического состава железосодержащих осадков, образующихся при переработке кислых подотвальных вод ЗАО «Бурибаевский ГОК» методом окислительного осаждения (при предварительном извлечении ионов меди, цинка и марганца). Полученные результаты анализа представлены в таблице.
Химический состав железосодержащих осадков, получаемых из кислых подотвальных вод Бурибаевского ГОКа
|
Символ химического элемента |
Fe |
С |
Al2O3 |
SiO2 |
Р |
CaO |
MgO |
|
Содержание, % |
52,1 |
0, 91 |
0,03 |
– |
– |
0,21 |
0,16 |
Анализ полученных результатов (таблица) показал, что образующиеся железо-содержащие осадки, согласно ТУ 13.1-32279599-001, являются кондиционным сырьем (βFe > 50 %) и могут быть использованы при изготовлении агломерационных и брикетированных форм сырья, идущего на переплавку в доменных и индукционных печах при получении литейного чугуна, а также в качестве железосодержащей добавки при производстве жидкого цемента.
Выводы
– разработанные технологические рекомендации позволяют эффективно извлекать железо из кислых рудничных вод методом кислотно-основного осаждения;
– железосодержащие осадки (βFe = 52 %), которые, согласно ТУ 13.1-32279599-001:2007, являются кондиционным сырьем и могут быть использованы при изготовлении агломерационных и брикетированных форм сырья, идущего на переплавку в доменных печах, для переплавки в индукционных печах при получении литейного чугуна, в качестве железосодержащей добавки при производстве жидкого цемента;
– внедрение усовершенствованных технологий очистки кислых рудничных вод горных предприятий позволит дополнительно извлекать тяжелые и цветные металлы в виде товарного продукта;
– осадки нейтрализации, обладающие определенными технологическими свойствами, возможно использовать как сырье в металлургической отрасли, а также для производства строительных материалов;
– вовлечение в переработку кислых рудничных вод медноколчеданных месторождений позволит повысить рентабельность горных предприятий, улучшить состояние водных ресурсов, сократить накопление отходов и отчуждение земель под их хранение.
Библиографическая ссылка
Мишурина О.А., Муллина Э.Р. ХИМИЧЕСКИЕ АСПЕКТЫ ПРОЦЕССА ДЕФЕРРИТИЗАЦИИ КИСЛЫХ РУДНИЧНЫХ ВОД // Успехи современного естествознания. 2016. № 12-1. С. 194-198;URL: https://natural-sciences.ru/ru/article/view?id=36286 (дата обращения: 17.12.2025).



