В настоящее время химия координационных соединений представляет собой наиболее перспективную область науки [1]. Согласно проведённым ранее исследованиям [2] многие антибиотики в молекулярной или ионной форме способны образовывать устойчивые комплексы с катионами различных металлов. Металлокомплексы оказывают влияние на антимикробную активность, химические свойства и на устойчивость к гидролизу [3–5].
Кристаллическая структура синтезированных антибактериальных соединений весьма ограничена. Опубликованы исследования [6–8] отражающие современное состояние кристаллохимии, ряда нитрофуранов и их комплексов с металлами, а именно с Mg (II), Ca (II), Cu (II), Cd (III), Ni (II) Zn (II), Co (III). Протолитическое равновесие нитрофуранов в растворителях обуславливает их разнообразие и способность координировать с металлами. Изучение способности к комплексообразованию нитрофуранов помогает лучше понять физико-химические свойства для практического использования этого класса антибиотиков. Их реакция в водных и водноорганических растворителях весьма многообразна, данные исследований позволят оценить координационные возможности и состав соединений в жидких средах, включая физиологические жидкости живых организмов.
Целью исследования является изучение процесса комплексообразования антибиотиков группы нитрофураны, а именно фуразолидона с ионами d-металлов (Zn (II), Mn (II), Cu (II)), определение термодинамических характеристик и построение ИК-спектров.
Материалы и методы исследования
Оптимизация геометрических параметров комплексов фуразолидона с металлами произведена в приближении HF/6-31 + G*, на функциях ограниченного метода Хартр – Фока с открытой оболочкой. Учет растворителя производили с помощью PCM-C [10]. При расчете колебательных спектров масштабирующий коэффициент не применялся. Все расчеты выполнены в программном пакете FifeFly 8.1 [9, 11].
Результаты исследования и их обсуждение
На первом этапе исследования произведена оптимизация геометрических параметров, для нахождения равновесных состояний молекулы фуразолидона. Схематическое строение молекулы антибиотика приведено на рис. 1, а.
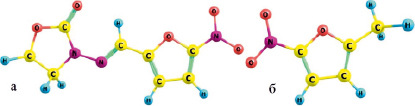
Рис. 1. Геометрическое строение оптимизированной молекулы фуразолидона: а – полная, б – упрощенная
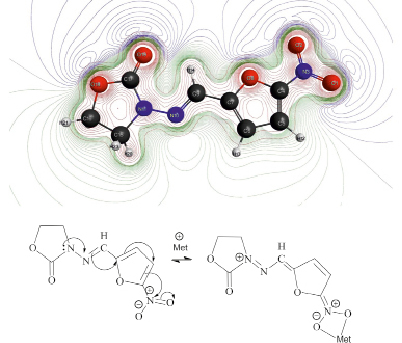
Рис. 2. Распределение электронной плотности в молекуле фуразолидона (зеленым показан отрицательный электростатический потенциал, синим – положительный; красными линиями показано распределение электронной плотности)
Предварительный анализ электронной плотности (рис. 2) в молекуле фуразолидона показал, что отрицательный электростатический потенциал расположен вдоль атомов кислорода и делит молекулу пополам. Основная часть электронной плотности сосредоточена у молекул кислорода и в равной степени распределяется между ними. Небольшая часть электронной плотности распределена между двумя атомами азота (N11, N12) с преобладанием положительного электростатического потенциала. Однако доступ к атомам азота N11, N12 пространственно затруднен. Следовательно, можно предположить, что с большой вероятностью именно атомы кислорода и будут участвовать в химической реакции по схеме, указанной на рис. 2.
Доказательством верности расчета может служить совпадение теоретического ИК-спектра молекулы фуразолидона с экспериментальным ИК-спектром. На рис. 3 показано хорошее соответствие расчетного ИК-спектра молекулы фуразолидона с экспериментальными данными. Небольшое различие 100–150 см-1 может быть связано с использованием континуальной модели PCM-C, в которой в качестве растворителя были выбраны молекулы воды, в то время как экспериментальный ИК-спектр молекулы фуразолидона был получен в твердой фазе. Также следует учесть, что масштабирующий коэффициент к теоретическим ИК-спектрам не применялся. На правильность результатов расчета указывает и совпадение, по абсолютному значению, расчетных интегральных интенсивностей с экспериментальными коэффициентами экстинкции (табл. 1). Частоты наиболее интенсивных мод колебаний комплексов фуразолидона по результатам HF/6-31+G* + PCM-C расчетов приведены в табл. 2.
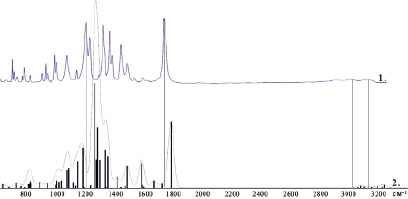
Рис. 3. Инфракрасные спектры фуразолидона (1 – эксперимент [12], 2 – расчет), расчет в приближении HF/6-31+G* + PCM-C
Таблица 1
Характеристические полосы поглощения фуразолидона (см-1). Сравнение экспериментального ИК-спектра с теоретически полученным в приближении HF/6-31+G*
|
Эксперимент |
Расчет |
Эксперимент |
Расчет |
|
750 (ср) |
621 (сл) |
1390 (с) |
1314 (с) |
|
1030 (ср) |
822 (сл) |
1475 (с) |
1410 (ср) |
|
1094 (ср) |
1112 (сл) |
1500 (ср) |
1553 (сл) |
|
1178 (сл) |
1158 (с) |
1620 (сл) |
1758 (сл) |
|
1250 (с) |
1181 (ср) |
1750 (с) |
1890 (ср) |
|
1380 (с) |
1211 (ср) |
3022 (сл) |
3320 (сл) |
Примечание. с. – сильное колебание, сл. – слабое колебание, ср. – среднее колебание. В соответствии с усредненными значениями расчетных интегральных интенсивностей ИК-полос, а также усредненными коэффициентами экстинкции.
Таблица 2
Частоты (см-1) наиболее интенсивных мод колебаний комплексов фуразолидона по результатам HF/6-31+G* + PCM-C расчетов
|
Отнесение |
Частота |
|
νas(С-O-C) |
1181 |
|
νas(С-N) |
1314 |
|
ν(NO2) |
1410 |
|
δ (С-Н) |
1553 |
|
ν(С=О) |
1890 |
|
νs(С-H) |
3320 |
Примечание. ν– валентные колебания: s – симметричное, as – антисимметричное; деформационные колебания.
Следующим этапом было решено рассмотреть возможность комплексообразования фуразолидона с катионами переходных металлов. В качестве примера выбраны три катиона металла: цинка, меди и марганца. Конформационный анализ, а именно присоединение металла к различным атомам кислорода, не проводился. Следует иметь в виду, что задачей данной работы являлось лишь наглядное отображение возможности комплексообразования молекулы фуразолидона. Катион металла располагали между атомами кислорода О2 и О1 нитрогруппы молекулы фуразолидона (рис. 2). Так как для исследуемых металлов возможно различное координационное число, то выбрана следующая модельная стратегия. Рассчитаны комплексы двузарядных катионов металла с разным количеством лигандов фуразолидона 1:1; 1:2; 1:3; 1:4. Ввиду большого количества оптимизируемых атомов в исследуемых комплексах фуразолидона с металлами было решено упростить модель оптимизации, включив в расчет только пентильное 2-нитрофуранильное кольцо с присоединенным к нему атомом азота и двумя атомами кислорода (рис. 1, б).
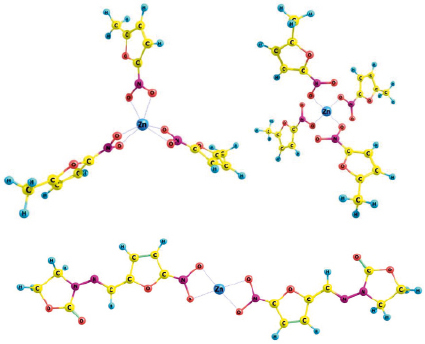
Рис. 4. Структура оптимизированных комплексов фуразолидона с двумя, тремя и четырьмя катионами металла, на примере цинка
На основе энергий образования комплексов (DE °), указанных в табл. 3, можно сделать вывод, что присоединение новой молекулы фуразолидона к образующемуся комплексу увеличивает его устойчивость. Однако при этом увеличение координационного числа катиона металла, за исключением комплексов с тремя молекулами фуразолидона, не происходит (рис. 4). Данный факт показывает, что наиболее устойчивый комплекс образуется при присоединении катиона металла к одному атому кислорода группы NO2, то есть координационное число для всех металлов в комплексе с фуразолидоном равно 4. Наиболее устойчивые соединения образуются с Cu и Zn. Отличие в энергиях образования комплексов с медью и цинком не превышает 20 ± 5 кДж/моль.
Вычисление изменения энергии Гиббса проводили для комплексов двух молекул фуразолидона с катионами металлов. Расчет энергии DG выполняли для нормальной (полной) молекулы фуразолидона. Учет растворителя производили с помощью поправки PCM-C. В качестве модельного растворителя выбрана вода. Вычисленные изменения свободной энергии Гиббса DG ° при образовании комплекса катионов металлов с фуразолидоном для всех структур приведены в табл. 3.
Таблица 3
Абсолютные (E °) и относительные (DE °) энергии образования комплекса, рассчитанные для описания комплексообразования Me (II) с фуразолидоном
|
Cu |
Zn |
Mn |
|
|
ΔE °, Энергия образования комплекса, кДж/моль |
|||
|
ΔE °1 |
– 882,5 |
– 880,1 |
– 701,2 |
|
ΔE °2 |
– 1420,6 |
– 1397,7 |
– 798,6 |
|
ΔE °3 |
– 1678,6 |
– 1691,0 |
– 756,2 |
|
ΔE °4 |
– 1858,1 |
– 1877,6 |
– 1212,4 |
|
E °, Хартри |
|||
|
Me 2+ |
– 1630,111886 |
– 1768,275039 |
– 1143,571479 |
|
MeFur 2+ |
– 2098,910864 |
– 2237,073063 |
– 1612,301385 |
|
MeFur2 2+ |
– 2567,578594 |
– 2705,733039 |
– 2080,801290 |
|
MeFur3 2+ |
– 3036,139670 |
– 3174,307565 |
– 2549,247934 |
|
MeFur2 2+ |
– 3504,670854 |
– 3642,841438 |
– 3017,884526 |
|
ΔG °, Энергия образования комплекса, кДж/моль (PCM-C) |
|||
|
Me2+ + 2Fur |
121,3 |
128,3 |
96,3 |
|
Me2+ + 2Fur + 2H2O |
281,6 |
304,6 |
218,7 |
Примечание. Fur – Фуразолидон (Furazolidone): 3-[[(5-Нитро-2-фуранил)метилен]амино]-2-оксазолидинон (C8H7N3O5). Величина энергии Гиббса для молекулы фурацилина G °, Хартри = – 468,4628157. Расчет в приближении HF/6-31+G*.
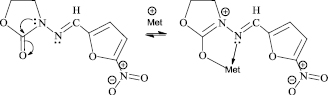
Рис. 5. Схема распределения электронной плотности в молекуле фуразолидона
Установлено, что для всех металлов характерно плоскоквадратное окружение катиона атомами кислорода. Вычисленные значения изменения свободной энергии Гиббса (табл. 2) показывают, что наиболее устойчивый комплекс образуется с катионами Zn и Cu, наименьшей устойчивостью обладает комплекс фуразолидона с Mn. Однако все полученные значения имеют положительный знак, следовательно, присоединение катионов металлов в воде невыгодно и при нормальных условиях комплексы фуразолидона с медью, цинком и марганцом по схеме, указанной на рис. 2, образовываться не будут. Данный факт предположительно можно объяснить тем, что фуразолидон плохо растворим в воде, а также возможностью присоединения металлов к молекулам кислорода О18 и О19 по другой схеме (рис. 5). Это подтверждается расчетами катионов металлов с фуразолидоном в присутствии воды. Молекулы воды еще больше увеличивают энергию образования комплексов.
Выводы
На основе расчета энергий образования комплексов фуразолидона с металлами DE °, а также изменении свободной энергии Гиббса DG ° выявлено, что наиболее устойчивые соединения образуются с медью и цинком. Для всех металлов характерно плоскоквадратное окружение катиона атомами кислорода, в случае присоединения с четырьмя и двумя молекулами фуразолидона. Полученные результаты представлены для реакции присоединения катиона металла к нитрогруппе молекулы фуразолидона.
Библиографическая ссылка
Чигринева Н.А., Абрамова В.В., Сагдеев М.А., Строганова Е.А., Ткачева Т.А., Пешков С.А. ИССЛЕДОВАНИЕ УСТОЙЧИВОСТИ ЛЕКАРСТВЕННЫХ СРЕДСТВ ГРУППЫ НИТРОФУРАНЫ С МЕТАЛЛАМИ // Успехи современного естествознания. 2017. № 7. С. 18-23;URL: https://natural-sciences.ru/ru/article/view?id=36471 (дата обращения: 14.05.2026).



