Зерновые культуры, в число которых входят пшеница, ячмень, кукуруза, рис, по продуктивным и кормовым качествам относятся к наиболее ценным сельскохозяйственным культурам и являются основным продуктом питания во многих регионах мира. Возрастающие потребности в зерне можно удовлетворить за счет повышения урожайности, интенсивности земледелия и внедрения новых технологий. Применение в селекционных программах современных биотехнологических подходов, основанных на использовании молекулярных маркеров, может способствовать решению этих проблем.
В настоящее время увеличивается число различных типов молекулярных маркеров вместе с достижениями современных технологий и знаниями об отдельных генах и геномах растений в целом [1–3]. Однонуклеотидный полиморфизм (ОНП), замена одного нуклеотида в любой части генома в результате естественной мутации, является одним из самых мощных инструментов в молекулярной биологии [4–6]. ОНП как точечные мутации могут быть эволюционно нейтральными и избегать влияния естественного отбора, если они происходят в некодирующих областях или не влияют на аминокислотную последовательность кодируемых полипептидов. Впоследствии ОНП стали широко распространяться в геномах всех живых организмов [7]. Для идентификации ОНП применяют различные типы молекулярных маркеров, каждый из которых имеет сопутствующие преимущества и недостатки. Одним из наиболее эффективных и быстрых способов использования маркеров ОНП является технология KASP (Competitive Allele Specific PCR) [8]. KASP – конкурентная аллель-специфичная ПЦР по конечной точке с флуоресцентной детекцией, в которой полиморфизм выявляют с помощью ОНП-маркеров за счет однонуклеотидных замещений, вставок и делеций. Этот универсальный метод диагностики характеризуется высокой точностью и производительностью и является удобным инструментом для маркер-опосредованной селекции (Marker-Assisted Selection, MAS). С использованием KASP-маркеров был картирован целый ряд генов и локусов количественных признаков (QTL). В анализе KASP используется новая гомогенная флуоресцентная система генотипирования, которая, по сравнению с мультиплексными методами (например, чиповая технология), очень быстрая и позволяет получать точные результаты (99,8 %) в течение нескольких часов. Таким образом, KASP-маркеры представляют собой эффективный инструмент как в молекулярно-генетических исследованиях, так и в селекции растений. Высокопроизводительная SNP маркерная технология очень эффективна для мягкой пшеницы (Triticum aestivum L.). Среди злаков геном пшеницы оценивается как один из наименее полиморфных. С помощью этих маркеров можно точно и быстро анализировать сотни образцов одновременно по маркерам ОНП.
Основная цель исследования направлена на скрининг 11 различных локусов, связанных с продуктивностью, показателями качества и устойчивостью к болезням коллекций мягкой пшеницы из Национального генетического банка Института генетических ресурсов Национальной академии Наук азербайджана, с использованием технологии KASP.
Материалы и методы исследования
В качестве исследовательского материала были использованы 166 образцов мягкой пшеницы из коллекции Национального генетического банка Института генетических ресурсов Национальной академии наук Азербайджана. Изученный материал представлен 35 сортами, созданными в разные годы, и образцами, собранными из разных регионов республики, изученными в полевых условиях и отобранными по биоморфологическим признакам в течение трех лет. Выделение геномной ДНК проводили согласно CTAB протоколу. Для генотипирования использованы 11 KAPS-маркеров (RhtB1_cim-KASP; RhtD1-KASP; Ppd-D1-D002-KASP; Glu-D1-DX-KASP; Gpc-B1-DUP-KASP; Lr21-GQ504819-1346-KASP; Lr34JagExon22-KASP; csSr2; Tsn1-KASP; FHB 5A; FHB 3BS/Fhb1), которые разработаны и изготовлены компанией LGC Genomics на основе соответствующего протокола, предоставленного компанией.
Результаты исследования и их обсуждение
Молекулярное тестирование и изучение генетических коллекций позволяет проводить скрининг на наличие новых генов и ценных аллелей, оценивать частоту встречаемости и гетерозиготность аллелей в популяции. В настоящем исследовании был проведен скрининг по таким важным показателям, как продуктивность, устойчивость к биотическому стрессу и качество зерна.
Основным требованием любой селекционной программы является создание сортов с высоким генетическим потенциалом продуктивности. Как известно, одним из важных фенотипических признаков, связанных с продуктивностью, являются высота растения и нечувствительность к фотопериоду. Генетическая природа признака – высота растения у пшеницы достаточно хорошо изучена. Для пшениц давно известно, что снижение высоты растений и формирование низкорослого, утолщенного стебля связано с мутациями в генах Rht (reduced height). Растения пшениц, содержащие в геноме мутированные гены Rht (гены карликовости), обнаруженные в 1935 г., отличались повышенной урожайностью и после «Зеленой революции» широко использовались в селекции пшеницы. Гены карликовости различного происхождения сыграли огромную роль в создании современных интенсивных сортов пшеницы, устойчивых к полеганию с высоким уборочным индексом (HI). На хромосомах идентифицировано и локализовано множество локусов Rht, контролирующих этот признак [9, 10]. Хотя пшеница обладает большим числом генов Rht, только три из них Rht-B1 (Rht1), Rht-D1 (Rht2) и Rht8 широко используются в селекции [11, 12, 13]. Из 166 исследованных образцов 43 являются носителями мутантных аллелей Rht-B1b гена Rht-B1, 5 – аллелей Rht-D1b гена Rht-D1. Кроме того, было установлено, что 6 генотипов являются гетерозиготами по гену Rht-B1, 4 – по Rht-D1. Наряду с разновидностями var. milturum, var. erythrospermum, var. lutescens, var. alborubrum, var. barbarossa, var. albidum, var. hostianum, var. velutinum, var. leucospermum, var. delfi аллель Rht-B1b была также выявлена у сортов Арзу, Карабах, Зардаби, Экинчи 84, Рузи 84, Азамот 95, Гобустан, Егяна и другие. Согласно литературным данным, сорта, несущие аллель Rht-D1b, в основном среднего размера и устойчивы к полеганию, у них высота растения колеблется в пределах от 81 до 100 см. Аллель Rht-D1b была выявлена лишь для сорта Гюнешли, обладающего самым низким показателем по признаку длины роста (81–92 см). Другие сортообразцы мягкой пшеницы характеризовались аллелями высокорослости Rht-B1a и Rht-D1a. Высота сортов Угур, Шеки 1, Азери, Шафаг 2 варьировала в пределах значений от 110 до 117 см. Известно, что в благоприятных условиях мутантные гиббереллин-нечувствительные карликовые аллели Rht-B1b и Rht-D1b способствуют повышению индекса продуктивности и устойчивости к полеганию [14]. Однако присутствие мутантных аллелей в неблагоприятных условиях (таких как засуха) может привести к уменьшению длины колеоптиля, что в свою очередь приводит к слабому росту проростков и потере урожая [15]. Напротив, генотипы, которые не имеют ни одного из упомянутых мутантных аллелей, являются более подходящими для культивирования в богарных условиях, так как не уменьшают длину колеоптиля [16]. Таким образом, генотипы, у которых не обнаружены аллели Rht-B1b и Rht-D1b, можно считать более целесообразными для культивирования в богарных условиях. Согласно некоторым литературным данным, существование одновременно двух мутантных аллелей вызывает резкое снижение продуктивности [17]. В изученной коллекции мягкой пшеницы генотипы с обеими мутантными аллелями не наблюдались.
Современные сорта пшеницы по своей фотопериодической чувствительности (ФПЧ) варьируют от сильночувствительных до абсолютно нечувствительных, способных к колошению даже в условиях короткого 8-часового дня [18]. Как правило, фотопериодическая нечувствительность считается важным свойством современных высокоадаптивных сортов со стабильно высокой продуктивностью. Возможность воздействовать на такой важный фактор, как сроки перехода к колошению в современных условиях изменяющегося климата и нестабильных погодных условий, может дать явное преимущество при селекции новых высокоадаптивных сортов пшеницы. Этим объясняется неизменно высокий интерес к донорам новых аллелей генов Ppd у мягкой пшеницы. Гены Ppd, отвечающие за чувствительность растения к длине дня (фотопериоду), играют важную роль при адаптации сортов пшеницы к разным агроклиматическим условиям. Доминантный аллель Ppd-D1a гена Ppd-D1, локализованный в хромосоме 2DS, отвечает за нечувствительность к фотопериоду и раннее цветение, в то время как другой рецессивный аллель – Ppd-D1b ответственен за фотопериодическую чувствительность (ФПЧ). В наших исследованиях среди изученных разновидностей более половины образцов мягкой пшеницы (53 %) несут нечувствительные к фотопериоду аллели гена Ppd-D1, 41,5 % – чувствительные. У девяти образцов была выявлена гетерозиготность по указанному выше локусу. Из 35 изученных сортов у 24 выявлены нечувствительные к фотопериоду аллели Ppd-D1a, тогда как сорта Йерли, Бол бугда, Перзиван1, Перзиван 2 и др. являлись носителями рецессивного аллеля Ppd-D1b гена Ppd-D1. Полученные результаты не согласуются с опубликованными ранее данными. Так, Guedira и другие в 2010 г. в своих исследованиях среди 174 изученной линии пшеницы выявили аллель Ppd-D1a только у 32 % генотипов [19]. Плейотропный эффект аллелей нечувствительности к фотопериоду и карликовости оказывает положительное влияние на формирование высокой биомассы. Из 88 образцов, несущих доминантный аллель Ppd-D1a гена Ppd -D1, три генотипа были идентифицированы с аллелем Rht-D1b, а 31 – с аллелем Rht-B1b. Эти генотипы, включая 10 сортов, созданных в разные годы, могут быть успешно использованы для создания новых разновидностей с комплексом положительных признаков.
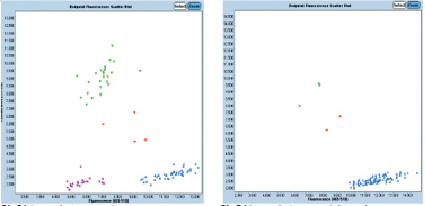
Рис. 1. Скрининг 96 генотипов мягкой пшеницы по генам Rht-B1 (слева) и Rht-D1 (справа). Синий – нормальный, зеленый – мутантный, красный – гетерозиготный, розовый – неизвестный
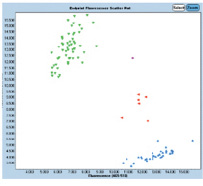
Рис. 2. Скрининг 96 образцов мягкой пшеницы по гену PPdD1. Зеленый – нечувствительные к фотопериоду, синий – чувствительные к фотопериоду, красный – гетерозиготный
Аллель Glu-D1a локуса Glu-D1, расположенной на длинном плече 1-й хромосомы и кодирующей глютеиновые субъединицы [20, 21], широко распространен у мягкой пшеницы и положительно влияет на хлебопекарное качество [22]. Для поиска ценных генов запасных белков была проведена оценка аллельного состава локуса Glu-D1 коллекции сортов мягкой пшеницы и выделены генотипы, несущие аллели Glu-D1a. При анализе частоты встречаемости аллелей локуса Glu-D1 показано, что 34 генотипа содержали аллель Glu-D1a, среди которых 31 образец оказался гомозиготой, 3 – гетерозиготами. Носителями аллеля Glu-D1a также оказались 7 селекционных сортов (Сяба, Тале 38, Сианотрикс 334/12, Арзу, Гарабах, Зердаби и Гюнешли). Jin с коллегами (2011) в результате скрининга 718 сортов из 20 стран, с помощью маркеров, сцепленного генами Glu-A1 и Glu-D1, обнаружили, что 50 % исследованных сортов являются носителями аллелей Glu-A1b или Glu-D1d [23]. Другой показатель – содержание протеина – оказывает большое влияние на хлебопекарные свойства пшеницы, так как воздействует на абсорбцию воды и формирование теста. Среди исследованных образцов выявлен только один образец разновидности var. milturum из Агдамского региона, несущий аллель, связанный с высоким содержанием белка. Указанный генотип с высоким содержанием белка можно использовать в селекционной работе в качестве доноров для выведения перспективных образцов.
Несмотря на большое разнообразие исследований, связанных с применением KASP-маркеров, основная часть этих работ нацелена на селекцию по признакам устойчивости к вирусам и болезням, а также к гербицидам. Устойчивость к различным болезням является чрезвычайно важным признаком у разных культур, но гены, контролирующие данные признаки, как и их нуклеотидные последовательности, остаются пока неизвестными. К настоящему времени во всем мире у пшеницы идентифицирован 71 ген устойчивости к листовой (Lr) и 57 стеблевой (Sr) ржавчине, которые использовались в селекционных программах. Гены Lr 21 и Lr 34 обеспечивают устойчивость у взрослых растений. В наших исследованиях, в результате скрининга, не выявлен ген Lr 21 и изученные генотипы можно охарактеризовать как восприимчивые к листовой ржавчине. Однако у 17 генотипов была установлена устойчивость по гену Lr 34, а 33 образца оказались носителями гена устойчивости в гетерозиготном состоянии. Среди сортов была выявлена устойчивость только у Сяба и Гюнешли. Приведенные выше сорта могут быть использованы в качестве ценного источника в селекционной работе, направленной на повышение устойчивости к листовой ржавчине.
Единственный ген устойчивости к стеблевой ржавчине, не являющийся расоспецифическим (Sr2), был выявлен у вида Triticum turgidum ssp. dicoccum (Schrank ex Schubler) Thell (Triticum dicoccum Schrank ex Schubler) [24]. В настоящем исследовании в результате скрининга по гену Sr2 все образцы оказались восприимчивыми к стеблевой ржавчине.
Наряду с биотрофными анализами мягкой пшеницы был также проведен гемибиотрофный анализ устойчивости к желтой пятнистости (Tsn) и фузариозу колоса, в результате чего получен ряд различных результатов. Несмотря на то, что было выявлено несколько QTL для устойчивости к фузариозу колоса, большинство исследователей в этом направлении подчеркивают, что наиболее важными являются гены Fhb1, расположенные в хромосоме 3BS, Fhb2 – в хромосоме 6 BS и Fhb5 – в хромосоме 5AS.
В наших исследованиях результаты скрининга локуса Fhb 5A выявили устойчивость 47 генотипов к фузариозу колоса, остальные образцы оказались чувствительными. Отмечена гетерозиготность четырех генотипов по этому локусу.
Скрининг генов устойчивости к желтой пятнистости выявил чувствительность всех образцов изученной коллекции.
Заключение
Таким образом, в результате скрининга 11 локусов, контролирующих хозяйственно ценные признаки, у 166 сортов и разновидностей в коллекции мягкой пшеницы были выявлены новые ценные генные источники.
Для всех генов, за исключением трех локусов (Lr 21, Tsn и Sr 2), были идентифицированы генотипы, обладающие селекционно значимыми аллелями.
Из 166 исследованных генотипов положительные результаты были достигнуты только у 20, а каждый из оставшихся 146 образцов (в гомо- или гетерозиготном состоянии) оказались носителями желаемых аллелей. С целью расширения генетического разнообразия эти образцы могут быть использованы как доноры продуктивности и устойчивости к болезням в различных селекционных программах. У разновидности мягкой пшеницы var. meridionale был выявлен 1, у сорта Гюнешли и разновидности var. alborubrum – 4 положительных аллеля. Эти сортообразцы, как генотипы с комплексом положительных признаков, рекомендованы для получения продуктов высокого качества в различных хозяйствах и как родительские формы для гибридизации.
Библиографическая ссылка
Аббасов М.А. ГЕНОТИПИРОВАНИЕ ОБРАЗЦОВ МЯГКОЙ ПШЕНИЦЫ (T. AESTIVUM L.) АЗЕРБАЙДЖАНА НА ОСНОВЕ KASP ТЕХНОЛОГИИ // Успехи современного естествознания. 2019. № 8. С. 7-12;URL: https://natural-sciences.ru/ru/article/view?id=37175 (дата обращения: 15.05.2026).



