Scientific journal
Advances in current natural sciences
ISSN 1681-7494
"Перечень" ВАК
ИФ РИНЦ = 0,976
RESEARCH OF APPLICATION CONDITIONS OF SOME ORGANIC SOLVENTS FOR CLEARING OF INULINASE FROM VARIOUS SOURCES
Инулиназы различного происхождения расщепляют инулин и другие фруктозосодержащие полимеры до фруктозы, воздействуя на гликозидные связи. Инулиназа (инулаза; 2,1-β-D-фруктан-фруктаногидролаза, КФ 3.2.1.7.) широко распространена среди высших растений и микроорганизмов. Данный фермент может применяться для получения фруктозы из растительного сырья: топинамбура, георгина, девясила, цикория, одуванчика, лопуха. Сиропы с высоким содержанием фруктозы, полученные путем ферментативного гидролиза экстрактов инулинсодержащих растений, могут быть широко использованы в кондитерской промышленности, в лечебном питании больных сахарным диабетом, а также для профилактики кариеса и ожирения.
УСЛОВИЯ ЭКСПЕРИМЕНТА
Объектами исследования послужили инулиназы из Aspergillus awamori 2250 и Saccharomyces cerevisiae ВГШ-2 (ВКПМ, Москва). В качестве субстрата для ферментативной реакции применяли инулин (Spofa, Прага).
Фермент экстрагировали из высушенной и измельченной культуры продуцента при 20-25 °С в течение 1,5 ч. Осаждение инулиназ проводили при температуре -4 °С и значении рН 4,0, полученный осадок отделяли центрифугированием, высушивали на воздухе и взвешивали. Содержание белка определяли методом Лоури [5], каталитическую активность измеряли спектрофотометрически на фотоэлектроколориметре КФК-3 (Россия) при помощи реакции Селиванова [2].
Статистическую обработку результатов экспериментов проводили с помощью пакета программ «Statgraphics». Достоверность отличий контрольных и экспериментальных результатов оценивали при помощи t-критерия Стьюдента.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
В этой работе нами было изучено влияние различных концентраций этанола и ацетона на эффективность осаждения инулиназы Aspergillus awamori и различных концентраций ацетона и изопропанола на степень очистки инулиназы Saccharomyces cerevisiae. Данные экспериментов (рис. 1 и 2) свидетельствуют о том, что использование этанола и ацетона в диапазоне концентраций 50 %-80 % по-разному отражается на выходе инулиназы Aspergillus awamori и эффективности ее очистки. Максимальный выход фермента наблюдается при концентрации ацетона 65 % и составляет 85 %, что на 5 % больше этой же величины, чем при осаждении этанолом. Более низкие концентрации данного растворителя (50 %), хотя и сохраняют большую активность инулиназы (до 13 ед/мг), но выход энзима при этом оказывается ниже. Более высокие концентрации ацетона (80 %) резко уменьшают ферментативную активность. Таким образом, оптимальной концентрацией ацетона для осаждения инулиназы из поверхностной культуры Aspergillus awamori является 65 %, в этом случае выход фермента и эффективность очистки максимальны.
В следующей серии экспериментов мы исследовали влияние этанола в различных концентрациях на процесс очистки инулиназы Aspergillus awamori. Оказалось, что для осаждения фермента этанолом требуется большая концентрация спирта - 75 %. При этом эффективность очистки максимальна, выход фермента составляет 81 %, а удельная активность оказывается на 7 % ниже этой же величины, чем при использовании оптимальной концентрации ацетона.
Анализируя полученные результаты, мы пришли к выводу, что использование ацетона в концентрации 65 % является наиболее эффективным, рациональным и экономичным. Ацетон обладает меньшим денатурирующим действием, чем этанол, отчасти потому, что требуются более низкие его концентрации для получения фермента. Кроме того, ацетон более летуч, что позволяет легко удалять его из полученного препарата, к тому же он оказывает стабилизирующее действие на белковую молекулу фермента.
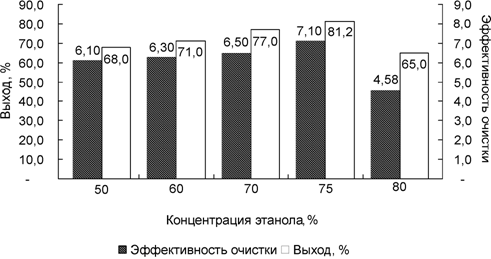
Рис. 1. Влияние различных концентраций ацетона на очистку инулиназы Aspergillus awamori
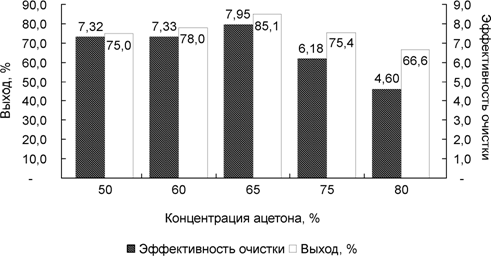
Рис. 2. Влияние различных концентраций этанола на очистку инулиназы Aspergillus awamori
Литературные данные указывают на то, что концентрация ионов водорода в среде может влиять на процесс осаждения ферментов органическими растворителями [1, 3]. В связи с этим, следующая серия экспериментов была посвящена изучению влияния различных значений pH на каталитическую активность инулиназы и степень ее очистки в ходе осаждения ацетоном оптимальной концентрации из поверхностной культуры Aspergillus awamori (рис. 3).
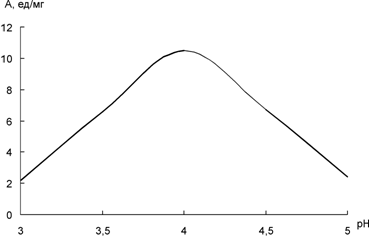
Рис. 3. Влияние различных значений pH на активность инулиназы Aspergillus awamori при осаждении ее ацетоном
Показано, что для выпадение инулиназы в осадок из раствора наиболее перспективным является значение pH 4,0. Данная концентрация ионов водорода, по-видимому, близка к изоэлектрической точке инулиназы из Aspergillus awamori. Известно, что почти все глобулярные белки при значении pH раствора, близком к их изоэлектрической точке, обладают меньшей растворимостью [4], так как в этом случае молекула не несет суммарного заряда и, следовательно, между соседними белковыми глобулами отсутствует электростатическое отталкивание. Поскольку белки, имеющие различные изоэлектрические точки, осаждаются при различных концентрациях ионов водорода в среде, используя оптимальное для осаждения инулиназы значение pH, можно успешно освобождаться от сопутствующих белков в ходе очистки.
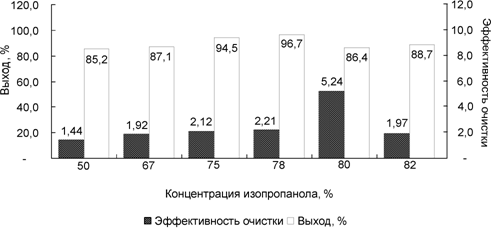
Рис. 4. Влияние различных концентраций изопропанола на очистку инулиназы Saccharomyces cerevisiae
Наши исследования показали, что обоими органическими растворителями инулиназа Saccharomyces cerevisiae осаждалась монотонно с последовательным увеличением их концентрации. На рис. 4 и 5 представлены данные о влиянии концентрации изопропанола и ацетона на осаждение инулиназы.
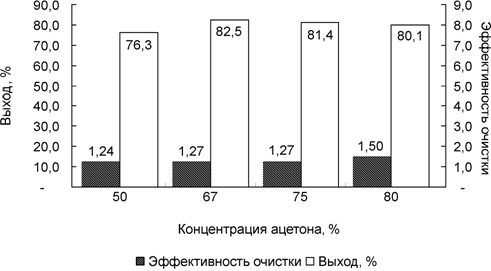
Рис. 5. Влияние различных концентраций ацетона на очистку инулиназы Saccharomyces cerevisiae
Показано, что лучшим осадителем для инулиназы Saccharomyces cerevisiae является изопропанол при содержании его в смеси в объемных соотношениях 1:3,5. В этом случае выход фермента составил 96,7 % при степени очистки 2,21. Самая высокая удельная активность энзима (9,54 ед/мг) получена при концентрации изопропанола 1:4, выход фермента в этом случае достигал 86,4 %.
Максимально возможный выход инулиназы, полученный при использовании ацетона в соотношении 1 объем растворителя на 3 объема экстракта составил 86,9 % при степени очистки 1,14.
Таким образом, анализ полученных результатов позволил заключить, что для получения технического препарата инулиназы из продуцентов Aspergillus awamori и Saccharomyces cerevisiae можно успешно использовать любой из указанных органических растворителей (этанол, изопропанол, ацетон) в оптимальных концентрациях.
СПИСОК ЛИТЕРАТУРЫ:
- Диксон М., Уэбб Э. Ферменты. М.: Мир, 1982. Т. 1-3. 1118 с.
- Ермаков А.И., Арасимович В.В., Ярош Н.П. Методы биохимического исследования растений. Л.: Агропромиздат, 1987. 429 с.
- Тертычная Т. Н. Исследование биосинтеза и некоторых физико-химических свойств инулазы: автореф. дис. канд. биол. наук. ВорГУ. Воронеж, 1994. 24 с.
- Уильямс В., Уильямс Х. Физическая химия для биологов. М.: Мир, 1976. 600 с.
- Lowry O.N., Rosebrough N.J., Farr A.L., Randall R.J. // J. Biol. Chem., 1951. - Vol. 193. - P. 265-275.
Библиографическая ссылка
Ковалева Т.А., Холявка М.Г., Сапрыкина Н.И. ИССЛЕДОВАНИЕ УСЛОВИЙ ПРИМЕНЕНИЯ РЯДА ОРГАНИЧЕСКИХ РАСТВОРИТЕЛЕЙ ДЛЯ ОЧИСТКИ ИНУЛИНАЗ ИЗ РАЗЛИЧНЫХ ИСТОЧНИКОВ // Успехи современного естествознания. 2008. № 9. С. 14-18;URL: https://natural-sciences.ru/en/article/view?id=10541 (дата обращения: 17.05.2026).



