Scientific journal
Advances in current natural sciences
ISSN 1681-7494
"Перечень" ВАК
ИФ РИНЦ = 0,976
Neuroendocrine interactions in the system: hypothalamus-pituitary-adrenal cortex under inflammation
сделанные в начале и середине ХХ столетия, когда было показано, что нейроны гипоталамической области мозга способны, сохраняя присущую им организацию и импульсную активность, секретировать пептидные нейрогормоны [3,4]. Первоначально это относилось к способности крупноклеточных нейронов гипоталамуса синтезировать нонапептиды (окситоцин, вазопрессин и их гомологи), транспортировать их по аксонам в заднюю долю гипофиза и оттуда выделять в общий кровоток. Последнее роднило нервные клетки гипоталамуса с эндокринными, с секреторными клетками эндокринных желез, поэтому сам феномен был назван нейросекрецией [5].
Впоследствии выяснилось, что нейросекреция свойственна также тем популяциям мелкоклеточных нейронов гипоталамуса, которые регулируют гормональные функции передней доли гипофиза с помощью стимулирующих нейрогормонов (либеринов) и тормозящих нейрогормонов (статинов), транспортируемых в переднюю долю гипофиза гуморальным путём через кровоток портальной системы гипофиза [6].
Наконец, когда по аналогии с клетками гипофиза, на мембранах секреторных нейронов гипоталамуса были выявлены рецепторы к гормонам периферических эндокринных желез, стали понятны механизмы гипоталамической регуляции эндокринных функций. В их основе, как было установлено ранее для гипофиза, лежит принцип обратной связи, который определяет работу контролирующих механизмов [6].
Эти яркие открытия и вытекающие из них заключения стали краеугольным камнем, который лёг в основу новой для того времени области знаний - нейроэндокринологии. Родившись на стыке казалось бы различных дисциплин, нейробиологии и эндокринологии, нейроэндокринология дала новое измерение нашим знаниям о механизмах, лежащих в основе регуляции важнейших гомеостатических функций. Родившись на стыке различных дисциплин, нейроэндокринология оказалась важной ветвью нейронаук. Она раскрыла эндокринные функции мозга и подняла завесу над некоторыми его тайнами.
Между тем удивительные факты продолжали накапливаться, однако фокус новых открытий сместился в область иммунологии. Стало обнаруживаться большое сходство в организации и функционировании нервной и иммунной систем. Если выше при обсуждении общности нервной и эндокринной систем упоминалось о том, что нейроны, сохраняя специфическую организацию и функцию (генерирование и распространение нервных импульсов) могут одновременно
функционировать как эндокринные клетки, то оказалось, что аналогичное можно сказать и о клетках иммунной системы. Участвуя в регуляции гомеостаза с помощью специфических иммунных механизмов, эти клетки оказались способными экспрессировать рецепторы ко многим сигнальным молекулам, опосредующим воздействия нейроэндокринной системой [2,7], а также синтезировать некоторые эволюционно древние (консервативные) пептиды. В их ряду заслуживают упоминания нейропептиды, тахикинины, инсулиновые гормоны, проопиомеланокортин, дериватами которого являются АКТГ, β-эндорфин и меланоцит-стимулирующий гормон, и, наконец, гормон роста и пролактин, рецепторы которых относятся к большому семейству гемопоэтиновых - рецепторов к интерлейкинам, эритропоэтину, гранулоцитарно-макрофагальному колониеобразующему фактору [7-9].
При анализе сходства в организации нервной и иммунной систем привлекает внимание тот факт, что обе системы состоят из большого числа фенотипически различающихся клеток, организованных в сложные сети. В пределах такой сети клетки взаимосвязаны и функционируют по принципу обратной связи, когда пусковым сигналом служит адекватный раздражитель, а конечный ответ направлен на обеспечение полезного результата. Различие заключается в том, что в нервной системе клетки жестко фиксированы в пространстве, тогда как в иммунной они непрерывно перемещаются и лишь кратковременно взаимодействуют друг с другом.
Наиболее демонстративно взаимодействия нейроэндокринной и иммунной систем проявляются в реакции стресс. Известно, что эта защитная биологическая реакция развивается в ответ на действие широкого спектра агрессивных факторов внешней среды, таких как микробные, температурные, болевые агенты, факторы неподвижности, гравитации, психоэмоциональные воздействия и ряд других. При всех этих воздействиях активируется гипоталамо-гипофизарноадренокортикальная система (ГГАС).
Центральным звеном этой системы являются нейроэндокринные нейроны паравентрикулярного ядра (ПВЯ) гипоталамуса, синтезирующие кортикотропин-рилизинг гормон (КРГ). Их аксоны следуют к наружной зоне срединного возвышения, откуда КРГ поступает в портальный кровоток, достигая клеток аденогипофиза. КРГ через рецепторы 1 типа, активирующие цАМФ, стимулирует синтез проопиомеланокортина (ПОМК) и его деривата АКТГ. Последний вызывает выделение и синтез глюкокортикоидов, которые оказывают множество общеизвестных эффектов, в том числе ограничивают распространение воспаления. Важно подчеркнуть, что помимо КРГ, в мелкоклеточных нейронах гипоталамуса синтезируется еще один нейрогормон - вазопрессин (ВП), который через рецепторы 1б типа действует синергично с КРГ на АКТГ клетки гипофиза [10,11].
Ещё Ганс Селье, впервые описавший стресссиндром, отмечал, что иммунная система остаётся небезразличной к стрессу. Позднее были исследованы механизмы, с помощью которых иммунная система вовлекается в стрессовые реакции. Так, было показано, что в ответ на действие патогенных агентов макрофаги и лимфоциты выделяют широкий спектр регуляторных пептидов, объединенным общим названием цитокинов. Эти иммунные пептиды способен проникать в мозг через гемато-энцефалический барьер в тех его участках, где существуют "окна" для подобного рода веществ. К ним относятся система циркумвентрикулярных органов (срединное возвышение нейрогипофиза, субфорникальный орган, задняя крайняя область или area postrema), в которых существуют специфические механизмы транспорта для цитокинов. Пониженная барьерная активность в таких участках обусловлена особенностями организации, в первую очередь, наличием капилляров с фенестрированным эндотелием, облегчающим транспортировку цитокинов в нервную ткань из общего кровотока [12].
Попав в мозг, цитокины (и, в первую очередь, интерлейкин-1, ИЛ-1) стимулирует секрецию центрального нейрогормона стресса КРГ в нейросекреторных нейронах ПВЯ гипоталамуса. Причем, этот процесс зависит от присутствия простагландина Е2 и окиси азота. В свою очередь, КРГ стимулирует секрецию АКТГ в гипофизе, что приводит к стимуляции секреции глюкокортикоидных гормонов в коре надпочечников. Последние при повышенной секреции способны тормозить секрецию ИЛ-1 в макрофагах и тем самым угнетать иммунный ответ в случае его избыточности. Таким образом, здесь в чистом виде работают механизмы отрицательной обратной связи, в которых роль триггера выполняет иммунный пептид, а функцию исполнителя - нейрогормон гипоталамуса и гормоны эндокринной системы [1,12].
Изучение тонких механизмов взаимодействия нейроэндокринной и иммунной систем мы продолжили в исследованиях, которые проводили совместно с отделом физиологии эндокринной системы (G. Aguilera) одного из Национальных Институтов Здоровья США. В них мы исследовали влияние острого и хронического иммунного стресса на состояние ГГАС у крыс. Острый иммунный стресс воспроизводился введением эндотоксина липополисахарида (ЛПС) E. Coli в дозе 250мкг/100г внутрибрюшинно (в/б), а хронический - длительным введением этого антигена в нарастающих дозах от 25 до 250 мкг/100 г в течение 13-ти дней [13]. Об активности нейроэндокринной оси судили по динамике экспрессии соответствующей мРНК: в паравентрикулярном ядре - КРГ, в гипофизе - ПОМК, в коре надпочечников -11β-гидроксилазы с помощью метода гибридизации in situ. Дополнительно исследовали динамику экспрессии мРНК рецепторов к КРГ и глюкокортикоидам (кортикостерон). Помимо этого, радиоиммунным методом оценивали уровни АКТГ и кортикостерону в крови [13].
Полученные результаты оказались весьма любопытными. Так, было показано, что реакция ГГАС на острое воспаление, вызванное однократной инъекцией ЛПС, характеризуется активацией всех звеньев этой системы, включая синтез КРГ и ВП в мелкоклеточных ПВЯ гипоталамуса [13,14]. Напротив, при длительном введении ЛПС в нарастающих дозах, происходит парадоксальное подавление синтеза КРГ и нарастание синтеза ВП [13].
Подобная картина наблюдается и при ряде длительных воспалительных аутоиммунных заболеваний, таких как артрит, системная красная волчанка и аллергический энцефаломиелит и другие [15-17]. Подавление синтеза КРГ в этих случаях может быть связано как с длительным угнетающим действием глюкокортикоидов, уровни которых повышены, так и с дисбалансом нейротрансмиттеров в гипоталамусе. В любом случае, при подавлении синтеза центрального нейрогормона ГГАС, отмечается парадоксальная активация ее гипофизарно-надпочечникового звена [15-17].
В качестве модели аутоиммунной патологии, демонстрирующей вовлечённость и взаимодействие трёх регулирующих систем в механизмах развития заболевания, может служить такое аутоиммунное заболевание как артрит, экспериментально вызываемый с помощью введения адьюванта культуры убитых нагреванием Micobacteium butyricum [15]. Как упоминалось ранее, при этой патологии отмечается парадоксальное подавление синтеза КРГ, сочетающееся с повышенной продукцией АКТГ и глюкокортикоидов. В этих условиях ответ на психоэмоциональный стресс заметно снижен.
Однако при изучении реакции этой оси на иммунный стресс (однократное в/б введение ЛПС в дозе 200 мкг животным с артритом) нами в сотрудничестве с Национальными Институтами Здоровья США (G. Aguilera), Университетом Бристоля, Англия (S. Lightman, M. Harbuz) и Свободным Университетом Амстердама, Голландия (F. Tilders) была обнаружена выраженная активация всех ее звеньев ГГАС [18]. Естественно, нас заинтересовали причины такой необычной реакции, в силу чего были исследован синтез и секреция наиболее значимых провоспалительных цитокинов - ИЛ-1 и ИЛ-6. Оказалось, что введение ЛПС на фоне артрита приводит к резкому нарастанию в крови уровней цитокинов в крови и их экспрессия в головном мозге и периферических органах [18].
Обобщенная схема нейроиммуноэндокринных взаимодействий в регуляции гипоталамогипофизарно-адреналовой системы при остром и хроническом воспалении представлена на рисунке (приводится по [19]). В то время как при остром воспалении происходит активация центральных звеньев ГГАС, то при хроническом выявляется подавление синтеза КРГ и нарастание синтеза ВП в мелкоклеточных нейронах гипоталамуса, что совпадает с активацией синтеза АКТГ и глюкокортикоидов. При сочетании острого и хронического воспаления обнаруживается цитокин-зависимая потенциация активности всех звеньев ГГАС. Подобная корреляция иммунной и нейроэндокринной систем была обозначена нами как феномен гиперчувствительности ГГАС к иммунному стрессу при хроническом (аутоиммунном) воспалении.
Таким образом, ГГАС служит удобным «объектом» для изучения нейроиммуноэндокринных взаимодействий, а представленные сведения могут являться теоретическим базисом для изучения патофизиологии хронических воспалительных и аутоиммунных заболеваний, их диагностики и коррекции у человека.
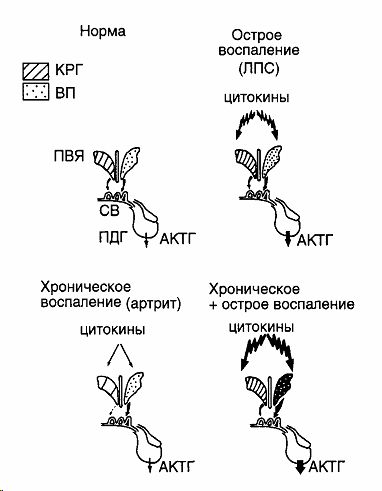
Рис 1. Гиперреактивность гипоталамо-гипофизарно-адренокортикальной системы при хроническом воспалении (артрит) в ответ на острое воспаление, вызванное новым антигеном (ЛПС). Стимуляция синтеза основных нейрогормонов стрессорной оси - кортикотропин-рилизинг гормона (КРГ) и вазопрессина (ВП) "мелкоклеточного происхождения", а также синтеза проопиомеланокортина в передней доле гипофиза и выделения в кровь АКТГ происходит за счет повышенной продукции цитокинов в головном мозге и периферических органах и их содержания в общем кровотоке. ПВЯ - паравентрикулярное ядро гипоталамуса, ПДГ - передняя доля гипофиза, СВ - срединное возвышение нейрогипофиза (по И.Г.Акмаеву и В.В.Гриневичу, 2001 [19]).
Литература
- Besedovsky H., del Rey A., Sorkin E. et al. Immunoregulatory feedback between interleukin-1 and glucocorticoid hormones. // Science.1986.V. 233. P. 652-654.
- Blalock J.E., Bost K.L. Neuroimmunoendocrinology. // Prog. Allergy. 1988.V. 43. P. 1-165.
- Scharrer E. Die Lichtempfindilichkeit blinder Elritzen (Untersuchungen über das Zwischenhirn der Frische. I.). // Z. Vergleich. Physiol. 1928. Bd. 7. S. 1-38.
- Scharrer E., Scharrer B. Secretory cells within the hypothalamus. // Res. Publ. Ass. Res.Nerv. Ment. Dis.1940. V. 20. P. 170-194.
- Scharrer E., Scharrer B. Neurosecretion. // Handbucher der mikroskopischen Anatomie des Menschen / Hrsg.: W. Bargmann. Berlin. Springer.1954. Bd. 6. T. 5. S. 953-1066.
- Schally A.V., Arimura A., Bowers C.Y. et al. Hypothalamic neurohormones regulating anterior pituitary function. // Rec. Prog. Horm. Res.1968. V.24. P. 497-588.
- Blalock J.E. The syntax of immune-neuroendocrine communication. // Immunol. Today. 1994.V. 15. P. 504-511.
- Ericsson A., Geenen V., Robert F. et al. Expression of preprotachykinin-A and neuropeptide-Y messenger RNA in the thymus. // Mol. Endocrinol.1990. V. 4. P. 1211-1218.
- Geenen V., Legros J.J., Franchimont P. et al. The neuroendocrine thymus: coexistence of oxytocin and neurophysin in the human thymus. // Science.1986. V. 232. P. 508-511.
- Aguilera G. Regulation of pituitary ACTH secretion during chronic stress. // Front. Neuroendocrinol. 1994. V. 15. P. 321-350.
- Гриневич В.В., Поскребышева Е.А., Савелов Н.А. и др. Иерархические взаимоотношения между органами гипоталамо-гипофизарно адреналовой системы (ГГАС) при воспалении. //Успехи физиол. наук. 1999. Т.30. С. 50-66.
- Turnbull A.V., Rivier C.L. Regulation of the hypothalamic-pituitary-adrenal axis by cytokines: actions and mechanisms of action. // Physiol. Rev.1999. V. 79. P. 1-71.
- Grinevich V., Ma X.M., Herman J.P. et al. Effect of repeated lipopolysaccharide administration on tissue cytokine expression and hypothalamicpituitary-adrenal axis activity in rats. // J. Neuroendocrinol. 2001. V.13. P. 711-723.
- Grinevich V., Ma X-M., Verbalis J., Aguilera G. Hypothalamic-pituitary-adrenal axis and hypothalamic-neurohypophyseal responses to restraint or immune challenge in water deprived rats. // Exper. Neurol. 2001. V. 171. P. 329-341.
- Harbuz M.S., Lightman S.L. Stress and hypothalamo pituitary-adrenal axis: Acute, chronic and immunological activation. // J. Endocrinol.1992. V. 134. P. 327-339
- Harbuz M.S., Rees R.G., Eckland D. et al. Paradoxical responses of hypothalamic corticotropin releasing factor (CRF) messenger ribonucleic acid (mRNA) and CRF-41 peptide and adenohypophysial proopiomelanocortin mRNA during chronic inflammatory stress. // Endocrinology. 1992. V. 130. P. 1394-1400.
- Harbuz M.S., Rees R.G., Lightman S.L. HPA axis responses to acute stress and adrenalectomy during adjuvant-induced arthritis. // Am. J. Physiol. 1993. V. 264. P.R179-185.
- Grinevich V., Harbuz M., Ma X.-M et al. Hypothalamic pituitary adrenal axis and immune responses to endotoxin in rats with chronic adjuvantinduced arthritis. // Exp. Neurol. 2002. V. 178. P.112-123.
- Акмаев И.Г., Гриневич В.В. От нейроэндокринологии к нейроиммуноэндокринологии. //Бюл. эксперим. биол. 2001. Т.131, №1. С. 22-32
Библиографическая ссылка
Гриневич В.В., Волкова О.В., Акмаев И.Г. НЕЙРОИММУНОЭНДОКРИННЫЕ ВЗАИМОДЕЙСТВИЯ В СИСТЕМЕ: ГИПОТАЛАМУС-ГИПОФИЗ-КОРА НАДПОЧЕЧНИКОВ ПРИ ВОСПАЛЕНИИ // Успехи современного естествознания. 2003. № 5. С. 10-14;URL: https://natural-sciences.ru/en/article/view?id=14276 (дата обращения: 07.05.2026).



