В настоящей работе допущено, что взаимодействие сахарозы с гидроксидами щелочных и щелочноземельных металлов носит ионообменный характер. В связи с этим проведены экспериментальные исследования рН тройных растворов вода-сахароза-гидроксид кальция в интервале температур 333,15 - 353,15 К.
В связи с тем, что в молекуле сахарозы наиболее подвижны три атома водорода, а также с учетом ступенчатой диссоциации гидроксида кальция в водных растворах, равновесия в системе вода-сахароза-гидроксид кальция имеют вид:
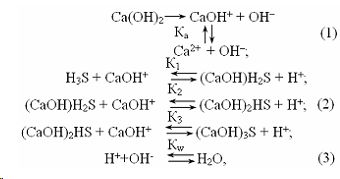
где Ка - константа диссоциации гидроксида кальция по второй ступени;
H3S - сахароза;
(СаОН)H2S, (СаОН)2HS, (СаОН)3S - моно- ди- и тризамещенные сахараты кальция;
К1, К2, К3 - константы ионного обмена;
Кw - термодинамическая константа диссоциации воды.
Так как три наиболее подвижных атома водорода в молекуле сахарозы значительно удалены друг от друга, принято, что их участие в ионообменных взаимодействиях имеет статистический характер, поэтому:
![]()
С использованием ранее установленных величин Ка и опытных данных о рН растворов вода-сахароза-гидроксид кальция различных составов рассчитаны значения константы К1 в интервале температур 333,15-353,15 К и приведены в табл.
Таблица. Величины константы К1 в интервале температур 333,15 - 353,15 К
|
Т, К |
333,15 |
343,15 |
353,15 |
|
К1 107 |
1,18 |
1,57 |
2,34 |
Значения рН водных растворов сахарозы и гидроксида кальция различных составов, рассчитанные с использованием полученных констант, удовлетворительно согласуются с экспериментальными данными, что свидетельствует о справедливости допущения об ионообменном характере взаимодействия сахарозы с гидроксидами щелочных и щелочноземельных металлов.
Имея данные о величие К1, можно рассчитать равновесный состав тройных растворов, а также растворимость гидроксида кальция в водно-сахарных растворах в интервале температур 333,15-353,15 К.



