Scientific journal
Advances in current natural sciences
ISSN 1681-7494
"Перечень" ВАК
ИФ РИНЦ = 0,976
THE INFLUENCE OF MICROENCAPSULATION ON THE PHYSICAL-TECHNOLOGICAL CHARACTERISTICS MICROCAPSULES AFOBAZOL
Микрокапсулирование - новая, быстро развивающаяся технология, нашедшая наибольшее применение в медицине и ветеринарии. Микрокапсулирование решает вопросы получения лекарственных препаратов пролонгированного действия, маскировки их неприятных вкусовых качеств.
Метод воднофазового разделения относится к одному из наиболее распространенных методов микрокапсулирования. В основе его лежит явление коацервации, при этом равновесный полимерный раствор в определенных условиях разделяется на две жидкие фазы: первая - с высоким содержанием полимера (коацерват) и вторая - с низким содержанием полимера в растворе. Коацерват находится в системе в виде капель, слияние которых приводит к образованию сплошного слоя [1]. Коацервация, или концентрирование материала оболочки вокруг частиц капсулируемого вещества, вызывается различными факторами: введение химических реагентов, изменением рН среды, изменением температуры [2].
Цель исследования - изучение влияния технологических параметров микрокапсулирования на такие свойства микрокапсул, как фактор формы (F), насыпная масса (Н), сыпучесть(V), средний диаметр частиц (dm), средний объемно-поверхностный диаметр (dvs).
Материал и методы исследования
Для проведения эксперимента нами методом простой коацервации были получены микрокапсулы афобазола. В качестве материала оболочки использовали пищевой желатин.
Образцы микрокапсул получали следующим образом. Готовили дисперсию лекарственного вещества в растворе полимера, к раствору пленкообразователя добавляли водный раствор натрия сульфата, который вызывал коацервацию желатина. Полученные микрокапсулы сушили в сушилках с водоотнимающими средствами.
Контроль процесса осуществляли микроскопически и по изменению оптической плотности среды на фотоколиметре. Процесс проводили при температуре 40 ± 1 °С. Основной стадией является получение коацервата.
Микрокапсулирование проводили при соотношениях полимер/ядро: 1:1 (I). 1:1,5 (II), 1:2 (III), 1:2,5 (IV), 1:3 (V).
Гранулометрический состав исследовали микроскопическим методом. Для построения графической зависимости измеряли горизонтальные диаметры 400 частиц и группировали по фракциям с интервалом 25 мкм.
dvs (в мкм) микрокапсул рассчитывали по формуле:
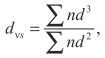
где d - среднеарифметический размер узкой фракции, мкм; n - количество частиц в узкой фракции.
Фактор формы определяли как отношение максимального и минимального диаметров.
Сыпучесть и насыпную плотность микрокапсул определяли по известным методикам.
Содержание оболочки определяли весовым способом после разрушения микрокапсул в ступке и промывки масляного раствора гексаном.
Результаты исследования и их обсуждение
Изучено влияние количества капсулируемого вещества на технологический процесс и физико-технологические показатели качества микрокапсул. На рис. 1 представлены данные об изменении оптической плотности системы желатин - вода - сульфат натрия от концентрации добавленного сульфата натрия. Как видно, резкое возрастание оптической плотности происходит в очень узком интервале концентрации сульфата натрия. Передозировка раствора соли приводит к коагуляции желатина. Нами выбрана 20 % концентрация сульфата натрия в качестве оптимальной.
Установлено минимальное количество частиц, необходимое для получения статистически достоверных результатов. В ходе исследования установлено, что dm, рассчитанные измерением 400 частиц, имели близкие величины (ошибка опыта не превышала 4 %).
На рис. 2 представлен графический метод определения dm микрокапсул, полученных при соотношении полимер/ядро 1:2.
Микрокапсулы были представлены частицами по форме близкими к сферической, при этом F различных образцов не превышало 1,8.
На рис. 3 показано изменение содержания оболочек при увеличении загрузки масляной фазы.
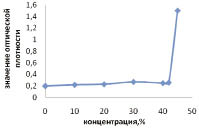
Рис. 1. Зависимость оптической плотности (D) системы желатин - вода - сульфат натрия от концентрации добавленного сульфата натрия

Рис. 2. Графический метод определения среднего диаметра микрокапсул
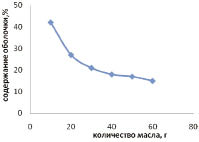
Рис. 3. Изменение содержания оболочки микрокапсул от содержания масла
Как видно, толщина оболочки микрокапсул при увеличении загрузки масляной фазы уменьшается, количество оболочечного материала становится недостаточным для покрытия всех капель эмульсии, и часть масла остается незакапсулированной, что приводит к получению продукта с плохой сыпучестью. Поэтому оптимальным можно считать соотношение полимер/ядро 1:2 и 1:2,5.
Показатели качества микрокапсул
в зависимости от массового соотношения полимер/ядро
|
Показатель качества |
Образцы микрокапсул |
|||||
|
I |
II |
III |
IV |
V |
VI |
|
|
F |
1,31 |
1,34 |
1,47 |
1,63 |
1,71 |
1,75 |
|
V, г/с |
12,1 |
11,2 |
10,9 |
9,7 |
9,2 |
8,7 |
|
H, г/мл |
0,35 |
0,35 |
0,36 |
0,41 |
0,46 |
0,40 |
|
dm , мкм |
190 |
193 |
189 |
192 |
190 |
188 |
|
dvs , мкм |
211 |
220 |
209 |
218 |
211 |
208 |
Из таблицы видно, что изменение соотношения полимер/ядро от 1:1 до 1:3 сопровождалось уменьшением сыпучести микрокапсул. Очевидно, уменьшение показателя сыпучести конечного продукта при увеличении капсулируемого вещества в системе можно объяснить изменением формы частиц. Так, при минимальном и максимальном содержании масляной фазы F микрокапсул равнялся 1,31 и 1,75 соответственно.
Заключение
На основании исследования условий микрокапсулирования частиц лекарственных веществ методом простой коацервации выявлены наиболее характерные зависимости показателей качества микрокапсул и технологических параметров процесса.
При увеличении количества капсулируемого вещества в системе отмечено увеличение насыпной массы и степени ассиметрии микрокапсул. Установлено уменьшение таких показателей, как содержание оболочки и сыпучесть. При этом изменение массового соотношения полимер/ядро практически не влияло на их размер.
Список литературы
- Пантюхин А.В. Разработка оптимальной технологии и исследование процесса микрокапсулирования гидрофобных веществ // Вестник Воронежского государственного университета. - Сер. 2. Фармация. - 2006. - №2. - С. 338-339.
- Солодовник В.Д. Микрокапсулирование. - М: Химия, 1980. - 216 с.
Библиографическая ссылка
Степанова Э.Ф., Полковникова Ю.А., Куль И.Я. ИЗУЧЕНИЕ ВЛИЯНИЯ УСЛОВИЙ МИКРОКАПСУЛИРОВАНИЯ НА ФИЗИКО-ТЕХНОЛОГИЧЕСКИЕ ХАРАКТЕРИСТИКИ МИКРОКАПСУЛ АФОБАЗОЛА // Успехи современного естествознания. 2011. № 5. С. 75-77;URL: https://natural-sciences.ru/en/article/view?id=21464 (дата обращения: 03.05.2026).



