Scientific journal
Advances in current natural sciences
ISSN 1681-7494
"Перечень" ВАК
ИФ РИНЦ = 0,976
CONTENTS WATER-SOLUBLE ANTIOXIDANTS AND TRACE ELEMENTS IN TEA SAMPLES
В ряде работ по нутрициологии отмечены серьезные нарушения в рационе питания населения России, в первую очередь упоминается дефицит витаминов, биологически активных веществ, макро- и микроэлементов [4, 8, 12]. Указанное должно способствовать снижению общей резистентности организма к неблагоприятным факторам среды, нарушению антиоксидантной защиты, формированию иммунодефицитных состояний и развитию ряда хронических заболеваний [7]. Одной из задач, сформулированных в Концепции государственной политики в области здорового питания населения России, является ликвидация дефицита микронутриентов в пищевом рационе населения [8, 12]. Одним из инструментов оптимизации питания населения России считаются специализированные пищевые продукты и биологически активные добавки к пище [12].
Пищевые продукты растительного и животного происхождения должны в норме содержать биологически активные вещества (БАВ): отдельные незаменимые аминокислоты, экзогенные пептиды, витамины, фитонциды, полифенолы, алкалоиды, гликозиды, органические кислоты, эфирные масла и некоторые другие соединения [4, 14]. Физиологическая роль и биохимические механизмы действия для многих биологически активных веществ (БАВ) и микроэлементов к настоящему времени изучены [8, 16]. Следовательно, необходимость присутствия БАВ и микроэлементов в рационе питания приобрели научное обоснование [10, 19].
Для жителей Волго-Уральского региона достаточно сложно обеспечить полноценное питание в зимне-весенний период по многим позициям [4]. Поэтому мы обратили внимание на чай, содержащий комплекс БАВ и микроэлементов и являющийся в России самым распространенным напитком [14, 15].
Целью нашего исследования стало изучение содержания микроэлементов и низкомолекулярных антиоксидантов в чае наиболее широко распространенных в торговой сети Волго-Уральского региона сортов и марок.
Материалы и методы исследования
Чай издавна применялся в качестве профилактического и лечебного средства при целом ряде заболеваний [9, 20]. Таниды, флавоноиды и фенолкарбоновые кислоты, содержащиеся в листьях чая, проявляют выраженную антиоксидантную активностью эффективно обезвреживая свободные радикалы в тканях человека [6, 11, 16, 18].
Таксономия чайного куста неоднозначна, в связи с чем данное растение имеет целый ряд наименований: Thea sinensis L., Camellia sinensis L. (О. Ktze), Camellia thea Link. и Camellia theifera Griff.
Объектами исследования были выбраны сорта чая, пользующиеся широкой популярностью у местного населения:
Чай черный байховый пакетированный «Беседа»;
Чай зеленый пакетированный китайский «Зеленый дракон»;
Чай зеленый байховый пакетированный китайский «Акбар»;
Чай зеленый пакетированный «Ахмад»;
Чай черный байховый пакетированный «Принцесса Нури»;
Чай черный байховый гранулированный первого сорта «Золотая Чаша»;
Чай зеленый байховый листовой «Ахмад»;
Чай черный байховый крупнолистовой «Принцесса Нури» Пекое;
Чай черный байховый крупнолистовой цейлонский «Ристон»;
Чай черный байховый мелколистовой цейлонский «Ристон»;
Чай зеленый крупнолистовой развесной (Тайвань) «Сен-ча»;
Чай черный крупнолистовой «Howery orange Pekoe», «Цейлонский щеголь»;
Чай черный крупнолистовой индийский «Dilmah»;
Чай черный крупнолистовой байховый «Акбар».
В образцах чая определяли содержание химических элементов, аскорбиновой кислоты, дубильных веществ и флавоноидов. Исследования проведены на базе комплексной аналитической межкафедральной лаборатории Оренбургского государственного аграрного университета. Содержание антиоксидантов полифенольной природы определялось методом высокоэффективной жидкостной хроматографии [3]. Определение элементного состава образцов чая проводилось методом атомно-абсорбционной спектрометрии [1]. Наличие и количественное содержание аскорбиновой кислоты в исследуемых образцах чая определяли методами, принятыми в биохимии [2].
Результаты исследования и их обсуждение
Известно, что содержание минеральных веществ в листьях чая составляет около 4–5 % в заварке, и 5–6 % – в готовом напитке [7]. Минеральные вещества чая, способны переходить в водный раствор при приготовлении отваров в среднем на 50-60 % [14]. Для некоторых элементов степень их извлечения водой при приготовлении отваров достигает 90–95 %, обогащая тем самым отвар необходимыми организму человека микро- и макроэлементами [14].
Функции микроэлементов в организме растений и животных разнообразны. Роль многих биогенных элементов изучена достаточно полно, а для некоторых предполагается их участие в работе ферментов. Высокие концентрации тяжелых металлов оказывают негативное действие на клеточный метаболизм. Известно несколько молекулярных механизмов токсического действия тяжелых металлов. На первое место многие исследователи ставят образование активных форм кислорода, автоокисление и реакции Фентона (1) и Хабера-Вейса (2), (3). Указанный механизм является типичным для металлов с переменной валентностью (Cu, Fe, Mn, Co и другие) и приводит к образованию высокотоксичных гидроксильных радикалов [17]:
Мe(n-1)+ + H2О2 → Men+ + HO- + НО•. (1)
Восстановление металла обеспечивает супероксиданион:
О2•-+ Меn+ → Мe(n-1)+ + О2. (2)
Цикл Хабера-Вейса представляет собой суммарную реакцию – восстановление пероксидов посредством супероксиданиона при участии металлов с переменой валентностью:
О2•-+ H2О2 → О2 + HO- + НО•. (3)
Гидроксильный радикал (HО•), является мощным окислителем не способным к внутриклеточной миграции, так как мгновенно реагирует с биологическими молекулами. Гидроксильный радикал инициирует перекисное окисление липидов, разрушение мембран, деградацию белков, повреждение ДНК и РНК [17]. В растительных клетках нет ферментных систем, способных к нейтрализации гидроксильного радикала, что повышает роль неферментативного звена антиокислительной защиты [11].
Другим механизмом токсического действия тяжелых металлов является блокирование функциональных групп в биомолекулах (в основном сульфгидридных), эта реакция в основном характерна для таких редокс-неактивных тяжелых металлов, как кадмий и ртуть [18]. Характерно, что действие на растения повышенных концентраций редокс-неактивных металлов также нередко приводит к повышению перекисного окисления липидов [10]. Для кадмия и некоторых других металлов установлена способность ингибировать антиоксидантные ферменты, особенно глутатионредуктазу [10].
В соответствии с СанПиН 2.3.2.1078-01 «Гигиенические требования безопасности и пищевой ценности пищевых продуктов» [5, 13], в чае определены предельно допустимые уровни ртути, мышьяка, свинца и кадмия (табл. 1).
Таблица 1
Нормирование тяжелых металлов в чае
|
Токсичный элемент |
Свинец |
Кадмий |
Мышьяк |
Ртуть |
|
Допустимые уровни, мг/кг, не более |
10,0 |
1,0 |
1,0 |
0,1 |
Анализ содержание химических элементов в чайном листе указывает на значительные различия показателей для различных сортов чая (табл. 2). Данный факт можно объяснить тем, что формирование химического состава тканей растений в естественных условиях происходит при одновременном воздействии большого количества факторов внешней среды, что затрудняет изучение закономерностей поглощения химических элементов [4, 11].
Таблица 2
Содержание элементов в образцах чая
|
№ п/п |
Сорт чая |
Элементы (мг/кг) |
||||||||||||
|
Cu |
Ni |
Mn |
Zn |
Mg |
Fe |
Cr |
Co |
Cd |
Pb |
As |
Na |
Hg |
||
|
1. |
Черный пакетированный Байховый «Беседа» |
0,16 |
0,38 |
0,20 |
4,01 |
3,41 |
5,60 |
0,15 |
0,07 |
0,07 |
0,13 |
0 |
0,42 |
0 |
|
2. |
Зеленый пакетированный китайский «Зеленый дракон» |
0,10 |
0,25 |
0,11 |
4,78 |
3,01 |
0,61 |
0,17 |
0,09 |
0,08 |
0,06 |
0 |
1,61 |
0 |
|
3. |
Зеленый пакетированный байховый китайский «Акбар» |
0,13 |
0,12 |
0,12 |
5,60 |
1,00 |
4,30 |
0,10 |
0,02 |
0,01 |
0,04 |
0 |
0,20 |
0 |
|
4. |
Зеленый пакетированный Ахмад» |
0,04 |
0,08 |
0,13 |
1,23 |
0,90 |
1,72 |
0,02 |
0,04 |
0,08 |
0,08 |
0 |
0,80 |
0 |
|
5. |
Черный пакетированный байховый «Принцесса Нури» |
0,14 |
0,26 |
0,15 |
4,23 |
1,11 |
7,02 |
0,11 |
0,02 |
0,13 |
0,07 |
0 |
0,20 |
0 |
|
6. |
Черный гранулированный байховый индийский «Золотая чаша» |
0,17 |
0,15 |
0,13 |
3,42 |
0,60 |
6,32 |
0,11 |
0,02 |
0,01 |
0,05 |
0 |
0,12 |
0 |
|
7. |
Зеленый листовой байховый «Ахмад» |
0,11 |
0,24 |
0,12 |
5,50 |
2,62 |
6,75 |
0,15 |
0,09 |
0,07 |
0,07 |
0 |
1,21 |
0 |
|
8. |
Черный крупнолистовой байховый «Принцесса Нури» |
0,16 |
0,36 |
0,16 |
3,01 |
2,61 |
4,33 |
0,12 |
0,06 |
0,06 |
0,13 |
0 |
0,61 |
0 |
|
9. |
Черный крупнолистовой байховый цейлонский «Ристон» |
0,14 |
0,20 |
0,14 |
3,84 |
1,01 |
7,42 |
0,10 |
0,01 |
0,01 |
0,06 |
0 |
0,23 |
0 |
|
10. |
Черный мелколистовой байховый «Ристон» |
0,14 |
0,25 |
0,14 |
5,73 |
2,78 |
5,35 |
0,14 |
0,07 |
0,07 |
0,08 |
0 |
0,90 |
0 |
|
11. |
Зеленый крупнолистовой развесной (Тайвань) «Сен-ча» |
0,13 |
0,34 |
0,12 |
5,11 |
0,70 |
4,12 |
0,17 |
0,02 |
0,07 |
0,13 |
0 |
0,40 |
0 |
|
12. |
Черный крупнолистовой Howery orange Pekoe целонский «Цейлонский щеголь» |
0,07 |
0,05 |
0,02 |
1,01 |
0,14 |
2,01 |
0,06 |
0,06 |
0,01 |
0,01 |
0 |
0,80 |
0 |
|
13. |
Черный крупнолистовой Индийский «Dilmah» |
0,11 |
0,09 |
0,03 |
1,04 |
0,11 |
2,00 |
0,02 |
0,02 |
0,02 |
0,01 |
0 |
0,58 |
0 |
|
14. |
Черный крупнолистовой Байховый «Акбар» |
0,04 |
0,04 |
0,02 |
1,03 |
0,11 |
3,10 |
0,04 |
0,03 |
0,02 |
0,01 |
0 |
0,67 |
0 |
Содержание меди в исследуемых образцах чая колеблется от 0,04 мг/кг до 0,17 мг/кг (табл. 2, рис. 1). Зависимости содержания меди от сорта и марки чая не отмечено (рис. 1). Лидируют по содержанию меди сорт чая «Золотая Чаша» черный гранулированный и «Принцесса Нури» черный крупнолистовой. Чай черный крупнолистовой байховый «Акбар» отличается самым низким содержанием меди в ряду исследуемых образцов.
Известно, что медь входит в состав активных центров целого ряда ферментов подкласса оксидаз [11]: полифенолоксидаз, аскорбатоксидазы и других ферментов фотосинтеза [16]. В организме человека медь оказывает влияние на процессы кроветворения, работу желез внутренней секреции, воздействует на функции яичников [5], способствует усвоению витамина С. Повышенные концентрации меди оказывают цитотоксическое и генотоксическое действие, так как являются радикалинициирующим фактором. Суточная потребность в меди составляет для взрослого человека около 1-2 мг.
Содержание никеля в исследуемых образцах колебалось от 0,04 до 0,38 мг/кг (табл. 2, рис. 1) и также не зависит от сорта чая. Лидируют по содержанию никеля: чай черный байховый пакетированный «Беседа»; чай черный байховый крупнолистовой «Принцесса Нури» Пекое; чай зеленый крупнолистовой развесной (Тайвань) «Сен-ча». Самым низким содержанием никеля характеризуется чай черный крупнолистовой байховый «Акбар» (табл. 2, рис. 1).
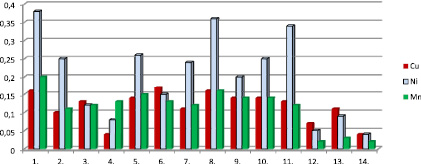
Рис. 1. Содержание микроэлементов Cu, Ni, Mn в образцах чая (мг/кг): 1 – чай черный байховый пакетированный «Беседа»; 2 – чай зеленый пакетированный китайский «Зеленый дракон»; 3 – чай зеленый байховый пакетированный китайский «Акбар»; 4 – чай зеленый пакетированный «Ахмад»; 5 – чай черный байховый пакетированный «Принцесса Нури»; 6 – чай черный байховый гранулированный первого сорта «Золотая Чаша»; 7 – чай зеленый байховый листовой «Ахмад»; 8 – чай черный байховый крупнолистовой «Принцесса Нури» Пекое; 9 – чай черный байховый крупнолистовой цейлонский «Ристон»; 10 – чай черный байховый мелколистовой цейлонский «Ристон»; 11 – чай зеленый крупнолистовой развесной (Тайвань) «Сен-ча»; 12 – чай черный крупнолистовой «Howery orange Pekoe», «Цейлонский щеголь»; 13 – чай черный крупнолистовой индийский «Dilmah»; 14 – чай черный крупнолистовой байховый «Акбар»
Никель относится микроэлементам, оказывающим неспецифическое действие на целый ряд металлоферментов, участвуя, тем самым, во многих клеточных реакциях. Никель активирует аргиназу, оксалоацетатдекарбоксилазу, трансаминазы, ускоряет окисление сульфгидридных групп в дисульфидные, ингибирует фосфатазу, стабилизирует работу трансляционного аппарата, стимулирует синтез антоцианов [5, 12]. Суточная потребность человека в никеле в зависимости от возраста, пола и веса составляет около 100-300 мкг. Повышенные концентрации никеля могут способствовать усилению перекисного окисления липидов мембран [16].
Содержание марганца в исследованных образцах чая составляет 0,02 до 0,20 мг/кг.
Марганец является биогенным элементом, входящим в состав многих металлофлавопротеидов, принимающих участие в окислительно-восстановительных процессах (фотосинтез, гликолиз, цикл трикарбоновых кислот) [16]. В растениях марганец активирует ферменты биосинтеза углеводов, стероидов, танидов, алкалоидов, аскорбиновой кислоты и витамина В2 [27], принимает участие в процессах дыхания, фотосинтеза, азотфиксации, отвечает за окисление железа. Суточная потребность человека в марганце составляет 5-10 мг. В организме человека марганец участвует в процессе остеогенеза, реакциях иммунитета, процессах кроветворения и тканевого дыхания, в реакциях общего обмена.
Максимальным содержание марганца характеризуются сорт чая «Беседа» черный пакетированный (0,38 мг/кг) и чай «Принцесса Нури» черный крупнолистовой (0,36 мг/кг). Самое низкое содержание никеля отмечено в сортах черного крупнолистового чая марок «Акбар» и «Цейлонский щеголь».
Цинк входит в состав активных центров целого ряда ферментов (в частности, ферментов синтеза полифенолов) [16, 20]. Цинк повышает устойчивость растений к засухе и гипертермии [16]. Суточная потребность человека в цинке оставляет около 10-25 мг. В организме человека цинк принимает участие в реакциях общего обмена, в остеогенезе, сахаро-инсулинового обмена, синтезе белков и нуклеиновых кислот, необходим для нормального функционирования половой системы. Для высоких концентраций цинка установлено генотоксическое действие.
Максимальное содержание цинка отмечается в черном мелколистовом байховом чае «Ристон» – 5,73 мг/кг, чуть меньшее количество цинка содержит чай черный байховый пакетированный «Принцесса Нури». Минимальное – в черном крупнолистовом «Целонский щеголь» – 1,01 мг/кг (табл. 1, рис. 2).
Магний является активатором более 300 ферментов, участвующих в процессах метаболизма [5]. Магний является s-элементом и не входит в число так называемых «тяжелых металлов». В организме человека магний влияет на работу сердечно-сосудистой системы, способствует передаче нервных импульсов, оказывает спазматическое и сосудорасширяющее действие, стимулирует перистальтику, повышает отделение желчи и способствует поддержанию кислотно-щелочного баланса. Суточная потребность в магнии – в среднем составляет около 400 мг.
Максимальное содержание магния отмечается в чае черном пакетированном «Беседа» – 3,41 мг/кг и зеленом пакетированном «Зеленый Дракон» (3,01 мг/кг). Минимальным содержанием магния (0,01 мг/кг) характеризуются сорта черный крупнолистовой «Цейлонский щеголь», черный крупнолистовой «Dilmah», черный крупнолистовой «Акбар» (табл. 1 , рис. 2).
Железо входит в состав ферментов растений, принимающих участие во многих окислительно-восстановительных реакциях. Известна роль железа в процессах фотосинтеза, тканевого дыхания, синтеза хлорофилла, метаболизме серы и азота [1, 17]. Дефицит железа в растениях приводит к хлорозу листьев и даже отмиранию молодых побегов. В организме человека железо содержится в структуре многих сложных белков: гемоглобина, миоглобина, цитохромов, пероксидаз. Суточная потребность организма взрослого человека в железе составляет от 10 до 30 миллиграммов. Дефицит железа – один из самых распространенных форм гипомикроэлементозов человека.
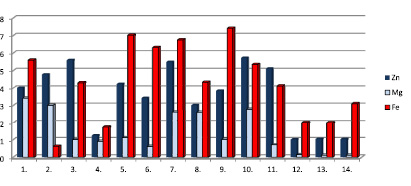
Рис. 2. Содержание микроэлементов Zn, Fe, Mg в образцах чая (мг/кг) *обозначения см. рис. 1
Максимальное содержание железа отмечено в чае черном крупнолистовом цейлонском «Ристон» – 7,42 мг/кг, черном пакетированном «Принцесса Нури» – 7,02 мг/кг и зеленом листовом «Ахмад» – 6,42 мг/кг (рис. 2). Самым низким содержанием железа характеризуется зеленый пакетированный китайский чай «Зеленый дракон» – 0,61 мг/кг (табл. 1, рис. 2).
Кобальт принимает участие в реакциях фосфорилирования, входит в состав витамина В12 и некоторых других кислородсвязывающих соединений, активирует ферменты симбиотической азотфиксации и, таким образом, связан с биосинтезом аминокислот и алкалоидов. Высказываются предположения о стимулировании этим элементом процесса оплодотворения [5]. В организме человека и животных ионы кобальта принимают участие в кроветворении, в обмене железа, углеводов, липидов [16, 17]. Есть сведения о влиянии кобальта на функцию щитовидной железы, состояние миокарда [5]. Суточная потребность взрослого человека в кобальте в среднем составляет около 0,1-0,2 мг.
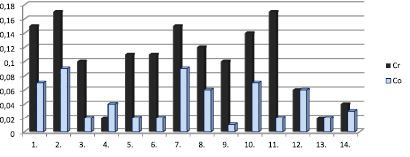
Рис. 3. Содержание микроэлементов Co, Cr в образцах чая (мг/кг) *обозначения см. рис. 1
Концентрация кобальта в исследуемых образцах чая колеблется от 0,01 мг/кг до 0,09 мг/кг (табл. 1, рис. 3). Максимальное содержание отмечено в сортах зеленого чая: зеленый пакетированный китайский «Зеленый дракон» и зеленый листовой «Ахмад». Минимальным содержанием кобальта характеризуются сорта черного чая: крупнолистовой цейлонский «Ристон» и гранулированный индийский «Золотая чаша».
Физиологическая роль хрома в растениях изучена недостаточно, предполагается его участие в фотосинтезе и продуцировании флавоноидов [5]. В организме человека хром принимает участие в регуляции обмена углеводов и является компонентом низкомолекулярного органического комплекса – фактора толерантности к глюкозе. Дефицит хрома может быть причиной диабетоподобного состояния. Суточная норма хрома в питании взрослого человека составляет в среднем 0,2-0,25 мг. Дефицит хрома приводит к задержке роста, нарушениям высшей нервной деятельности, снижению оплодотворяющей способности сперматозоидов [16].
Максимальное содержание хрома отмечается в сортах чая: зеленый пакетированный «Зеленый дракон» (0,17 мг/кг), черный пакетированный «Беседа» (0,15 мг/кг) и зеленый листовой «Ахмад» (0,15 мг/кг). Минимальное содержание хрома зафиксировано в черном крупнолистовом цейлонском чае «Ристон» (0,01 мг/кг), черном крупнолистовом индийском чае «Dilmah», зеленом крупнолистовом чае «Сен-ча» и зеленом пакетированном чае «Ахмад» (0,02 мг/кг).
В числе изучаемых нами микроэлементов не относится к числу «тяжелых металлов» s-элемент натрий. В живых организмах ионы натрия способствуют поддержанию водно-электролитного равновесия. Содержание натрия в организме растений составляет в среднем 0,02 %. Ионы натрия принимают участие в транспорте веществ через мембраны, с помощью так Na+/K+АТФазы. Максимальное содержание натрия отмечено в зеленом китайском чае в пакетиках марки «Зеленый дракон» – 1,61 мг/кг (табл. 1, рис. 4). Минимальным содержанием натрия отличается гранулированный черный чай индийского производства «Золотая чаша» (0,12 мг/кг).
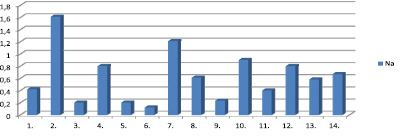
Рис. 4. Содержание Na в образцах чая (мг/кг) *обозначения см. рис. 1
Свинец и кадмий считаются основными фитотоксикантами среди анализируемых нами тяжелых металлов [5] так как не относятсяк биогенным, но отличаются высокой токсичностью и темпами накопления в окружающей среде. Свинец для растений менее токсичен, чем для человека и животных, так как его соединения малорастворимы, что снижает его биодоступность. Токсическое действие свинца связывают с тем, что ионы свинца образуют с сульфгидридными группами SH-содержащих ферментов устойчивые меркаптиды и таким образом приводят к блокированию ферментных систем. В организме человека свинец нарушает синтез гемоглобина, нуклеиновых кислот, протеидов и гормонов. Свинец поражает кроветворную, нервную и почечную системы. При накоплении в организме свинца развивается малокровие, общая слабость, туберкулез, происходит перерождение тканей, печени и почек [17].
Наибольшее содержание свинца отмечено в сортах чая «Беседа» черный байховый пакетированный, «Принцесса Нури» черный байховый крупнолистовой и сорте «Сен-ча»зеленом крупнолистовом – 0,13 мг/кг (табл. 1, рис. 5). Самое низкое содержание свинца характерно для сортов: «Цейлонский щеголь» черный крупнолистовой, «Dilmah» черный крупнолистовой, «Акбар» черный крупнолистовой (0,01 мг/кг).
Опасным для жизнедеятельности растений фитотоксикантом является кадмий, активно нарушающий работу ферментных систем [17]. Кадмий легче, чем свинец поглощается корневой системой и листьями. Кадмия способен ингибировать антиоксидантные ферменты, особенно глутатионредуктазу [16], вызывая повреждение клеточных мембран и ДНК. В гигиене питания человека кадмий считается одним из самых опасных токсикантов внешней среды. Период полувыведения кадмия составляет более 10 лет, поэтому возможно хроническое отравление этим элементом. Симптомы отравления – поражение почек и нервной системы с последующим возникновением острых костных болей, иногда нарушение функции легких.
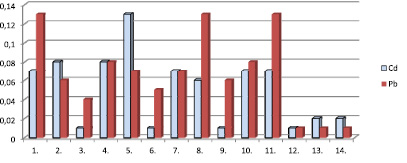
Рис. 5. Содержание токсичных элементов Pb, Cd в образцах чая (мг/кг) *обозначения см. рис. 1
Наиболее высоким содержанием кадмия отличаются сорта: чай черный пакетированный «Принцесса Нури» (0,13 мг/кг), чай зеленый байховый листовой «Ахмад» (0,08 мг/кг), чай зеленый пакетированный китайский «Зеленый дракон» (0,08 мг/кг), чай зеленый пакетированный «Ахмад» (0,08 мг/кг). Минимальное содержание кадмия (0,01 мг/кг) установлено в образцах чая «Акбар» зеленого байхового пакетированного, «Ристон» черного крупнолистового цейлонского, «Цейлонский щеголь» черного крупнолистового (табл. 1, рис. 5).
Ввиду способности большинства исследуемых микроэлементов принимать участие в окислительных процессах живых клеток нами была сделана попытка определить уровень содержания компонентов неферментативного звена антиокислительной защиты чайного листа (табл. 3). Чай, как и все высшие растения, отличается достаточно высокой толерантностью к воздействию повышенных концентраций тяжелых металлов. К механизмам устойчивости растений можно отнести задержку тяжелых металлов в подземных органах для защиты ассимилирующих и генеративных органов. А также выработку низкомолекулярных антиоксидантов (полифенолов, аскорбиновой кислоты, каротиноидов, токоферола).
Производные фенолов играют важную роль в повышении стрессоустойчивости растений и в целом ряде работ отмечается индукция синтеза полифенольных соединений под влиянием техногенных факторов [12, 19, 16]. Вещества группы полифенолов обладают способностью тормозить перекисное окисление липидов клеточных мембран, которое можно условно изобразить следующей принципиальной схемой [19]:
1) Образование R•
2) R• + O2 → RO2•
3) RO2• + RH → ROOH + R•
Фенольные соединения способны блокировать взаимодействие окисляющегося субстрата с перекисным радикалом и, следовательно, тормозить цепное окисление по схеме:
PhOH + RO2• → PhO• + ROOH.
В результате при окислении фенолят-иона образуется феноксильный радикал, который претерпевает димеризацию с образованием связей углерод-углерод или углерод-кислород:
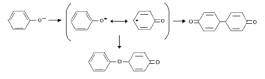
Феноксильные радикалы далее могут обезвреживаться глутатионпероксидазой по схеме:
2 PhO• + 2 HS–G → 2 PhOH + GS–SG.
Таким образом, фенольные соединения в тканях растений выполняют антиоксидантные функции.
Аскорбиновая кислота также входит в число соединений, способствующих повышению устойчивости клеток к неблагоприятным условиям, что не в последнюю очередь обусловлено ее способность проявлять антиоксидантные свойства [17]:
НО-аск-ОН + R–С•→ НО-аск-О• + R–СН;
2 НО-аск-О•+ 2 HS–G → 2 НО-аск-ОН + GS–SG.
Содержания флавоноидов в исследуемых образцах чая колеблется 2,25±0,05 мг/кг до 4,01±0,07 мг/кг (табл. 3). Четкой зависимости содержания флавоноидов от сорта чая не просматривается (табл. 3, рис. 6). В целом, сорта гранулированного чая и чая в пакетиках характеризуются несколько пониженным содержанием флавоноидов (от 2,25±0,07 до 3,80±0,04 мг/кг). Несколько выше содержание флавоноидов в крупнолистовых сортах – от 3,10±0,04 до 4,01±0,07 мг/кг.
Содержание танидов в чае варьирует от 9,00±0,02 до 16,47±0,05 мг/кг. Сорта черного и зеленого чая в нашем исследовании по содержанию танидов различий не имеют (табл. 3, рис. 6). Минимальным содержанием танидов отличаются пакетированные чаи: от 9,00±0,02 до 13,1±0,03 мг/кг.
Уровень содержания аскорбиновой кислоты в образцах чая составил от 11,0±0,2 до 20,4±0,4 мг/кг. Зависимость содержания витамина С от сорта и марки чая не прослеживалась (табл. 3, рис. 6).
Таблица 3
Содержание водорастворимых антиоксидантов в чайном листе (мг/кг)
|
№ п/п |
Сорта чая |
Содержание антиоксидантов (мг/кг) |
||
|
витамин С |
флавоноиды |
таниды |
||
|
1 |
Черный пакетированный байховый «Беседа» |
14,2±0,1 |
2,95±0,05 |
10,10±0,04 |
|
2 |
Зеленый пакетированный китайский «Зеленый дракон» |
14,4±0,3 |
3,80±0,04 |
9,00±0,02 |
|
3 |
Зеленый пакетированный байховый китайский «Акбар» |
13,0±0,2 |
3,19±0,04 |
10,70±0,03 |
|
4 |
Зеленый пакетированный Ахмад» |
13,6±0,2 |
2,84±0,05 |
11,06±0,04 |
|
5 |
Черный пакетированный байховый «Принцесса Нури» |
15,6±0,2 |
2,25±0,07 |
13,10±0,03 |
|
6 |
Черный гранулированный байховый индийский «Золотая чаша» |
20,3±0,4 |
2,86±0,05 |
15,60±0,04 |
|
7 |
Зеленый листовой байховый «Ахмад» |
19,5±0,2 |
3,09±0,04 |
15,50±0,04 |
|
8 |
Черный крупнолистовой байховый «Принцесса Нури» |
17,7±0,3 |
3,73±0,04 |
13,03±0,03 |
|
9 |
Черный крупнолистовой байховый цейлонский «Ристон» |
13,1±0,2 |
3,16±0,06 |
15,01±0,04 |
|
10 |
Черный мелколистовой байховый «Ристон» |
15,6±0,3 |
3,57±0,04 |
13,14±0,06 |
|
11 |
Зеленый крупнолистовой развесной (Тайвань) «Сен-ча» |
15,6±0,4 |
2,57±0,06 |
10,18±0,03 |
|
12 |
Черный крупнолистовой целонский «Цейлонский щеголь» |
16,7±0,3 |
3,10±0,04 |
11,36±0,04 |
|
13 |
Черный крупнолистовой индийский «Dilmah» |
11,0±0,2 |
4,01±0,07 |
14,05±0,05 |
|
14 |
Черный крупнолистовой байховый «Акбар» |
20,2±0,4 |
3,11±0,04 |
16,47±0,05 |
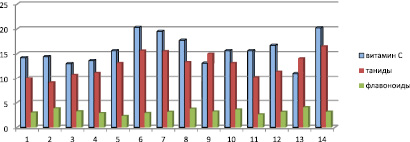
Рис. 6. Содержание витамина С, танидов и флавоноидов в образцах чая *обозначения см. рис. 1
В биогенезе полифенольных соединений и аскорбата принимает участие группа флавопротеиновых ферментов, активируемых ионами меди, марганца, цинка и молибдена [16, 19]. В условиях повышенного содержания тяжелых металлов можно предполагать индукцию синтеза низкомолекулярных антиоксидантов, что связано с мембраностабилизирующим, цитозащитным действием указанных соединений в условиях окислительного стресса. С другой стороны – хорошая обеспеченность растений микроэлементами, являющимися компонентами активных центров оксидоредуктаз (Cu, Co, Zn, Ni, Fe), может способствовать индукции синтеза антиоксидантов (флавоноидов, танидов, антоцианов, фенолкарбоновых кислот и аскорбиновой кислоты). Нами рассчитана корелляция между содержанием тринадцати эссенциальных и токсических элементов и содержанием дубильных веществ, флавоноидов и аскорбиновой кислоты (табл. 3, 4).
Таблица 4
Корелляция содержания водорастворимых антиоксидантов и микроэлементов в чайном листе (мг/кг)
|
Элементы |
Zn |
Ni |
Cr |
Cu |
Pb |
Mn |
Co |
Cd |
Fe |
Mg |
Na |
|
Корелляция содержания элемента и витамина С |
0,23 |
0,4 |
0,81 |
-0,15 |
0,46 |
-0,12 |
0,82 |
0,10 |
0,30 |
0,54 |
0,64 |
|
Корелляция содержания элементов и флавоноидов |
-0,35 |
-0,09 |
-0,02 |
-0,02 |
-0,20 |
-0,28 |
0,56 |
-0,61 |
-0,45 |
0,25 |
0,48 |
|
Корелляция содержания элементов и танидов |
-0,45 |
-0,31 |
-0,32 |
-0,01 |
-0,26 |
-0,27 |
-0,26 |
-0,33 |
0,47 |
-0,32 |
-0,22 |
В исследуемых образцах чая наблюдается выраженная положительная корелляция между содержанием в растениях чая витамина С и микроэлементов: Cr (0,81), Co (0,82), Mg (0,54), Na (0,64). Для остальных микроэлементов уровни положительной корелляции колебались от 0,23 (цинк/аскорбат) до 0,47 (железо/таниды), уровни отрицательной корреляции– от –0,22 (натрий/таниды) до –0,45 (железо/флавоноиды; цинк/таниды). Не наблюдается корелляции между содержанием в образцах чая меди и низкомолекулярными антиоксидантами. Не выявлена корреляция между содержанием в чае никеля и хрома с содержанием флавоноидов и между содержанием марганца и кадмия с витамином С. Для токсичных элементов свинца и кадмия обнаружена положительная корелляция их содержания с содержанием аскорбиновой кислоты и отрицательная с содержанием флавоноидов и танидов. Выраженная отрицательная корелляция (-0,61) характерна лишь между содержанием кадмия и флавоноидами. Для остальных элементов корелляция выражена слабо (от 0,1 до 0,46).
Выводы
1. Исследование 14-ти образцов закупленного в городе Оренбурге чая позволило определить характеристики их элементного состава. Приведенные данные свидетельствуют о том, что уровни содержания эссенциальных и токсических элементов в товарных образцах чая различаются порой на порядковую величину и не зависят от сорта и марки чая. Во всех исследуемых образцах чая содержание кадмия и свинца не превышает установленных норм (СанПиН 2.3.2.1078-01). Ртуть и мышьяк в исследуемых образцах не обнаружены.
2. Не выявлена зависимость содержания танидов, флавоноидов и витамина С от сорта чая, но в ряде случаев выражена корелляция между содержанием тяжелых металлов и вышеперечисленных антиоксидантов в чае. Содержание витамина С в образцах чая кореллирует с концентрациями хрома, кобальта и магния. Уровень содержания флавоноидов в чае показывает положительную корелляцию с уровнем содержания кобальта и отрицательную – с содержанием кадмия. Содержание танидов имеет слабую отрицательную корелляцию со всеми исследуемыми элементами, кроме железа, с которым наблюдается положительная корреляция. Концентрация меди в образцах чая не кореллирует с содержанием низкомолекулярных антиоксидантов.
3. Учитывая высокую значимость чая, как источника биологически активных веществ для населения России, следует проводить подробные исследования с целью выявления сортов чая с максимальным содержанием антиоксидантов.
Библиографическая ссылка
Немерешина О.Н., Гусев Н.Ф., Филиппова А.В. СОДЕРЖАНИЕ ВОДОРАСТВОРИМЫХ АНТИОКСИДАНТОВ И МИКРОЭЛЕМЕНТОВ В ОБРАЗЦАХ ЧАЯ // Успехи современного естествознания. 2013. № 11. С. 54-64;URL: https://natural-sciences.ru/en/article/view?id=33120 (дата обращения: 23.05.2026).



