Scientific journal
Advances in current natural sciences
ISSN 1681-7494
"Перечень" ВАК
ИФ РИНЦ = 0,976
PHYSICAL CAUSES REDISTRIBUTION OF MAIN CHEMICAL COMPONENTS IN CELLULAR SOLUTIONS
Жизнедеятельность организмов связана с поглощением природной воды. Вместе с водой в организмы поступают растворенные вещества. В организмах вещества перераспределяются. Перераспределения регистрируются химическим анализом. Полученные данные отражают процессы, происходящие в организмах.
Типичные соотношения содержаний натрия и калия в природных средах, где обитают организмы, представлены данными табл. 1:
– средние содержания натрия и калия в твердой фазе горных породах континентальной коры – преимущественно близки [4]. Также близки растворимости наиболее распространенных минералов горных пород – микроклина (KAlSi3O8) и альбита (NaAlSi3O8) [4];
– несмотря на это в водах, протекающих по горным породам, содержания натрия в 4–30 раз больше, чем калия [3].
В водах, поглощенных организмами, соотношения содержаний натрия и калия существенно изменяются (табл. 2):
Таблица 1
Различие распределений натрия и калия в твердой и жидкой фазах горных пород
|
Горные породы |
Твердая фаза ( %) |
Жидкая фаза (мг/л) |
||||
|
Состав: |
Na |
K |
Na/K |
Na |
K |
Na/K |
|
Ультраосновные |
0,5 |
0,03 |
19 |
3,2 |
0,15 |
21,3 |
|
Основные |
1,9 |
0,8 |
2,3 |
59 |
2 |
29,5 |
|
Средние |
3 |
2,3 |
1,3 |
6,3 |
1,6 |
3,9 |
|
Кислые |
2,7 |
3,3 |
0,8 |
2,4 |
0,5 |
4,8 |
|
Осадочные |
0,7 |
2,3 |
0,3 |
32,8 |
3,6 |
9,1 |
– внеклеточные растворы характеризуются соотношением 36:1. Это заметно превышает соотношения содержаний натрия и калия в природных водах;
– внутриклеточные растворы – соотношением 1:13, диаметрально противоположным соотношению натрия и калия в жидкой фазе окружающей среды.
Т.е. жизнедеятельность биологических организмов приводит к перераспределению основных химических компонентов (натрия, калия, кальция, хлора и гидрокарбонат-иона). Очевидно, что наиболее существенные изменения происходят при переходе растворов из межклеточного пространства и обратно. Границами раздела клеток и межклеточного пространства являются мембраны клеток. Именно при движении растворов через мембраны вещества перераспределяются.
Возникает вопрос: какая причина приводит к указанному перераспределению калия и натрия в клеточном растворе? Движение растворов через мембраны является механическим процессом. Без привлечения дополнительных факторов объяснение причин воздействия механического процесса (движения растворов) на содержания химических компонентов сред – невозможно.
Прохождение химических реакций, обуславливающих перераспределение веществ, возможно только в случае различия энергии клеток и межклеточного пространства. В условиях организма различие наиболее проявлено в уровнях кинетической энергии движения растворов: клетки характеризуются пониженной подвижностью растворов и пониженной энергией относительно межклеточного пространства. Одним из возможных следствий выравнивания энергий клетки и межклеточного пространства является перераспределение концентраций веществ между ними.
Само по себе различие в механической энергии не может непосредственно и значимо влиять на прохождение химических реакций. Гравитационные и магнитные эффекты живыми организмами не производятся. Это же относится радиационному излучению, а также к испарению и вымораживанию, как следствию внутренних биологических процессов. Давление и температура поддерживаются в таких узких пределах, что значимо влиять на изменение направления и скорости химических реакций непосредственно в живых организмах не могут. Объемы жидкой и твердой фаз изменяются крайне медленно по сравнению со скоростями химических реакций, происходящими в организмах.
Методом исключения устанавливается, что наиболее вероятным и значимым по происхождению и воздействию на химические процессы в организмах является электрическое поле [6].
Напряженность электрического поля оказывает непосредственное и направленное силовое воздействие на электрически заряженные частицы твердой и жидкой фаз (ионы). Соответственно происходит воздействие на обмен веществ между фазами и прохождение химических реакций.
Согласно принципу электронейтральности [6] через мембрану и ее каналы должны проходить не потоки одноименно заряженных ионов, а молекулы с суммарным электрическим зарядом равным нулю. Электрическое поле оказывает силовое воздействие на электронейтральные молекулы. Основание: ионы, составляющие молекулы, характеризуются различными уровнями энергии взаимодействия с электрическим полем. В большинстве случаев энергия воздействия электрического поля на катионы превышает энергию воздействия на анионы. В результате, электрически нейтральные молекулы движутся в сторону понижения потенциала.
Таблица 2
Внутри- и внеклеточные концентрации ионов веществ в мышечных клетках гомойотермных животных. Данные [2, 8]
|
Компонент |
В клетке |
Вне клетки |
Ионный радиус |
|
ммоль/л |
10-10м |
||
|
K+ |
155 |
4 |
1,33 |
|
Na+ |
12 |
145 |
0,98 |
|
Ca2+ |
0,00005 |
2 |
1,04 |
|
Cl- |
4 |
120 |
2,22 |
|
HCO3- |
8 |
27 |
1,58 |
|
Aнионы высокомолекулярные |
155 |
||
|
Катионы (прочие) |
5 |
||
Таблица 3
Значения энергии, сообщаемые ионам электрическим полем (относительно иона водорода)
|
Ион |
Валентность [1] |
Ионный радиус r (*10-10м) [1] |
Энергия (Аi/AH) |
|
Cl- |
– 1 |
1,72–1,81 |
0,055–0,058 |
|
НСО3- |
– 1 |
1,58 |
0,063 |
|
OH- |
– 1 |
0,35 |
0,285 |
|
Rb+ |
1 |
1,49–1,57 |
0,064–0,067 |
|
K+ |
1 |
1,33–1,46 |
0,068–0,075 |
|
Na+ |
1 |
0,95 – 0,98 |
0,102–0,105 |
|
Li+ |
1 |
0,60–0,82 |
0,122–0,167 |
|
Cs+ |
2 |
1,65–1,78 |
0,224–0,242 |
|
Ca++ |
2 |
0,99–1,06 |
0,377–0,404 |
|
H+ |
1 |
0,10 |
1 |
Для определения энергии электрического поля ионов используется известная формула [5]:
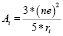
где Ai – энергия поля, создаваемого ионом, e – заряд электрона, n – валентность иона; ri – радиус иона.
Сравнение характеристик энергии воздействия электрического поля на ионы, входящие в состав жидкой фазы организмов, приведено в табл. 3.
Сравнительная характеристика силового воздействия электрического поля на различные вещества представлена в табл. 4, проиллюстрированной рисунком. Наименьшие значения энергии воздействия свойственны RbHCO3, наибольшие – CaCl2.
Содержания ионов натрия и хлора в растворах вне клеток – наибольшие (табл. 2). С учетом принципа электронейтральности близость содержаний определяет преимущественную взаимосвязь натрия и хлора. Повышенная электроположительность катионов рубидия относительно катионов лития, натрия, калия, цезия и кальция, также обуславливает преимущественное соединение рубидия с анионами хлора, имеющими наибольшую электроотрицательность. При этом калию достается преимущественная связь с менее электроотрицательным гидрокарбонат-ионом.
На основании изложенного принимается, что основным фактором, влияющим на перераспределение химических веществ, является естественное электрическое поле, возникающее при движении водных растворов относительно тканей организма.
Таблица 4
Значения энергии, сообщаемые соединениям ионов электрическим полем (относительно иона водорода)
|
Ион |
Cl- |
НСО3- |
|
Rb+ |
0,010 |
0,003 |
|
K+ |
0,016 |
0,009 |
|
Na+ |
0,048 |
0,041 |
|
Li+ |
0,088 |
0,081 |
|
Cs+ |
0,177 |
0,170 |
|
Ca++ |
0,340 |
0,333 |

Сопоставление воздействий электрического поля на главные ионные соединения внеклеточных растворов
Значения энергии, представленные в табл. 4 и на рисунке, указывают на существенное различие электрических характеристик веществ. При прочих равных условиях электрическое поле существенно слабее воздействует на ионы калия и рубидия по сравнению с воздействием на ионы натрия, лития, цезия и кальция.
Электрическое поле в биологических организмах формируется при движении водных растворов относительно тканей. Величина напряженности электрического поля (E), возникающего при движении раствора со скоростью v, удельной диэлектрической проницаемости e, удельного электрического сопротивления r через капилляр радиусом r0, выражается известной [7] формулой:
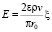 .
.
Электрический потенциал клеток больше потенциала окружающего пространства. Вектор напряженности, как силовая характеристика поля, направлен противоположно движению растворов и препятствует поступлению катионов в клеточное пространство из межклеточного. Препятствие поступлению калия и рубидия минимально по сравнению с остальными катионами. Существенно меньшая распространенность в природе рубидия, по сравнению с калием [3], объясняет преимущественность накопления в клетках соединений калия.
Таким образом, определяется физическая предпосылка перераспределения веществ между клетками и межклеточными пространством: воздействие электрического поля, образующегося при движении растворов относительно биологической ткани (в частности – мембраны клеток). Данная предпосылка может быть учтена только в случае разработки и применения принципиально новой физической модели мембранных процессов [6].
Библиографическая ссылка
Романов А.М. ФИЗИЧЕСКАЯ ПРИЧИНА ПЕРЕРАСПРЕДЕЛЕНИЯ ГЛАВНЫХ ХИМИЧЕСКИХ КОМПОНЕНТОВ В КЛЕТОЧНЫХ РАСТВОРАХ // Успехи современного естествознания. 2015. № 1-7. С. 1126-1129;URL: https://natural-sciences.ru/en/article/view?id=35021 (дата обращения: 16.05.2026).



