В связи с высоким процентом рецидивов инфекции, тяжелых осложнений, лечение хронического остеомиелита до сих пор остается одной из сложных проблем гнойной хирургии. Актуальным является изучение свойств возбудителей, обуславливающих инфекционный процесс при хроническим остеомиелите. Наиболее частыми возбудителями хронического остеомиелита являются грамположительные кокки рода Staphylococcus spp. с преобладанием штаммов S. aureus и грамотрицательные микроорганизмы: Pseudomonas aeruginosa, Escherichia coli, Enterobacter cloacae, и др. [5]. Наличие у больных в очаге воспаления грамотрицательных микроорганизмов чаще всего свидетельствует о присоединении внутрибольничной флоры [1]. Патогенность грамотрицательных микроорганизмов связывают с низкой проницаемостью их клеточной стенки, а также с наличием выраженной капсулы, синтезом фимбрилярных белков адгезии (фимбрии или пили I и III типа) [7]. Адгезивные свойства бактерий играют важную роль в развитии инфекционного процесса, обеспечивая колонизацию бактерий к различным клеткам и тканям микроорганизма. Благодаря образованию биопленок на живых и неживых поверхностях грамотрицательные бактерии колонизируют медицинские катетеры, трубки, протезы, а также долго сохраняются на аппаратуре и предметах больничного ухода [6].
Изучение персистентных свойств грамотрицательной микрофлоры у больных хроническим остеомиелитом, их адгезивных характеристик и антибиотикочувствительности к используемым в лечении инфекции препаратам, имеет большое практическое значение для предотвращения развития внутрибольничных инфекций.
Цель исследования
Изучить адгезивные характеристики и биопленкообразующую способность клинических штаммов грамотрицательных микроорганизмов, выделенных у больных хроническим остеомиелитом длинных трубчатых костей.
Материалы и методы исследования
Исследованы адгезивные характеристики 95 клинических штаммов бактерий, принадлежащих к 6 таксонам (Pseudomonas. aeruginosa – 40, Acinetobacter baumannii – 14, Klebsiella pneumoniae – 13, Escherichia coli – 12, Enterobacter cloaceae – 9, Serratia marcescens – 7), выделенных из свищей в дооперационном периоде и из очага воспаления, во время операции у больных хроническим остеомиелитом длинных трубчатых костей в период с 2013 по 2015 гг.
Идентификацию исследуемых штаммов проводили на бактериологическом анализаторе WalkAway-40 Plus («Siemens», США)1. Адгезивную активность штаммов изучали на модели эритроцитов человека А (ІI) Rh+ по методике В.И. Брилиса [2]. При оценке адгезивных свойств использовали индекс адгезивности микроорганизмов (ИАМ). Исследование проводили под световым микроскопом, учитывая в общей сложности не менее 50 эритроцитов. Микроорганизмы считали неадгезивными при ИАМ – до 1,75; низкоадгезивными – от 1,76 до 2,5; среднеадгезивными – от 2,51 до 4,0; высокоадгезивными, – ≥ 4,1.
Исследование способности выделенных штаммов формировать биопленки на поверхности 96-луночных полистироловых планшетах проводили по методу G.OʼToole и R. Kolter [9]. По уровню адсорбции красителя этанолом, измеренному в единицах оптической плотности (OD630) на фотометре ELx808 (BioTek, США) при длине волны 630 нм оценивали активность формирования биопленки. Для интерпретации полученных данных определяли способность штаммами формировать биопленки в соответствии с критериями, разработанными Stepanovic S. et al [10]: при значениях OD630 ниже 0,090 – считали, что штаммы не обладали способностью к образованию биопленки; при 0,090 < OD630 ≤ 0,180 – штаммы обладали слабой; при 0,180 < OD630 ≤ 0,360 – средней; при OD630 ˃ 0,360 – высокой способностью к образованию биопленки.
Статистическую обработку результатов проводили с помощью программного обеспечения анализа данных AtteStat, версия 13.0 [3]. Значимость различий между группами проверяли с помощью непараметрических критериев Вилкоксона и Манна-Уитни. Различия между группами наблюдений считали значимыми при Р < 0,05.
Результаты исследования и их обсуждение
Как показало исследование, все изученные клинические штаммы грамотрицательных микроорганизмов обладали адгезивными свойствами. Наибольшим адгезивным потенциалом обладали штаммы S. marcescens (ИАМ = 3,45 ± 0,24 ед.).
Cреднеадгезивные свойства проявляли 64,3 % штаммов Ac. baumannii, 57,5 % штаммов P. aeruginosa, 55,6 % штаммов E. cloaceae, 53,9 % штаммов K. pneumoniae, 16,7 % штаммов E. coli (таблица).
Адгезивная способность грамотрицательных микроорганизмов, выделенных у больных хроническим посттравматическим остеомиелитом[
|
НШ, % |
СШ, % |
ВШ, % |
ИАМ, ед. |
|
|
Pseudomonas aeruginosa (n = 40) |
22,5 |
57,5 |
20,0 |
2,74 ± 0,19 |
|
Acinetobacter baumannii (n = 14) |
7,1 |
64,3 |
28,6 |
2,92 ± 0,20 |
|
Klebsiella pneumoniae (n = 13) |
30,7 |
53,9 |
15,4 |
2,91 ± 0,18 |
|
Escherichia coli (n = 12) |
75 |
16,7 |
8,3 |
2,31 ± 0,15 |
|
Enterobacter cloaceae (n = 9) |
44,4 |
55,6 |
– |
2,42 ± 0,18 |
|
Serratia marcescens (n = 7) |
– |
66,7 |
33,3 |
3,45 ± 0,28 |
Примечание. НеАШ – неадгезивные штаммы; НАШ – низкоадгезивные штаммы; СШ – среднеадгезивные штаммы; ВАШ – высокоадгезивные штаммы; ИАМ – индекс адгезивности микроорганизмов.
По данным фотометрического анализа, все клинические изоляты P. aeruginosa, S. marcescens, Ac. baumannii обладали выраженной способностью к образованию биопленок. Наиболее активно биопленку на поверхности 96-луночного полистиролового планшета в течение 24 часов эксперимента формировали штаммы P. aeruginosa, о чем свидетельствуют средние значения OD630 (рис. 1). Штаммы E. coli обладали слабой биопленкообразующей способностью (OD630 = 0,147 ± 0,06 ед. опт пл.). OD630 штаммов Ac. baumannii, S. marcescens, E. cloaceae, K. pneumoniae была в пределах средних значений.
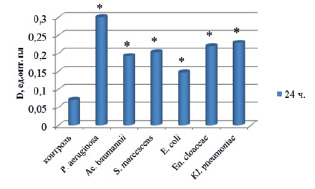
Рис. 1. Изменение средней оптической плотности красителя в лунках полистироловых планшетов, отражающей интенсивность формирования биопленки на их поверхности грамотрицательными микроорганизмами, полученными in vitro. Примечание: * Р < 0,001 – различия значимы по сравнению с контролем
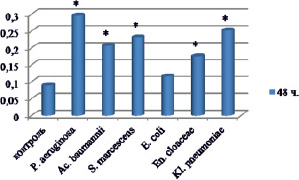
Рис. 2. Изменение средней оптической плотности красителя в лунках полистироловых планшетов, отражающей интенсивность формирования биопленки на их поверхности грамотрицательными микроорганизмами, полученными in vitro. Примечание: * Р < 0,001 – различия значимы по сравнению с контролем
Через 48 ч эксперимента активнее всего биопленку формировали штаммы P. aeruginosa, K. pneumoniae, S. marcescens, что подтверждается средними значениями OD630. Уровень биопленкообразования штаммов E. coli достоверно не отличался от контрольных значений.
Как показало исследование, грамотрицательные микроорганизмы (P. aeruginosa, K. pneumoniaе, S. marcescens, Ac. baumannii) сохраняют высокую активность формирования биопленки на поверхности 96-луночного планшета как на первые, так и на вторые сутки эксперимента. Среди энтеробактерий наибольшим сродством к биопленкообразованию обладают штаммы S. marcescens, K. pneumoniaе.
Недооценка роли грамотрицательной микрофлоры у больных хроническим остеомиелитом может привести к утяжелению течения заболевания, развитию внутрибольничной инфекции. Наибольшее клиническое значение имеет выраженная устойчивость госпитальных штаммов A. baumannii, P. aeruginosa, K. pneumoniae к большинству антибиотиков [4, 8]. Универсальным фактором патогенности грамотрицательных условно-патогенных бактерий является белково-липополисахаридный комплекс клеточной стенки – эндотоксин. Мишенью для него служат клетки почти всех органов человека, что определяет многогранность и идентичность вызванных им поражений [7].
Заключение
Из исследуемых клинических штаммов грамотрицательных микроорганизмов (P. aeruginosa, K. pneumoniae, Ac. baumannii, S. marcescens, E. cloaceae, E. coli), наилучшая способность к биопленкообразованию выявлена у неферментирующих микроорганизмов рода P. aeruginosa. Штаммы E. coli, обладая низкоадгезивными свойствами, слабо формируют биопленки. Учитывая, что количественные параметры биопленочной активности микроорганизмов могут варьироваться, перспективным для клиники будет использование методов, оценивающих активность биопленкообразования микроорганизмами и ингибиции биопленок.



