Scientific journal
Advances in current natural sciences
ISSN 1681-7494
"Перечень" ВАК
ИФ РИНЦ = 0,976
THE ALGORITHM OF COMPLEX EXAMINATION OF THE SOFT TISSUES DURING TREATMENT OF SPINAL PATIENTS WITH PRESSURE WOUNDS AND CHRONIC OSTEOMYELITIS
Цель настоящего исследования состояла в изучении информативности показателей состояния мягких тканей у спинальных больных с гнойными трофическими язвами (пролежнями), основным заболеванием которых является травматическая болезнь спинного мозга и хронический остеомиелит костей и создание диагностического алгоритма в различные периоды лечения.
Материалы и методы исследования
Обследована группа спинальных больных (n = 19) с пролежнями и остеомиелитом различной локализации. Возраст варьировал от 20 до 70 лет. У одиннадцати больных пролежни локализовались в области крестца, у пятерых – в ягодичной области, у трех – в области большого вертела бедренной кости. Соответственно у каждого из них диагностирован хронический остеомиелит крестца или большого вертела бедренной кости. Основными принципами хирургического лечения пролежневых ран являются: полноценное иссечение раны без остаточных полостей и внутренних швов; полноценный гемостаз и адекватное дренирование; ушивание без натяжений.
Проведение диагностического комплекса обследований включало следующие методики: биомеханическое тестирование тканей в участках, близлежащих к ране, локальную электротермометрию и инфракрасную термометрию в тех же участках, фотометрию. По клиническим показаниям для оценки структурных взаимоотношений мягких тканей вблизи пролежня проводили эхографию. К таким показаниям относятся трудности субъективной оценки состояния тканей после неоднократных рецидивов хронического остеомиелита крестца или других костей с последующим развитием многочисленных рубцов и спаек. Локальное измерение кожной температуры выполняли с помощью электротермометра ТПЭМ-1, используемого для измерения температуры кожи. Термочувствительный элемент выполнен в виде точечного термощупа, площадь контакта которого с исследуемым объектом 1–2 мм2. Устройство имеет две шкалы с общим диапазоном 16–42° и ценой деления 0,2°. Для инфракрасной термометрии использовали портативный термометр с дисплеем. Биомеханическое тестирование покровной ткани проводили с помощью акустического анализатора кожи – ASA (Россия и Сербия). Диапазон скоростей распространения поверхностной акустической волны (СПАВ) – 15–300 м/с. Эхографию выполняли используя ультразвуковые сканеры Logiq S-6 (General Electric Co) и Avius (Hitachi) с линейным датчиком 7–12 МГц. Применяли описательную статистику с оценкой типа статистического распределения, оценивали среднее значение, стандартную ошибку с помощью пакета прикладных программ РС при использовании программы Attestat, встроенной в Microsoft Excell (автор – разработчик И.П. Гайдышев).
Результаты исследования и их обсуждение
Биомеханическое тестирование покровных тканей в соседних с пролежнями участках показало необходимость проведения предварительной их «маркировки» и выполнения замеров минимум в четырех участках – выше, ниже, латеральнее справа и латеральнее слева раневой области (рис. 1). Важно отметить, что биомеханическое тестирование кожного покрова основано на учете анизотропных свойств ткани, поэтому тестирование следует осуществлять при четырех различных ориентациях датчика относительно продольной оси тела. В связи с этим СПАВ определяли при продольной, поперечной (90 град. относительно продольной оси тела) и диагонально – 45 и 135 град. в декартовой системе координат. Такой методический прием позволил устанавливать форму акустического поля в коже каждого участка и оценивать его видоизменение в динамике лечения. Действительно, в целом в группе обследованных больных с пролежнем крестцовой или ягодичной области происходит видоизменение конфигурации огибающих кривых векторов скоростей звука в коже (акустических полей). После проведенного комплексного лечения (консервативного и оперативного) в результате перераспределения напряжений в коже форма акустических полей видоизменяется. Это проявляется при тестировании участков кожи вблизи раны как в крестцовой области, так и в ягодичной (рис. 1, 2). Например, переход из эллиптической формы акустического поля с большей горизонтальной осью в округлую конфигурацию к 37 дням после операции, а к 95 дням – трансформация в косо-диагональную эллиптическую форму. Возможно значительное повышение СПАВ в коже (рис. 2) с сохранением формы акустического поля, что, по-видимому, связано с анатомическими особенностями исследуемой области и отражает развитие достаточно высокой степени натяжения в покровной ткани, что коррелирует с клинической оценкой текущего состояния тканей.
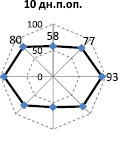
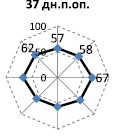
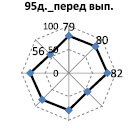
10 дней после операции
37 дней после операции
95 дней после оперативного лечения
Рис. 1. Пациент Ж., 27 лет. Диагноз: травматическая болезнь спинного мозга (ТБСМ), подострый период. Компрессионно-оскольчатые переломы D12-L1 с компрессией спинного мозга. Нижний грубый вялый парапарез. Нарушение функции тазовых органов. Пролежень крестцовой области. Пролежни обеих стоп. Хронический остеомиелит крестца, костей обоих голеностопных суставов, свищевая форма. Несросшиеся переломы костей обеих голеней. Использован критерий – форма акустических полей по результатам биомеханического тестирования кожи крестцовой области. Исследуемый участок – латеральнее справа от раны. Пояснения в тексте
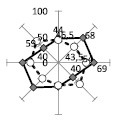
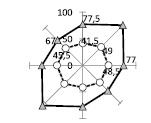
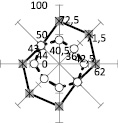
До операции 5 дней после операции 20 дней после операции
Рис. 2. Больная А., 27 лет. Диагноз: ТБСМС, поздний период. Последствия перелома L1 позвонка. Нижняя спастическая параплегия. Нарушение функции тазовых органов. Пролежень правой вертельной области. Хронический посттравматический остеомиелит правой бедренной кости. Тестирование кожи в вертельной области, участок выше раны. Сплошная кривая – показатель СПАВ в коже пораженной ягодичной области, пунктирная кривая – параметры СПАВ в коже интактной области. Пояснения в тексте
В последующем происходит снижение СПАВ и площадь акустического поля в коже также снижается, косвенно указывая на снижение напряжений в соседних с раной участках кожного покрова. Следовательно, указанное изменение конфигурации акустических полей и динамика величины СПАВ косвенно свидетельствует о перераспределении напряжений в кожном покрове и отражает степень натяжения ткани в различных направлениях относительно продольной оси тела.
У части больных (n = 4) после неоднократных рецидивов пролежней и хронического остеомиелита седалищных костей проводилась эхография мягких тканей в ягодичных областях (n = 4) для уточнения толщины тканей, особенностей структуры (четкая или размытая граница между различными слоями тканей), уровень эхогенности. На пораженной стороне у обследованных пациентов выявлены эхопризнаки отека тканей (невозможность определения границы между кожей, гиподермой, мышцами). Рисунок ягодичных мышц при эхографии был атипичным – размытым, отсутствовала контрактильная реакция при произвольном мышечном напряжении. Следовательно, информативность эхопараметров мягких тканей может определяться тяжестью общих патологических изменений при травматической болезни спинного мозга на уровне различных систем организма. Кроме того, у таких пациентов в подавляющем числе случаев существенно снижается регенерационный потенциал. Поэтому унификация критериев эхографии мягких тканей с учетом выше сказанного нецелесообразна, а параметры эхографии могут лишь уточнить структурные взаимоотношения мягких тканей, особенно при неоднократных рецидивах как самого остеомиелитического процесса, так и развития пролежней. Хотя применение эхографии имеет ограниченный характер, предлагаемая объективизация оценки результатов лечения мягких тканей может внести определенный вклад в изучение реабилитационного процесса у данной категории пациентов.
Установлено, что в группе пациентов с хроническим остеомиелитом и пролежнями в крестцовой области показатели обоих видов локальной термометрии во всех тестируемых соседних с пролежнем участках (латеральнее, выше и ниже раны) после оперативного лечения имели тенденцию к снижению относительно предоперационных значений (рис. 3). Результаты локальной термометрии и инфракрасной термометрии согласуются между собой.
Ранее было обнаружено, что биомеханические свойства кожного покрова (показатель растяжимости) на разных участках тела у пациентов с травматической болезнью спинного мозга разного возраста ниже, чем у здоровых людей [2]. Вместе с тем методическая база контроля процесса лечения пролежней остается недостаточно развитой. Мало изученной остается прижизненная оценка ряда объективных параметров мягких тканей в типичных при развитии пролежней областях тела. Необходим количественный анализ параметров, характеризующих состояние мягких тканей соседних с пролежнями, с целью выявления критериев прогнозирования развития пролежневых ран в группах риска. В группу риска входят пациенты с травматической болезнью спинного мозга (после перенесенных травм позвоночника; больные с различными заболеваниями, вынужденные быть длительно прикованными к постели, после тяжелых оперативных вмешательств и др.). Так, ряд авторов пришли к выводу, что повышение температуры кожи в крестцовой области на 1,2 градуса позволяет рассматривать в качестве предиктора возможного развития пролежня в указанной области в течение 24–96 часов [3]. С другой стороны, продолжается поиск решения сложной проблемы лечения трофических язв [5]. Изучаются факторы, влияющие на развитие и заживление пролежней у лиц, прикованных к постели в результате спинномозговой травмы, или у пациентов престарелого возраста [6, 7]. Большое значение придается своевременной правильной систематической профилактике развития пролежней у различного контингента пациентов. По данным статистики, частота возникновения пролежней у госпитализированных больных в США в среднем составляет от 2,7 до 29 %, достигая 40–60 % у пациентов, перенесших позвоночно-спинномозговую травму, а стоимость лечения пролежневой раны достигает $2000–40000. Затраты на лечение пролежней в госпитальном секторе в США составляют $11 млрд в год. Ежегодные затраты на лечение пролежней в Национальной службе здравоохранения Великобритании оцениваются в £1,4–2,1 млрд. Пролежни являются значительным бременем для систем здравоохранения по всему миру.

До оперативного лечения

После оперативного лечения
Рис. 3. Динамика показателей термометрии в группе пациентов с хроническим остеомиелитом крестца (n = 11). Обозначения – на верхнем рисунке диаграммы с точечной заливкой – показатели электротермометрии, столбики с косой штриховкой – параметры инфракрасной термометрии. На нижнем рисунке – столбики в косую черту – данные электротермометрии, точечной заливкой обозначены показатели инфракрасной термометрии
У 26 % больных с незаживающими пролежнями развивается остеомиелит, а риск летального исхода возрастает в 4–5 раз. Это свидетельствует о необходимости приложения серьезных усилий – лечебно-профилактических, организационных, образовательных, финансовых и интеграцию усилий специалистов различного профиля (врачей общей практики, нейрохирургов, гериатров, травматологов-ортопедов, реабилитологов) для решения проблемы профилактики и лечения трофических язв, нередко осложняющихся хроническим остеомиелитом. В этом аспекте остается актуальным вопрос использования объективных критериев при изучении динамики ряда параметров в процессе лечения пролежней в зависимости от сложного комплекса факторов, определяющих его успех. Ряд авторов предложили проводить мониторинг заживления ран используя оптическую когерентную томографию – оptical coherence tomography (ОСТ) [1], которая позволяет обнаружить частичную потерю эпидермиса, сужение сосудов, и нарушение эпителизации. Были достигнуты сопоставимые результаты между гистологическими данными и показателями оптической когерентной томографии [1].
Алгоритм комплексного исследования мягких тканей, близлежащих к пролежневой ране, у спинальных больных с хроническим остеомиелитом
|
№ п/п |
Методика исследования |
Исследуемый участок |
|
1 |
Биомеханическое тестирование покровных тканей |
На 3–4 см выше, ниже, латеральнее справа, латеральнее слева от раны |
|
2 |
Электротермометрия |
На 3–4 см выше, ниже, латеральнее справа, латеральнее слева от раны |
|
3 |
Инфракрасная термометрия |
На 3–4 см выше, ниже, латеральнее справа, латеральнее слева от раны |
|
4 |
Эхография** (ограниченное применение) |
Вблизи пролежня в зависимости от доступа для размещения датчика |
|
5 |
Фотометрия |
Пролежневая рана |
Примечание. **эхография проводится ограниченно (по клиническим показаниям) для уточнения структурных взаимоотношений мягких тканей при наличии обширных рубцовых изменений, неоднократных рецидивах развития пролежня и обострения хронического остеомиелита.
Заключение
Апробация предлагаемого нами алгоритма и результаты диагностического обследования мягких тканей указанной группы пациентов показали целесообразность его дальнейшего использования в клинике гнойной остеологии. Особенностью БТ и локальной термометрии является необходимость проведения замеров в условиях перевязочного кабинета, когда достигается хороший доступ к соседним с пролежневой раной участкам. Противопоказанием для проведения БТ кожи и эхографии тканей у больных с трофическими язвами (пролежнями) является наличие обильного отделяемого из раны, хотя этот симптом может быть временным и нивелируется по мере лечения. Определены этапы проведения мониторинга состояния мягких тканей у пациентов с указанной патологией. Они включают следующие периоды:
1 – до начала лечения в стационарных условиях;
2 – перед оперативным вмешательством;
3 – через 4–5 дней после операции;
5 – через 3–5 дней после снятия послеоперационных швов;
6 – при завершении лечебных мероприятий в клинике.
Одним из распространенных способов лечения пролежневой раны является ее ушивание, однако не исключается риск избыточного натяжения краев раны, что может привести к краевому некрозу.
Таким образом, предложен алгоритм комплексного исследования состояния мягких тканей у пациентов с последствиями позвоночно-спинномозговой травмы, наличием пролежневых ран и хроническим остеомиелитом (таблица).
Использованный в нашем исследовании параметр биомеханического тестирования кожи – СПАВ – свидетельствует о том, что критерий «форма акустического поля» является количественной и качественной характеристикой характера и степени натяжения ткани. Его информативность состоит в косвенной оценке пространственного распределения напряжений в кожном покрове, т.е. его анизотропного биомеханического состояния, которое определяется локализацией пролежневой раны, индивидуальными анатомическими особенностями тканей, возрастом, видами применяемых методов лечения раны (консервативное или оперативное), давностью заболевания, наличием рубцовых изменений. Механо-акустическое тестирование кожи позволяет косвенно оценивать степень натяжения близлежащей к ране кожи. Анализ динамики показателей БТ дает дополнительную информацию для внесения коррекции в тактику лечения. С учетом данных литературы для углубленного анализа получаемых показателей и практического их использования целесообразно учитывать ряд параметров. Они включают возраст пациента, наличие структурных особенностей кожи (ее истончение, отечность и др.), массу тела, нагрузку на кожу в виде трения или сдвиговой нагрузки и др. Перечисленные факторы составляют неполную группу признаков, которые необходимо принимать во внимание при прогнозировании риска развития пролежней и возможного характера их заживления на этапах лечения [4].
Библиографическая ссылка
Гребенюк Л.А., Мухтяев С.В. АЛГОРИТМ КОМПЛЕКСНОГО ОБСЛЕДОВАНИЯ МЯГКИХ ТКАНЕЙ ПРИ ЛЕЧЕНИИ СПИНАЛЬНЫХ БОЛЬНЫХ С ПРОЛЕЖНЕВЫМИ РАНАМИ И ХРОНИЧЕСКИМ ОСТЕОМИЕЛИТОМ // Успехи современного естествознания. 2015. № 9-2. С. 198-203;URL: https://natural-sciences.ru/en/article/view?id=35559 (дата обращения: 12.05.2026).



