Scientific journal
Advances in current natural sciences
ISSN 1681-7494
"Перечень" ВАК
ИФ РИНЦ = 0,976
DEVICE AND MICROINSTRUMENT FOR HOLDING STITCHES FOR SMALL-DIAMETER ARTERIES ANASTOMOSIS, AND THEIR EXPERIMENTAL TESTING
Микрохирургия последнего десятилетия характеризуется техническими усовершенствованиями: развитием телемикрохирургии и роботизированной ассистенции, а также супермикрохирургии. Робот-телеманипулятор позволяет контролировать тремор рук хирурга и эргономику движений, что успешно используется при обучении [6], однако его внедрение в клиническую микрососудистую хирургию проблематично. По сравнению с операциями без участия роботов при роботизированной ассистенции время выполнения микрососудистого анастомоза увеличивается вдвое; иглодержатели роботов позволяют манипулировать с шовным материалом до 10-0, но не тоньше. Техника сшивания сосудов с наружным диаметром менее 0,8 мм, получившая название «супермикрохирургия» [5], требует не только специальных навыков, но и более прецизионного оснащения: микроскопа с большим увеличением и фокусным расстоянием, шовного материала калибра 12-0 и ультратонких пинцетов с диаметром рабочей части 0,1 мм [8]. Практическая значимость прецизионной техники доказана для пластической [5] и реплантационной [4] хирургии.
По мнению некоторых авторов, выполнение супермикрохирургического анастомоза возможно обычными микрохирургическими инструментами с применением интраваскулярного стентирования [9]. В качестве стента используют фрагмент нейлоновой монофиламентной нити, который вводят в просветы концов пересечённого сосуда, что позволяет предотвратить их слипание, исключить повреждение иглой противолежащей стенки сосуда при проведении швов, а также равномерно распределить швы. По данным C. Bossut, O. Barbier [2], этот приём облегчает задачу сшивания субмиллиметровых сосудов для молодых хирургов, однако манипуляции по установке и удалению стента создают риск тромбогенных повреждений интимы.
Таким образом, анализ литературы свидетельствует, что хотя супермикрохирургия стала реальностью клинической практики и обеспечена индустрией развитых стран, остаются актуальными разработки инструментов и приспособлений, облегчающих сшивание тонких сосудов и сочетающих атравматичность, прецизионность и простоту использования.
Цель исследования – разработка оригинального микроинструмента и приспособления для проведения швов, экспериментальная оценка целесообразности их применения при анастомозировании сосудов малого диаметра.
Материалы и методы исследования
Разработано приспособление – силиконовый микростент с заострёнными концами (рис. 1, а), а также микроинструмент – зонд с максимальным диаметром рабочей части 0,3 мм, имеющий прорезь под иглу (рис. 1, б). На первом этапе исследования проведена апробация приспособления и инструмента на неживой биологической модели, рекомендованной для тренировки супермикрохирургических анастомозов – охлаждённом бедре цыплёнка [3]. Апробированы приёмы введения разработанного приспособления и инструмента в просвет малых сосудов и выполнено 24 анастомоза артерий диаметром от 0,5 до 0,8 мм – ветвей a. ischiadica первого и второго порядков. Диаметры артерий измеряли миллиметровой шкалой, тарированными клипсами фирмы Aesculap с ценой деления шкалы 0,5 мм и тарированной с помощью объект-микрометра картонной шкалы с ценой деления 0,125 мм.
При выделении и анастомозировании сосудов применялся бинокулярный стереомикроскоп МБС-10 (Россия) – увеличения 8, 16 и 32х, а также инструменты фирмы Aesculap (Германия). Для механической дилатации сосудов использовались ультратонкие пинцеты с диаметром рабочей части 0,1 мм, полученные методом тонкой ручной шлифовки концов стандартных микрохирургических пинцетов. В контрольной группе (n = 12) ультратонкие пинцеты применялись также и при проведении швов. Швы выполнены нитями 10/0 и 11/0 на круглых атравматических иглах диаметром 50 и 75 мкм фирмы Ethicon.
После перерезки артерий охлаждённого бедра цыплёнка концы их в большинстве случаев значительно сокращаются, поэтому их фиксировали и сближали сдвоенной клипсой-аппроксиматором. Для визуализации и дилатации спавшегося просвета артерии её концы орошали тёплым физиологическим раствором, осторожно отодвигали адвентицию от торцов, при необходимости её резецировали, а затем дилатировали просвет тонким пинцетом. После этого накладывали два установочных шва на расстоянии около 120 градусов друг от друга, которые завязывали инструментальными двойным и одинарным узлами. Затем, используя установочные швы для натяжения стенки сосуда и разворотов анастомоза, накладывали от 4 до 7 дополнительных отдельных узловых швов, каждый из которых завязывали двумя одинарными узлами. При проведении швов использовали увеличения микроскопа 16х и 32х, что позволяло визуально контролировать прохождение иглы сквозь просвечивающую стенку сосуда.
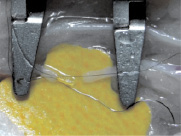
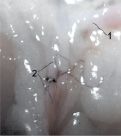
В опытной группе (n = 12) при анастомозировании артерий диаметром 0,6 мм и более для проведения установочных швов через проксимальный конец артерии применяли разработанный металлический зонд. Фиксируя адвентицию проксимального конца сосуда вколом иглы, зонд вводили в дилатированный просвет. Сквозной вкол и выкол иглы проводили, направляя иглу по прорези зонда. Для анастомозирования более тонких сосудов использовали силиконовый гемистент, который вводили в проксимальный конец пересечённой артерии примерно на половину его длины. Удерживая свободный конец стента пинцетом и создавая встречное противодавление игле, через стенку проксимального конца артерии проводили два установочных шва (рис. 2, а). Затем гемистент удаляли и проводили иглы через симметричные точки дистального конца артерии. Остальные швы выполнены аналогично контролю (рис. 2, б).


а б
Рис. 1. Интраваскулярные стенты (а) и зонд с прорезью под иглу (б) для анастомозирования сосудов малого диаметра: 1 – силиконовый стент; 2 –монофиламентный стент
а б в
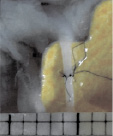
Рис. 2. Этапы анастомозирования ветви a. ischiadica охлаждённого бедра цыплёнка: a – стентирование проксимального отрезка и проведение установочных швов; б – окончание анастомоза; в – контроль заполнения a. ischiadica (1) и её пересечённой и анастомозированной ветви (2) окрашенной жидкостью. Цена деления шкалы 1 мм
Проходимость анастомозов тестировали инъекцией окрашенной жидкости в a. ischiadicae (рис. 2, в) и последующей диссекцией анастомоза. При диссекции оценено качество проведения швов: наличие или отсутствие признаков их прорезывания, повреждений иглой противолежащей стенки сосуда, а также равномерность длины стежков и расстояний между ними.
На втором этапе исследования проведена апробация разработанного стента и микрозонда на 6 живых белых крысах. Животных содержали в виварии, оперативные вмешательства и эвтаназию осуществляли в соответствии с требованиями Министерства здравоохранения Российской Федерации к работе экспериментально-биологических клиник, а также «Европейской конвенции по защите позвоночных животных, используемых для экспериментальных и других научных целей». Операции (перерезка и анастомозирование бедренной артерии диаметром от 0,5 до 0,7 мм) выполнены под общей анестезией, которая достигалась внутримышечным введением гидрохлорида ксилазина (0,8 mg/100 g) и тилетамина/золазепама (0,4 mg/100 g), в асептических условиях с применением операционного микроскопа Opton. В течение 15 минут после окончания анастомоза оценивали выраженность горизонтальной пульсации артерии и результаты двухпинцетной пробы. Через 4 недели после операции животных наркотизировали повторно, проводили ревизионную операцию и биомикроскопию зоны анастомоза, оценивая выраженность пульсации артерии и её ветвей. Визуальный контроль проходимости анастомозов дополняли определением объёмной скорости кровотока ультразвуковым допплеровским флоуметром T101 (Transonic Systems Inc., США).
Статистическую обработку количественных данных проводили с использованием критериев Манна – Уитни и Барнарда, значения которых получали в программе Attestat (разработчик – И.П. Гайдышев).
Результаты исследования и их обсуждение
Выявлено преимущество разработанного силиконового стента по сравнению с известным монофиламентным нейлоновым [9]. Прямоугольный в сечении упруго-эластический силиконовый стент гораздо легче удерживать пинцетом и вводить в просвет сосуда.
Металлический зонд по сравнению с наиболее близким зарубежным аналогом [1] также показал преимущества при введении в просвет сосуда в силу меньшего диаметра (0,3, а не 0,5–1,5 мм); кроме того, в отличие от аналога он имел сквозную прорезь под иглу, что обеспечивало более точную ротацию последней при проведении через стенку сосуда.
Введение силиконового стента или металлического зонда левой рукой в просвет сосуда навстречу вколу иглы при проведении первого шва требовало более сложного навыка, чем противодавление введённым в просвет тонким пинцетом, однако при выработке такого навыка разработанные микроинструмент и приспособление облегчали проведение установочных швов. Более быстрое и точное их выполнение в среднем сокращало время выполнения анастомоза. В опытной группе оно варьировало от 12 до 36 минут и составило в среднем 24,8 ± 2,3 минуты, а в контроле – от 18 до 42 минут, в среднем 30,4 ± 2,3 минуты (p < 0,05).
Все анастомозы оценены как проходимые. В контрольной группе отмечено три случая прорезывания установочных швов и два случая повреждения иглой противолежащей стенки сосуда. В одном случае прорезывание было полным и потребовало перепроведения шва, в двух других оно было замечено только при диссекции анастомоза и микроскопии лигатурных каналов. В опытной группе технических ошибок не выявлено. При сравнении частоты ошибок по критерию Барнарда p < 0,01.
Анастомозы бедренной артерии на живых крысах, выполненные с применением разработанного приспособления и инструмента, были проходимыми не только в ближайшие 15 минут после операции, но и через месяц после неё. Объёмная скорость кровотока в анастомозированных артериях во всех шести опытах была сопоставима с контрлатеральной стороной и составляла от 8 до 12 мл/мин.
Для восстановления и сохранения кровотока в артериях малого диаметра требуется щадящая и прецизионная техника, поскольку уже при выделении таких сосудов из окружающих тканей происходит интенсивное слущивание эндотелиальных клеток и формирование тромбоцитарных агрегатов [7]. Внедрение супермикрохирургии в клиническую практику, отмеченное в последние годы, вызывает необходимость экспериментальных разработок инструментов и приспособлений, не только облегчающих выполнение микрососудистого анастомоза, но и улучшающих его качество и тем самым способствующих сохранению кровотока в ближайшем и отдалённом периодах. Выполненное исследование показало, что решение этой задачи достигается щадящей инструментацией просвета артерии на этапе проведения установочных швов и исключением её при выполнении последующих швов. Обычный для микрохирургической практики приём – коррекция прохождения иглы при её проведении снаружи в просвет сосуда противодавлением браншами тонкого пинцета, введёнными в просвет навстречу игле, – не гарантирует защиты от повреждения остриём иглы противолежащей стенки сосуда. Кроме того в некоторых случаях браншами тонкого пинцета создаётся большое удельное давление на стенку сосуда и риск её повреждения. И, наконец, при применении пинцета не всегда удаётся точная ротация иглы соответственно её кривизне. Именно поэтому в контрольной группе опытов в пяти случаях из 12 отмечены технические ошибки, выявленные при микроскопии анастомозов после их диссекции. При испытании на неживой модели они не повлияли на проходимость (заполнение анастомоза жидкостью), но в живом организме такие дефекты могут быть предпосылкой тромбоза в ближайшем послеоперационном периоде или стенотического ремоделирования сосуда в отдалённом. Результаты опытной группы показали, что альтернативные инструмент и приспособление не только облегчают задачу выполнения установочных швов, но и позволяют исключить технические ошибки, отмеченные в контроле. Атравматично и прецизионно выполненные установочные швы, несомненно, определяют качество анастомоза в целом, что подтвердилось в испытании как на неживой, так и на живой биологической модели.
Использование неживой модели не только для отработки навыков микрохирургии, но и апробации новых инструментов и приспособлений представляется целесообразным. Такой подход позволяет существенно снизить расходы на исследование, а также исключает контаминацию человека микробной флорой лабораторных животных. Модель охлаждённого бедра цыплёнка адекватна задачам экспериментальной супермикрохирургии в силу анатомических особенностей сосудистого русла [10] – наличием большого количества артерий с наружным диаметров 0,8 мм и менее.
Заключение
Применение тонкого зонда с проточкой под иглу либо силиконового гемистента на этапе проведения установочных швов через проксимальный отрезок артерии малого диаметра позволяет сократить время выполнения анастомоза и обеспечить эффективное восстановление кровотока в ближайшем и отдалённом периодах после операции. Разработанные инструмент и приспособление могут быть изготовлены самостоятельно, просты и атравматичны в использовании.
Библиографическая ссылка
Щудло Н.А., Щудло М.М., Cбродова Л.И., Щурова Е.Н. ПРИСПОСОБЛЕНИЕ И МИКРОИНСТРУМЕНТ ДЛЯ ПРОВЕДЕНИЯ ШВОВ ПРИ АНАСТОМОЗИРОВАНИИ АРТЕРИЙ МАЛОГО ДИАМЕТРА И ИХ ЭКСПЕРИМЕНТАЛЬНАЯ АПРОБАЦИЯ // Успехи современного естествознания. 2015. № 9-2. С. 260-263;URL: https://natural-sciences.ru/en/article/view?id=35573 (дата обращения: 12.05.2026).



