Scientific journal
Advances in current natural sciences
ISSN 1681-7494
"Перечень" ВАК
ИФ РИНЦ = 0,976
STUDY OF THE REGULARITIES OF EXTRACTION OF ZINC FROM AQUEOUSSOLUTIONS IN THE FIELD OF GALVANIC COUPLES OF IRON-CARBON
Технологический процесс разработки и переработки рудных месторождений сопровождается образованием значительного количества техногенных вод. Учитывая объемы гидротехногенных образований, а также высокие концентрации ионов тяжелых и цветных металлов, данные воды можно классифицировать как техногенное гидроминеральное сырье, переработка которого позволит более полно использовать природные ресурсы. Кроме того, ужесточение экологической политики государства выводит на ведущие позиции решение вопросов по переработке техногенных образований с целью снижения концентраций канцерогенных веществ до норм ПДК и организации цикла оборотного водоснабжения на предприятиях [5–9, 14].
Кислые подотвальные воды горных предприятий Южного Урала по концентрации ионов цинка (до 900 мг/дм3), объемам (до 2000 м3/сут.) и возможности их переработки можно отнести к категории «жидких» техногенных цинксодержащих ресурсов. В настоящее время эффективные технологии, позволяющие селективно извлекать цинк в виде товарного продукта, отсутствуют. В современных условиях целесообразно получение рациональных продуктов, утилизируемых в металлургическом переделе, с массовой долей цинка 6–7 %, в соответствии с нижним пределом, содержащим для рентабельной переработки в металлургическом переделе. Рациональным продуктом является продукт с содержанием ценного компонента, в осадке позволяющего переработать в металлургическом переделе. Поэтому разработка технологии, позволяющей в комплексе селективно извлечь цинк и другие ценные металлы из кислых рудничных вод с одновременным снижением их концентраций в стоке до норм ПДК, является актуальной научно-практической задачей [2, 12, 13, 14].
Наиболее перспективно для переработки цинксодержащих техногенных вод использовать метод гальванокоагуляции. Эффективность данного метода обусловлена простотой аппаратурного оформления, дешевизной используемых материалов, а также возможностью селективного извлечения ионов цинка из высокоминерализованных кислых растворов [3, 4, 10, 11].
Метод гальванокоагуляции основан на использовании эффекта короткозамкнутых контактов гальванического элемента, образуемого гальванопарами «железо ? кокс» и «алюминий ? кокс», помещаемыми в очищаемый раствор. За счет разности электрохимических потенциалов железо анодно поляризуется и переходит в раствор [10, 11]. Метод гальванокоагуляции эффективен в результате действия пяти механизмов: катодного осаждения ионов металлов, образования ферритов, клатратов, коагуляции и сорбции примесей на свежеобразованных микрокристаллах оксидных форм железа. Железосодержащий осадок, образующийся в процессе очистки, может использоваться как вторичное сырье. Метод гальванокоагуляции применяется для вод с различным диапазоном концентраций, рН, солесодержания.
Изучение закономерностей извлечения цинка из однокомпонентных растворов проводилось в несколько этапов. На первом этапе исследований изучены кинетические закономерности извлечения цинка из однокомпонентных растворов с концентрацией от 250 до 750 мг/дм3. Результаты исследований представлены на рис. 1.
Анализ полученных результатов показал, что при 10-минутной обработке растворов происходит снижение концентрации в сливе гальванокоагулятора на 10–20 %. При этом отмечено, что чем меньше исходная концентрация, тем более эффективно происходит удаление цинка из раствора за один и тот же промежуток времени.
Для концентрации 500 мг/дм3 изучена кинетика извлечения в промежутке времени до трех минут. В сливе одновременно с цинком определяли концентрацию железа. Отмечено, что рост концентрации железа не является эквивалентным снижению концентрации цинка, а при увеличении времени обработки до одной минуты происходит одновременное снижение концентраций металлов, что видимо, является следствием связывания их в ферриты.
Это предположение подтверждается ростом удельного веса ферритного осадка (рис. 2) при увеличении времени обработки раствора.
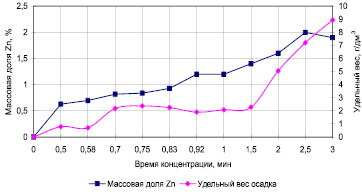
Рис. 2. Влияние времени обработки на удельный выход и массовую долю цинка в осадке
За одну минуту обработки при содержании цинка в растворе 500 мг/дм3 выход ферритного осадка составил 2,0 г/дм3, а за три минуты увеличился до 8,6 г/дм3. Рост массовой доли цинка в осадке наблюдается в течение 2,5 минут и затем стабилизируется в области 1,7–1,9 %.
Эту закономерность нельзя объяснить тем, что в растворе содержится повышенное количество железа в растворенной форме, которое, с увеличением времени очистки, как в первом, так и во втором случае, окисляясь кислородом воздуха, переходит в гидратную форму и выпадает в осадок. В этом случае происходило бы разубоживание осадка по цинку. Вероятнее всего за промежуток времени 2,5 минуты в системе достигается некое равновесие между переводом в жидкую фазу железа вследствие растворения анода и связывания его в ферриты совместно с цинком.
Результаты исследования влияния температуры раствора на показатели извлечения цинка показали, что отклонение температуры раствора от 20 градусов в ту или иную сторону приводит к повышению концентрации железа в сливе гальванокоагулятора. Концентрация цинка снижается до температуры 30–40 градусов, а затем начинает возрастать, что является следствием повышения растворимости образующихся цинксодержащих соединений при повышении температуры.
При анализе влияния рН на показатели гальванокоагуляционного извлечения ионов цинка установлено, что с увеличением исходного значения рН раствора с 5,2 до 6,5 возрастает извлечение ионов цинка с 75 до 87 %, массовая доля цинка увеличивается с 5,5 до 6,78 % и наблюдаются максимальные значения удельного выхода осадка и массовой доли цинка. Максимальное извлечение ионов цинка характерно для области рН более 8,5. Это объясняется протеканием процесса кислотно-основного осаждения ионов цинка в виде гидроксида Zn(OH)2. Следовательно, для гальванокоагуляционного извлечения цинка оптимальная область рН обрабатываемых растворов от 5,2 до 6,5.
Сравнительный анализ скорости перевода цинка и железа в осадок (рис. 3) позволил утверждать, что в предварительно аэрированном растворе происходит интенсификация процесса растворения и окисления анодного железа, однако скорость перехода в осадок железа повышается незначительно (от 0,55 до 0,57 мг/с). Скорость перехода цинка в ферритный осадок повышается после предварительной аэрации более значимо с 0,50… до 0,59 мг/с.
Повышение скорости перехода цинка в осадок в случае предварительной аэрации растворов подтверждено изучением кинетических закономерностей – изменения остаточной концентрации цинка в процессе гальванокоагуляции при обработке раствора сульфата цинка различных концентраций. Установлено, что скорость снижения остаточной концентрации цинка в растворе заметно возрастает после аэрации в первые четыре минуты контакта раствора с гальванопарой.
Изучение фазового состава образующейся дисперсной фазы проводили рентгеноструктурным методом.
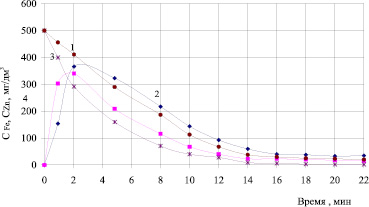
Рис. 3. Кинетика изменения концентрации ионов железа 2, 4 и цинка 1, 2 в растворах с концентрацией CZn2+ = 500 мг/дм3 в процессе гальванокоагуляции с предварительной аэрацией 3, 4 и без предварительной аэрации 1, 2
В качестве образцов исследования были взяты представительные пробы осадков, полученных при одинаковой длительности контакта раствора с гальванопарой и предварительной аэрацией раствора. Анализ проб показал, что значительная масса осадка приходится на долю мелкодисперсного кокса, который вымывается из гальванокоагулятора в результате истирания при непрерывном вращении барабана.
Обработанные результаты рентгенофазового анализа цинксодержащего осадка, полученного из сульфатсодержащих растворов, приведены в таблице.
Рентгенофазовым анализом осадков, полученных при обработке однокомпонентного раствора, не подверженного предварительной аэрации, содержащего ионы цинка, фиксируется наличие фаз магнетита Fe3O4, франклинита ZnFe2O4, гематита Fe2О3, лепидокрокита FeOOH, гидроксидов цинка и железа(III) Zn(OH)2 и Fe(OH)3, вюстита FeO, цинкита ZnO. В осадках, полученных при обработке раствора цинкового купороса с концентрацией 500 мг/дм3 и рН 5,5, обнаружена фаза смитсонита ZnCО3.
Учитывая рыхлую поверхность образующегося Fe(OH)3, процесс сорбции при гальванокоагуляционной обработке раствора, теоретически может протекать с захватом как катионов Zn2+, ZnОН+ , так и ZnO, Zn(ОН)2.
Фазовые составы осадков, полученных без предварительной аэрации / с аэрацией
|
№ п/п |
Фазовый состав в порядке убывания количества фаз |
№ п/п |
Фазовый состав в порядке убывания количества фаз |
||
|
формула |
название фазы |
формула |
название фазы |
||
|
без предварительной аэрации |
с предварительной аэрацией |
||||
|
1 |
Fe3O4 |
магнитит |
1 |
ZnO |
цинкит |
|
2 |
Fe(OH)3 |
гидроксид |
2 |
FeO |
вюстит |
|
3 |
ZnCО3 |
смитсонит |
3 |
Fe3O4 |
магнитит |
|
4 |
ZnFe2O4 |
франклинит |
4 |
Fe2Оз |
гематит |
|
5 |
Fe2О3 |
гематит |
5 |
Fe(OH)3 |
гидроксид |
|
6 |
Zn(OH)2 |
гидроксид |
6 |
ZnFe2O4 |
франклинит |
|
7 |
FeOOH |
лепидокрокит |
7 |
Fe(OH)2 |
гидроксид |
|
8 |
FeO |
вюстит |
8 |
ZnCО3 |
смитсонит |
|
9 |
ZnO |
цинкит |
|||
Выводы
Метод гальванокоагуляции, основанный на использовании эффекта короткозамкнутых контактов гальванического элемента, образуемого гальванопарами «железо-кокс» и «алюминий-кокс», позволяет эффективно извлекать катионы цинка из техногенных гидроминеральных образований.
Установлено что с уменьшением концентрации возрастает доля цинка, удалённая из раствора переводом в труднорастворимые соединения за один и тот же промежуток времени обработки в поле гальванопары «железо-кокс». Смещение рН раствора в более щелочную область значений приводит к увеличению удельного выхода и массовой доли цинка в осадке.
Данные рентгенофазового анализа указывают на то, что на поверхности образующего золя Fe(OH)3 происходит процесс сорбции преимущественно в виде соединений ZnO.
Гальванокоагуляционная обработка цинксодержащих растворов с дополнительной аэрацией и подщелачиванием до рН 6,5–7,5 позволяет извлечь из раствора цинк до 65,14 % в виде ферритов цинка.
Эффективное время обработки растворов составляет 12 минут.
Библиографическая ссылка
Орехова Н.Н., Чалкова Н.Л., Чалкова К.Д. ИЗУЧЕНИЕ ЗАКОНОМЕРНОСТЕЙ ИЗВЛЕЧЕНИЯ ЦИНКА ИЗ ВОДНЫХ РАСТВОРОВ В ПОЛЕ ГАЛЬВАНОПАРЫ ЖЕЛЕЗО-УГЛЕРОД // Успехи современного естествознания. 2016. № 1. С. 147-151;URL: https://natural-sciences.ru/en/article/view?id=35775 (дата обращения: 15.05.2026).



