Scientific journal
Advances in current natural sciences
ISSN 1681-7494
"Перечень" ВАК
ИФ РИНЦ = 0,976
EFFECT OF BASIC STOMATOLOGICAL POLYMERS ON THEIR THERMOMECHANICAL PROPERTIES AND RESISTANCE TO EXTERNAL ENVIRONMENTS
Современные базисные материалы – малорастворимые в водной среде соединения. Однако в большом количестве научных работ доказывается негативное влияние на состояние здоровья пациентов веществ, которые выделяются из материалов [1, 3–6, 8]. Технические требования к качеству и методам испытаний полимерных материалов для базисов зубных протезов изложены в ГОСТ Р 51889-2002 [2] и регламентируют содержание остаточного мономера метилакрилата, которое определяется хроматографическим методом после предварительной экстракции образцов в ацетоне или метаноле. В работе [6] авторы предлагают промывать не менее суток в проточной воде протезы на основе нейлона в связи с тем, что в водной вытяжке содержание формальдегида превышает нормативное значение в 6,9 раза.
Безусловно, в инструкции по синтезу полимерного материала учтены требования ГОСТ Р 51889-2002, и содержание остаточного мономера в готовом изделии не должно превышать установленных нормативных значений. В то же время очевидно, что в процессе взаимодействия материала со средой могут выделяться соединения, которые не нормируются в ГОСТ Р 51889-2002. В этой связи необходимы обобщенные критерии оценки качества изготовленных зубных протезов.
Цель работы – экспериментально исследовать термомеханические свойства образцов базисного стоматологического полимера «Фторакс», приготовленных при различных соотношениях компонентов – порошка (Т) и жидкости (Ж) в различных пропорциях (в пределах допустимых значений) до и после взаимодействия с отмывочными растворами различного состава.
Материалы и методы исследования
На базе зуботехнической лаборатории стоматологической поликлиники УГМУ были изготовлены пластмассовые определенной массы образцы марки «Фторакс» – диаметром 50 мм, толщиной 0,6 мм согласно ГОСТу [2] с соотношением компонентов 2:1 – № 1 (1); № 1 (2); 2:0,9 – № 0,9 (1); № 0,9 (2); 2:1,1 – № 1,1 (1). Образцы погружали: в дистиллированную воду, 0,9 % раствор хлорида натрия, 0,9 % раствор хлорида кальция и модельный раствор слюны, состав которого приведен в табл. 1.
Таблица 1
Состав модельного раствора слюны
|
Компонент |
Формула |
Концентрация, г/л |
|
Роданид калия |
KSCN |
0,5170 |
|
Бикарбонат натрия |
NaHCO3 |
1,2530 |
|
Хлорид калия |
KCl |
1,4710 |
|
Дигидрофосфат натрия |
NaH2PO4 ·2Н2О |
0,1878 |
|
Молочная кислота |
C3H6O3 |
0,9000 |
|
Физико-химические свойства |
рН = 6,60 œ = 3,86 мСм/см Вк = 3,18 ммоль/л∙Во = 1,5 ммоль/л |
|
Объем каждого раствора, в который погружался образец, составлял 30 мл. Через 24 часа измеряли электропроводность растворов (с помощью кондуктометра «Анион 7020») и концентрацию веществ в водной среде (с использованием осмометра криоскопического медицинского ОСКР-1М).
Таблица 2
Условия определения термомеханических кривых
|
Параметр |
Значение |
|
Режим |
Пенетрация |
|
Диаметр индентора |
3,94 мм |
|
Диаметр образца |
8–9 мм |
|
Толщина образца |
1–3 мм |
|
Величина нагрузки |
5 сН |
|
Действие нагрузки во времени |
Постоянная |
|
Скорость нагрева |
2 К/мин |
|
Среда |
Азот, 50 мл/мин |
Обзорные ИК-спектры НПВО (нарушенного полного внутреннего отражения) образцов записывали на кафедре высокомолекулярных соединений УрФУ с помощью ИК-Фурье Nicolet 6700 спектрометра в области волновых чисел 4000–500 см–1. Спектры определяли на отражение света. Термомеханические исследования проводили с помощью прибора TMA 202 Netzsch в диапазоне температур 20–250 °С. Условия измерений приведены в табл. 2.
Термомеханические кривые получали для образцов до и после их взаимодействия с водными средами различного состава. По термомеханическим кривым определяли температуру стеклования (Тс). Температура стеклования – это температура, при которой аморфный полимер из высокоэластичного состояния переходит в стеклообразное состояние. Чем выше температура стеклования, тем меньше низкомолекулярных примесей содержит образец [7].
Результаты исследования и их обсуждение
В табл. 3 приведены результаты экспериментов.
Из данных табл. 3 следует:
– электропроводность водных систем увеличивается по сравнению с электропроводностью дистиллированной воды (№ 1–4). Это свидетельствует о том, что примеси, которые вымываются из твердых образцов акрилового полимера, являются электролитами. Наименьшее возрастание электропроводности раствора наблюдается после его взаимодействия с образцом, приготовленным при соотношении компонентов 2:1.
– плотность растворов после взаимодействия с образцами увеличилась, что свидетельствует об извлечении веществ из полимера. Однако концентрацию веществ в растворе не удалось измерить методом осмометрии;
– электропроводность МРС после взаимодействия с образцами увеличивается, концентрация веществ в растворе и плотность растворов незначительно снижаются;
Таблица 3
Электропроводность, плотность и концентрация водных вытяжек из образцов, изготовленных при разном соотношении компонентов (Т:Ж)
|
№ п/п |
Образец Т:Ж |
Раствор |
Электропроводность, мкСм/см (мСм/см) |
Плотность, г/мл |
Концентрация, ммоль/кг |
|
1 |
Н2О |
2,1 мкСм/см |
0,9967 |
0 |
|
|
2 |
2:0,9 |
Н2О |
44,5 мкСм/см |
0,9992 |
0 |
|
3 |
2:1,0 |
Н2О |
9,7 мкСм/см |
1,0019 |
0 |
|
4 |
2:1,1 |
Н2О |
70,2 мкСм/см |
1,0035 |
0 |
|
5 |
МРС |
3,78 мСм |
1,0045 |
78 |
|
|
6 |
2:0,9 |
МРС |
3,94 мСм |
1,0025 |
77 |
|
7 |
2:1,0 |
МРС |
4,0 мСм |
0,9997 |
76 |
|
8 |
2:1,1 |
МРС |
3,97 мСм |
1,0020 |
76 |
|
9 |
NaCl |
13,0 мСм |
1,0112 |
278 |
|
|
10 |
2:0,9 |
NaCl |
13,7 мСм |
1,0060 |
286 |
|
11 |
2:1,0 |
NaCl |
13,2 мСм |
1,0059 |
282 |
|
12 |
2:1,1 |
NaCl |
13,3 мСм |
1,0047 |
275 |
|
13 |
CaCl2 |
15,0 мСм |
1,0108 |
189 |
|
|
14 |
2:0,9 |
CaCl2 |
16,8 мСм |
1,0029 |
197 |
|
15 |
2:1,0 |
CaCl2 |
17,2 мСм |
1,0069 |
200 |
|
16 |
2:1,1 |
CaCl2 |
17,2 мСм |
1,0083 |
197 |
– концентрация веществ в растворе и электропроводность 0,9 % раствора хлорида натрия после взаимодействия с образцами увеличивается незначительно, а плотность растворов снижается. Это может быть связано с сорбцией хлорида натрия образцом;
– концентрация веществ в растворе и электропроводность 0,9 % раствора хлорида кальция после взаимодействия с образцами увеличивается более существенно, чем после взаимодействия с 0,9 % раствором хлорида натрия, а плотность растворов также снижается. Это можно объяснить сорбцией веществ из раствора образцом.
ИК-спектры водных растворов, полученных после контакта дистиллированной воды с образцами с соотношением исходных компонентов 2:0.9; 2:1; 2:1.1, приведены на рис. 1.
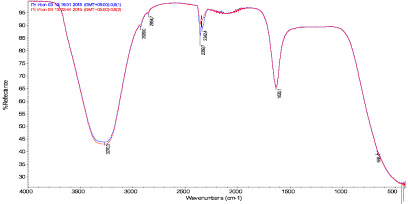
Рис. 1. ИК-спектры водных растворов веществ, вымытых из этих образцов с соотношением исходных компонентов 2:0,9
Из рис. 1 видно, что спектры двух параллелей образца «0,9» качественно совпадают, однако интенсивности полос образца «0,9 (1)» в диапазонах 2340–2360 и 2840–2945 см–1 (валентные колебания в группах СН3 и СН2) больше, в сравнении со спектром образца «0,9 (2)». Во всех спектрах идентифицируются полосы, характерные для ИК-спектра воды, что подтверждается сравнением с библиотечными данными. Интенсивности широкой полосы с максимумом в области валентных колебаний О-Н-связей при 3200–3400 см–1 и небольших пиков, характерных для спектров алифатических углеводородов, около 2929 и 2855 см–1 (связанных соответственно с асимметричными и симметричными валентными колебаниями С-Н-связей в метиленовых группах) изменяются антибатно в ряду 0,9 (1) – 1 (1) – 1,1 интенсивность полосы в этом ряду возрастает, а пиков – убывает. Из этого можно предположить уменьшение концентрации органического вещества в растворе.
Из анализа ИК-спектров исходного материала следует, что частоты полос 2989; 2984; 2919 и 2849 см–1 отвечают валентным колебаниям групп СН3 и СН2, 1780 см–1 – колебаниям С = О групп, 1141–1260 см–1 и 839, 668, 657 – колебаниям С-F групп. Это согласуется с литературными данными о химическом строении «Фторакса», который получается сополимеризацией фторсодержащих акриловых мономеров.
Сравнение спектров образцов с библиотечными данными однозначно показывает, что основным компонентом в составе всех образцов является полиметилметакрилат: степень соответствия – более 95 % . В пробах отсутствуют примеси этилметакрилата и метилметакрилата, поскольку в спектре образцов не наблюдаются полосы вблизи 3430 см–1, при 3105 см–1, в интервалах 1640–1580 и 580–690 см–1. По тем же причинам можно исключить присутствие дибутилфталата. Принципиальные отличия спектра диоксида титана от спектров пробы и полимера подтверждают отсутствие в образцах TiO2. Гидрохинон проявляет себя в спектре рядом характеристических полос: с максимумом 3320 см–1, полосы 1856; 1606 и 1626 см–1, группа полос в интервале 495–625 см–1. В исследованных образцах гидрохинона нет, так как не наблюдаются характеристические полосы (рис. 2).
Анализ спектров образцов с соотношением компонентов 2:0,9; 2:1 и 2:1,1 в совмещенных координатах (рис. 2) позволяет констатировать: интенсивность полос 2849,3 и 2922,9 см–1 убывает в ряду 2:0,9 > 2:1 > 2:1,1. Полосы в этом спектральном диапазоне характерны для спектров алифатических углеводородов и отражают колебания связей C–H в группах СН3 и СН2.
В табл. 4 приведена температура стеклования образцов до и после контакта с низкомолекулярными жидкостями.
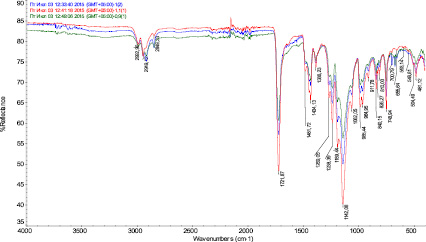
Рис. 2. ИК-спектры образцов «0,9 (1)», «1 (2)» и «1,1» в совмещенных координатах
Таблица 4
Результаты определения температуры стеклования образцов до и после взаимодействия образцов с водными средами разного состава
|
Образец Т:Ж |
Температура стеклования (Тс), °С (±0,5 °С) |
||||
|
Образцы без отмывки |
Дистиллированная вода |
0,9 % NaCl |
0,9 %CaCl2 |
МРС |
|
|
2:0,9 |
109 |
119 |
118,5 |
121 |
119 |
|
2:1 |
112 |
120 |
120 |
120 |
119 |
|
2:1,1 |
100 |
101 |
113 |
102 |
103 |
Разные величины Тс образцов, приготовленных при разном соотношении компонентов, могут свидетельствовать о разном содержании низкомолекулярных органических примесей в образцах [7]. Минимальное содержание органических примесей в образце, приготовленном при соотношении Т:Ж = 2:1, максимальное – в образце, приготовленном при соотношении Т:Ж = 2:1,1.
Из данных, представленных в табл. 4, следует, что образец, приготовленный с соотношением компонента Т:Ж = 2:1, может быть эффективно отмыт в дистиллированной воде и состав раствора не влияет на конечный результат (за исключением модельного раствора слюны). Образец, приготовленный при соотношении Т:Ж = 2:0,9, может быть эффективно отмыт в растворе с большой ионной силой – 0,9 % раствор хлорида кальция. Образец, приготовленный при соотношении Т:Ж = 2:1,1, содержит большое количество примесей, которые не выделяются в вышеперечисленные растворы.
Выводы
1. Выделение из образцов непрореагировавших органических соединений в водную среду зависит от соотношения Т:Ж, при котором приготовлен образец, и от состава водной среды, с которой он взаимодействует. Образец, приготовленный с соотношением компонента Т:Ж = 2:1, может быть эффективно отмыт дистиллированной водой. Образец, приготовленный при соотношении Т:Ж = 2:0,9, может быть эффективно отмыт в 0,9 % растворе хлорида кальция. Образец, приготовленный при соотношении Т:Ж = 2:1,1, не может быть эффективно отмыт ни в дистиллированной воде, ни в 0,9 % растворах солей натрия или кальция.
2. Оценить количество вымытых нелетучих веществ из полимера, при использовании в качестве отмывочного раствора дистиллированной воды, можно по изменению плотности раствора. При использовании в качестве отмывочного раствора 0,9 % раствора хлорида кальция качественно оценить отмывку образца (или изделия) можно по относительному изменению электропроводимости или концентрации веществ, измеренной методом осмометрии.
3. При использовании в качестве отмывочного раствора 0,9 % раствора хлорида натрия или МРС оценить эффективность отмывки образца (или изделия) можно только по анализу термомеханических свойств образца (или изделия) т.е. по определению температуры стеклования.
4. В качестве критерия оценки свойств базисных стоматологических полимерных материалов можно использовать температуру стеклования изделий или образцов, определенную термомеханическим методом.
Библиографическая ссылка
Белоконова Н.А., Костров Я.В., Жолудев С.Е., Вшивков С.А., Галяс А.Г. ВЛИЯНИЕ СОСТАВА БАЗИСНЫХ СТОМАТОЛОГИЧЕСКИХ ПОЛИМЕРОВ НА ИХ ТЕРМОМЕХАНИЧЕСКИЕ СВОЙСТВА И УСТОЙЧИВОСТЬ К ВНЕШНИМ СРЕДАМ // Успехи современного естествознания. 2016. № 5. С. 9-13;URL: https://natural-sciences.ru/en/article/view?id=35889 (дата обращения: 17.05.2026).



