Scientific journal
Advances in current natural sciences
ISSN 1681-7494
"Перечень" ВАК
ИФ РИНЦ = 0,976
STUDY OF CONDENSATION PRODUCT OF 4-AMINO-1,2,4-TRIAZOLE AND FORMALDEHYDE; PREPARATION OF COPPER (II) COMPLEX ON ITS BASE AND COMPARISON OF THEIR BIOLOGICAL ACTIVITY
Азотсодержащие гетероциклические соединения класса 1,2,4-триазола составляют большую группу фунгицидов и активаторов роста растений. Так, например, паклобутразол (4,4,-диметил-2-(1,2,4-триазол-1-ил)-1-(4-хлорфенил)-пентанол-3) используется в сельском хозяйстве в качестве ретардантов роста растений, при этом он проявляет и фунгицидные свойства. Аналогичную бинарную активность проявляют производные 1,2,4-триазола: униказол, диниконазол и баронет [4].
Производители препаратов для борьбы с болезнями сельскохозяйственных культур, как правило, не учитывают тот факт, что азотсодержащие соединения способны взаимодействовать с ионами металлов, находящихся в почве, с образованием достаточно прочных комплексных соединений. Процессы комплексообразования ионов металлов с азотсодержащими лигандами могут привести либо к увеличению их биологической активности, либо полностью подавить данный процесс. Влияние комплексообразования на процессы роста и развития растений изучено недостаточно. Поэтому синтез нового полиазотсодержащего соединения класса 1,2,4-триазолов, изучение возможностей его комплексообразования с ионами меди (II), а также исследование биологической активности полученных соединений и их влияние на рост и развитие растений является актуальной задачей.
Цель исследования – получить продукт конденсации 4-амино-1,2,4-триазола с формальдегидом и на его основе синтезировать новое комплексное соединение с нитратом меди (II). Для полученных соединений определить биологическую активность на примере экспериментов по проращиванию семян огурцов сорта «Мазай».
Материалы и методы исследования
Экспериментальная часть
Для синтеза использовали 4-амино-1,2,4-триазол (NH2trz) (х.ч.), формальдегид CH2O (17 %-ный водный раствор), Cu(NO3)2·3H2O (х.ч.). Элементный анализ на C, H, N выполнен в аналитической лаборатории ИНХ СО РАН (г. Новосибирск) на приборе EURO EA 3000 фирмы EuroVector (Италия). ИК-спектры поглощения снимали на FTIR-спектрометре IRAffinity-1S (Shimadzu) в области 400–4000 см–1. Образцы готовили в виде таблеток в KBr.
Синтез
Синтез органического соединения общей формулой С15H22N20O (L) проводили по методике, близкой к [7]. Навеску 4-амино-1,2,4-триазола (0,2522 г; 0,003 моль) растворяли в 7 мл дистиллированной воды и к полученному раствору приливали 0,46 мл (0,003 моль) 17 %-го раствора формальдегида. Смесь нагревали при постоянном перемешивании при температуре 60 °С в течение 45 мин. После окончания процесса из образовавшегося раствора отгоняли воду в ротационном испарителе. Полученный бесцветный продукт высушивали на воздухе, а затем в эксикаторе над ангидроном до полного удаления воды.
Найдено ( %): C, 36,0; H, 4,9; N, 55,9. С15H22N20O. Вычислено ( %): C, 36,1; H, 4,5; N, 56,2. ИК-спектр, ν/см–1: 3380, 1650 (ОН, NH2); 3108 (С–Н); 1504, 650 (NH2trz); 1198, 1205 (N–NН2).
Синтез комплексного соединения состава [Cu3L(H2O)](NO3)6 проводили следующим образом. Полученный в синтезе лиганд (0,001 моль) растворяли в 20 мл этилового спирта, образовывавшуюся маслянистую пленку удаляли с помощью фильтра «синяя лента». К раствору лиганда приливали этанольный (15 мл) раствор Cu(NO3)2·3H2O (0,3622 г; 0,0015 моль) с добавлением одной капли конц. азотной кислоты. Сразу после перемешивания выпадал осадок голубого цвета. Осадок отфильтровывали и промывали несколько раз этиловым спиртом, высушивали на воздухе. Содержание меди определяли трилонометрически после разложения проб в смеси конц. H2SO4 и HClO4 (1:1).
Найдено ( %): C, 16,2; H, 2,6; N, 34,0; Cu, 17,9. C15H24Cu3N26O20. Вычислено ( %): C, 16,7; H, 2,2; N, 33,7; Cu, 17,6. ИК-спектр: ν/см–1: 3394, 1650 (ОН, NH2); 3266 (С–Н); 1557, 630 (NH2trz); 1212 (N–NН2).
Результаты исследования и их обсуждение
Реакция конденсации 4-амино-1,2,4-триазола и формальдегида проведена по схеме:
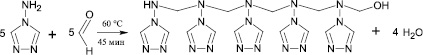
Полученный продукт является прозрачной гелеобразной массой. Нерастворим в CH2Cl2, бензоле, толуоле, гексане; хорошо растворим в воде, этаноле, ацетоне, кислотах, ДМСО. При хранении на воздухе при комнатной температуре сильно гигроскопичен.
Комплекс образуется в результате взаимодействия этанольных растворов нитрата меди (II) и лиганда. Раствор нитрата меди подкисляли азотной кислотой для улучшения растворимости. Осадок комплекса выделяется по схеме 2:
3Cu(NO3)2 + H2O + L → [Cu3L(H2O)](NO3)6↓.
Комплекс нерастворим в этаноле, изопропаноле, ацетоне, CH2Cl2, бензоле, толуоле, гексане; хорошо растворяется в воде, кислотах, ДМСО. При хранении на воздухе при комнатной температуре устойчив в течение длительного времени, не гигроскопичен.
В высокочастотной области ИК-спектров L и комплекса наблюдаются полосы при 3380, 3394 и 1650 cм–1, которые соответствуют валентным колебаниям связанной ОН-группы и координационной воды.
Для вывода о способах координации лиганда наиболее информативным является анализ положения полос поглощения в области 1550–1510 см–1. Так, полосы валентно-деформационных колебаний триазольных циклов NH2trz наблюдаются при 1530–1520 см–1, в спектре комплекса они смещены на 20–30 см–1 в область высоких частот. Смещение и изменение интенсивности полос поглощения свидетельствует о координации атомов азота азольных циклов к меди [8].
В области 600–700 см–1 в спектре NH2Trz присутствует одна полоса при 654 см1. В спектре комплекса наблюдается одна полоса при 630 см–1, что указывает на бидентатно-мостиковую координацию H2Trz атомами N1,N2 цикла (симметрия C2v) [8]. Вывод о способе координации NH2trz подтверждает анализ положения полосы экзоциклической связи (N–NН2) данного лиганда. В спектре NH2trz наблюдается дублет при 1190, 1205 см–1, а в спектре комплекса присутствует одна полоса при 1212 см–1. Такое смещение также указывает на бидентатно-мостиковую координацию NH2trz [3] к ионам меди атомами N1, N2.
Анализ полученных данных свидетельствует, что реакция конденсации 4амино-1,2,4-триазола с формальдегидом прошла успешно. В результате образовалось новое азотсодержащее органическое соединение, которое выступает в качестве лиганда при взаимодействии с нитратом меди (II) с образованием комплекса димерного строения, в котором к каждому иону меди координированы атомы азота соседних триазольных циклов молекулы L, а также атомы кислорода её гидроксильной группы и молекулы воды. При таком способе координации координационное число иона меди (II) равно 4, а координационные полиэдры – искаженные тетраэдры CuN4 и CuN2O2. Полоса колебания ν3(NO3) нитрат-анионов при 1350 см–1 в спектре комплекса практически не смещается по сравнению с полосой в спектре нитрата меди, что указывает на внешнесферное положение данных анионов. Наиболее вероятная структура комплекса в виде димера представлена на рис. 1. Структуры и свойства комплексных соединений меди (II) с подобной бидентатно-мостиковой координацией 1,2,4триазолов описаны в статьях [5, 6, 9, 10].
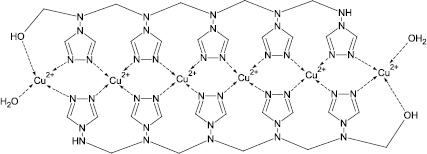
Рис. 1. Модель димера олигомерной структуры катиона [Cu3L(H2O)]6+
Для определения биологической активности полученного лиганда и его комплекса были проведены эксперименты по проращиванию семян огурцов сорта «Мазай».
Семена огурцов проращивали в 0,025 %-ных растворах полученного лиганда, его комплекса, а также в растворе известного активатора роста растений «Энерген» (ЗАО «ТПК Техноэкспорт», Россия) по методикам [2, 1]. В качестве контроля использовали семена огурцов, замоченные в дистиллированной воде. На 4-е и 8-е сутки подсчитывали число проросших семян и измеряли длину корня у каждого проростка. На 15-е сутки измеряли длину стебля, корня и площадь поверхности листа взрослого растения.
Эксперимент показал (рис. 2), что прирост длины корня проростков в растворе L относительно контрольного опыта составил 21 %, а взрослого растения 20 %. Для «Энергена» эти показатели – 8 и 38 % соответственно. Раствор комплекса проявляет противоположные свойства – длина корня проростков относительно контрольного ниже на 72 %, взрослого растения на 89 %. Площадь поверхности листа в опытах с L больше относительно контрольного на 17 %, а длина стебля ниже на 36 %. Площадь поверхности листа в опытах с комплексом практически не отличается от контрольного, а длина стебля взрослого растения ниже на 72 %, такие же показатели наблюдаются в опыте с «Энергеном».
Полученные данные указывают на то, что синтезированное соединение С15H22N20O проявляет ярко выраженные свойства активатора роста растений, а полученное на его основе комплексное соединение меди (II) проявляет свойства ретарданта. Значительное утолщение стебля и более темный цвет листьев в опытах с комплексным соединением по сравнению с остальными образцами, подтверждает ретардантные свойства комплекса. Ретарданты, как класс соединений, являются эффективным средством в борьбе против полегания зерновых культур, а также используются для выведения карликовых форм декоративных растений (рис. 3).
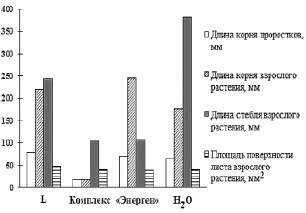
Рис. 2. Ростовые показатели проростков и взрослых растений огурцов сорта «Мазай»

Рис. 3. Нормальная (два слева) и ретардантная (два справа) формы растений
Однократное воздействие L и его комплекса меди (II) на семена растений не привело к снижению урожайности огурцов сорта «Мазай», в обоих случаях наблюдается высокий показатель – не менее 1,5 кг в неделю с куста. Отметим заметное ускорение начала цветения ретардантной формы – на две недели ранее остальных образцов.
Таким образом, в представленной работе показано, что использование в сельском хозяйстве азотсодержащих соединений в качестве активаторов роста растений может приводить к образованию новых соединений, обладающих ретардантными свойствами. Это может происходить в результате протекания реакций комплексообразования с ионами металлов, активно используемых в сельском хозяйстве и находящихся в почве.
Библиографическая ссылка
Проценко А.Н., Шакирова О.Г. ИЗУЧЕНИЕ ПРОДУКТА КОНДЕНСАЦИИ 4-АМИНО-1,2,4-ТРИАЗОЛА И ФОРМАЛЬДЕГИДА, ПОЛУЧЕНИЕ КОМПЛЕКСА МЕДИ (II) НА ЕГО ОСНОВЕ И СРАВНЕНИЕ ИХ БИОЛОГИЧЕСКОЙ АКТИВНОСТИ // Успехи современного естествознания. 2016. № 5. С. 38-42;URL: https://natural-sciences.ru/en/article/view?id=35894 (дата обращения: 16.05.2026).



