Scientific journal
Advances in current natural sciences
ISSN 1681-7494
"Перечень" ВАК
ИФ РИНЦ = 0,976
THE IMPROVING METHOD OF SAMPLE PREPARATION FOR THE QUANTITATIVE DETERMINATION OF HEAVY METALS IN THE FLOWERS OF CHAMOMILE (MATRICАRIA CHAMOMILLA) BY ICP-AES
Цветки ромашки аптечной обладают широким спектром биологической активности. Они оказывают спазмолитическое, противовоспалительное, антисептическое, ранозаживляющее, потогонное, желчегонное, спазмолитическое, слабовыраженное анальгетическое действие и входят в число двадцати самых используемых лекарственных растительных препаратов в России [1].
Важным показателем качества ЛРС и ЛРП является содержание в них тяжелых металлов. В настоящее время одним из основных фармакопейных методов элементного анализа ЛРС и ЛРП является метод атомно-эмиссионной спектрометрии с индуктивно связанной плазмой (ИСП-АЭС) [5]. Он характеризуется высокой селективностью, чувствительностью и надежностью и показывает индивидуальные, а не суммарные результаты для всех анализируемых металлов.
В процедуре элементного анализа методом ИСП-АЭС наиболее сложным звеном является этап пробоподготовки, на долю которого приходится до 90 % времени и общей ошибки результатов количественного определения содержания элементов в образце [2]. Выбор методики пробоподготовки во многом зависит от определяемого элемента и его концентрации, а также от природы матрицы. Цветки ромашки аптечной представляют собой органическую матрицу, в составе которой тяжелые металлы могут находиться в очень малых количествах и в связанном состоянии с органическими соединениями. В настоящее время отечественной и зарубежными фармакопеями, а также агентством по охране окружающей среды США (Environmental Protection Agency – ЕРА) разработаны методики пробоподготовки растительного сырья для спектрального элементного анализа, предусматривающие полное разложение органических молекул с помощью различных смесей на основе концентрированной азотной кислоты и других сильно действующих реагентов (концентрированных плавиковой, хлорной, соляной, серной кислот, пероксида водорода и т.д.) [2, 6, 9, 10]. Использование одной концентрированной азотной кислоты не обеспечивает разложение ароматических соединений, так как π-связь бензольного кольца не разрушается под ее действием даже при высоких температурах и под давлением [4]. Однако из литературных данных известно, что при контролируемых условиях азотная кислота при высоких давлении и температуре позволяет сделать разложение воспроизводимым. Как следствие, результаты, получаемые при микроволновом разложении органических матриц азотной кислотой в закрытых сосудах, сравнимы с результатами разложения в автоклавах традиционными методами [4].
Цель данного исследования – определить условия микроволнового разложения, обеспечивающие максимальный переход тяжелых металлов в раствор при неполном разложении органической матрицы, и разработать на их основе альтернативную методику мокрой минерализации азотной кислотой цветков ромашки аптечной в системе микроволнового разложения. Эта методика позволит упростить и обезопасить этап пробоподготовки элементного анализа методом ИСП-АЭС за счет отказа от пожаро- и взрывоопасных окислителей (хлорной кислоты и пероксида водорода). Кроме того, исключение солюбилизаторов (серной, плавиковой и соляной кислот) снизит риск загрязнения анализируемого раствора реактивами, что очень важно при определении малых содержаний элементов (азотная кислота является одной из немногих кислот, для которых достижима сверхвысокая степень чистоты [4]).
Материалы и методы исследования
В качестве объектов исследования использовали стандартный образец чая TEA LEAVES (INCT-TL-1) производства Institute of Nuclear Chemistry and Technology, Польша, отраслевой стандартный образец состава зерна ржи (ЗРЖ-01) ОСО № 10-201-2014, производства ВНИИ агрохимии имени Д.Н. Прянишникова, Россия, цветки ромашки аптечной производителей ОАО «Красногорсклексредства» серия 90314, НПО «Микроген» серия Б010811, ООО «Парафарм» серия 150315, ЗАО «Иванчай» серия 030515, ООО «РосБио» серия 10612, приобретенные в розничных аптечных сетях г. Москвы.
Подготовку образцов для анализа проводили по трем методикам: ЕРА [10], фармакопейной [6, 9] и разрабатываемой альтернативной. Все образцы сушили до постоянной массы при 105 °С в течение двух часов, растирали в однородный порошок и просеивали через сито с диаметром отверстий 1 мм. Образцы массой 1,0 г (точная навеска) помещали в сосуд для микроволнового разложения и добавляли реагенты в соответствии с выбранной методикой. По методике ЕРА использовали смесь 9 см3 концентрированной азотной кислоты, 0,5 см3 концентрированной соляной кислоты и 2 см3 концентрированного пероксида водорода. По фармакопейной методике разложение проводили в 2 этапа по одинаковой программе: сначала с использованием 6 см3 концентрированной HNO3 и 4 см3 концентрированной HCL, затем с добавлением 4 см3 H2SO4. Все реагенты, применяемые при минерализации, были аналитической степени чистоты (For Trace Metal Analysis), производства Acros Organics. Минерализацию проб проводили с помощью микроволновой системы Anton Paar Multiwave 3000. Использовали параметры микроволновой печи, обеспечивающие максимальный переход определяемых элементов в раствор (см. раздел «обсуждение результатов»). Полученные после микроволнового разложения растворы охлаждали до комнатной температуры, фильтровали через фильтр «синяя лента» в мерные колбы объемом 25 см3 и доводили до метки деионизованной водой, очищенной на установке Milli-Q – Integral 3 фирмы Millipore, Франция.
Измерения содержания тяжелых металлов проводили на атомно-эмиссионном спектрометре с индуктивно связанной плазмой Оptima 8300 DV фирмы Реrkin Elmer с использованием стандартных образцов мышьяка, кадмия, хрома, меди, железа, ртути, никеля, свинца, цинка производства фирмы Merck (CRM) c аттестованным значением СО 1000 мг/дм3. Характеристические длины волн (λ, нм) по выбранным элементам представлены в табл. 1. За результат 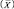 принимали среднее значение концентраций, полученных по результатам четырех параллельных измерений по выбранным длинам волн. Доверительный интервал ( ± Δx) определяли по формуле
принимали среднее значение концентраций, полученных по результатам четырех параллельных измерений по выбранным длинам волн. Доверительный интервал ( ± Δx) определяли по формуле
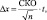
где n – число параллельных измерений; t – коэффициент Стьюдента при числе степеней свободы f = n – 1 и доверительной вероятности P = 0,95.
Результаты исследования и их обсуждение
Частные фармакопейные статьи на ромашку аптечную не содержат перечня тяжелых металлов, подлежащих контролю при фармакопейном анализе. Выбранный нами круг определяемых в ромашке элементов (As, Cd, Cr, Cu, Fe, Ni, Pb, Zn) обусловлен представленными в литературе результатами исследований содержания тяжелых металлов в различных типах растительного сырья и требованиями к нормированию тяжелых металлов в ЛС, ЛРС и фитопрепаратах в национальных, региональных и международных фармакопеях [5].
Таблица 1
Длины волн элементов, пределы обнаружения и относительная погрешность метода по диапазонам содержания
|
Элемент |
Длина волны, нм |
Предел обнаружения7, мкг/дм3 |
Диапазон содержания3, мг/кг |
Относительная погрешность метода3, %, Р = 0,95 |
|
Cd (кадмий) |
226,502 |
0,1 |
0,01–0,10 0,1–1,0 |
70 50 |
|
Pb (свинец) |
220,353 |
0,05 |
0,05–0,50 0,5–5,0 |
70 50 |
|
Cu (медь) |
324,752 224,700 |
0,4 |
0,5–5,0 |
40 |
|
Fe (железо) |
238,204 239,256 |
0,1 |
2–1000 |
20 |
|
Zn (цинк) |
206,200 213,857 |
0,2 |
1–5000 |
25 |
|
Cr (хром) |
267,716 |
0,2 |
1–100 |
25 |
|
As (мышьяк) |
188,979 |
1 |
н/д* |
н/д* |
|
Hg (ртуть) |
194,168 |
1 |
0,01–1,0 |
20 |
|
Ni (никель) |
231,604 227,022 |
0,5 |
0,5–5,0 |
50 |
Примечание. *н/д – нет данных.
Таблица 2
Временно-температурные режимы микроволнового разложения
|
Этап |
I режим |
II режим |
III режим |
IV режим |
||||
|
Время, мин |
Т, °С |
Время, мин |
Т, °С |
Время, мин |
Т, °С |
Время, мин |
Т, °С |
|
|
1 |
5 |
0–120 |
3 |
0–80 |
3 |
0–80 |
3 |
0–80 |
|
2 |
5 |
120 |
2 |
80 |
2 |
80 |
2 |
80 |
|
3 |
10 |
120–165 |
10 |
80–165 |
10 |
80–165 |
10 |
80–165 |
|
4 |
– |
– |
10 |
165 |
30 |
165 |
45 |
165 |
Разработка альтернативной методики микроволнового разложения цветков ромашки концентрированной азотной кислотой заключалась в выборе значений объема кислоты, температуры, времени разложения, обеспечивающих наиболее полное извлечение As, Cd, Cr, Cu, Fe, Ni, Pb, Zn из 1 г навески образца (навеска, максимально допустимая для используемой микроволновой печи). Сначала подбирали температурно-временной режим при фиксированном объеме кислоты. При навеске в 1 г максимально достижимая температура составляет 165 °С, что соответствует давлению 40 бар. Были рассмотрены 4 режима микроволнового разложения (табл. 2).
Как видно из представленных в табл. 3 данных, минимальная степень извлечения наблюдается при использовании режима I, который характеризуется высокой скоростью подъема температуры и, как следствие, резким возрастанием давления, вплоть до критических значений. При достижении более равномерного нагревания образцов (режим II) степень извлечения тяжелых металлов выше. Максимальная степень извлечения наблюдается при использовании режима III (увеличенное время выдержки образца при высокой температуре и давлении 38–39 бар), который признан оптимальным. Дальнейшее увеличение времени выдержки (режим IV) не оказывает существенного влияния на степень извлечения тяжелых металлов из образца в раствор.
На следующем этапе определяли оптимальный объем концентрированной азотной кислоты, обеспечивающий максимальное вскрытие пробы (табл. 4). Полное смачивание 1 г навески измельченной ромашки происходит при использовании 7 см3 кислоты, поэтому эта величина была принята за минимальное значение.
Как следует из табл. 4, степень извлечения тяжелых металлов при использовании 8, 9 и 10 см3 кислоты отличается незначительно.
Результаты извлечения тяжелых металлов по разработанной альтернативной методике (навеска образца – 1 г, объем концентрированной азотной кислоты – 8 см3, III режим микроволнового разложения) сравнивали с результатами извлечения по референсным методикам (ЕРА и фармакопейной), оценивая их содержание в стандартных образцах чая и зерен ржи (табл. 5).
Таблица 3
Результаты разложения цветков ромашки производителя ОАО «Красногорсклексредства» с использованием 4 режимов разложения
|
Режим разложения |
Содержание элементов в цветках ромашки, мг/кг |
||||||||
|
Fe |
Ni |
Zn |
Cu |
Cr |
As |
Pb |
Cd |
Hg |
|
|
I режим |
571,1 |
1,66 |
24,76 |
9,23 |
1,55 |
< ПКО |
< ПКО |
0,10 |
< ПКО |
|
II режим |
578,9 |
1,67 |
25,06 |
9,31 |
1,59 |
< ПКО |
< ПКО |
0,11 |
< ПКО |
|
III режим |
609,3 |
1,79 |
26,96 |
9,41 |
1,70 |
< ПКО |
< ПКО |
0,11 |
< ПКО |
|
IV режим |
610,1 |
1,79 |
26,93 |
9,40 |
1,71 |
< ПКО |
< ПКО |
0,11 |
< ПКО |
Таблица 4
Результаты разложения цветков ромашки с использованием различного объема концентрированной азотной кислоты
|
Элемент |
7 см3 HNO3 |
8 см3 HNO3 |
9 см3 HNO3 |
10 см3 HNO3 |
|
Fe |
565,7 |
585,3 |
586,1 |
586,2 |
|
Ni |
1,62 |
1,81 |
1,81 |
1,81 |
|
Zn |
25,6 |
27,0 |
27,3 |
27,2 |
|
Cu |
8,51 |
10,3 |
10,2 |
10,3 |
|
Cr |
1,71 |
2,01 |
2,02 |
2,01 |
Таблица 5
Сравнение результатов извлечения тяжелых металлов из СО растительного сырья с помощью различных методик пробоподготовки
|
Cтандартный образец |
Элемент |
Аттестованное значение*, мг/кг |
Экспериментальное значение |
||
|
EPA |
EP |
Альтернативная |
|||
|
TEA LEAVES (INCT-TL-1) |
Cd |
0,030 ± 0,004 |
0,060 ± 0,026 |
0,070 ± 0,055 |
0,040 ± 0,026 |
|
Cr |
1,91 ± 0,22 |
1,96 ± 0,16 |
2,08 ± 0,54 |
2,14 ± 0,18 |
|
|
Cu |
20,4 ± 1,5 |
28,8 ± 3,5 |
20,6 ± 2,2 |
26,0 ± 1,2 |
|
|
Fe** |
432 |
610 ± 93 |
524 ± 22 |
565 ± 54 |
|
|
Ni |
6,12 ± 0,52 |
5,77 ± 0,49 |
5,58 ± 0,40 |
6,45 ± 0,88 |
|
|
Pb |
1,78 ± 0,24 |
1,73 ± 0,65 |
2,03 ± 1,77 |
1,27 ± 0,45 |
|
|
Zn |
34,7 ± 2,7 |
36,8 ± 9,9 |
41,2 ± 4,3 |
42,8 ± 6,1 |
|
|
(ЗРЖ-01) ОСО № 10 – 201–2014 |
Cd |
0,333 ± 0,093 |
0,333 ± 0,008 |
0,245 ± 0,016 |
0,325 ± 0,016 |
|
Cu |
4,07 ± 1,11 |
4,30 ± 0,86 |
3,71 ± 0,30 |
4,62 ± 0,14 |
|
|
Fe |
40,1 ± 23,1 |
55,9 ± 6,5 |
46,4 ± 1,9 |
54,4 ± 2,2 |
|
|
Pb |
0,77 ± 0,24 |
0,59 ± 0,08 |
0,73 ± 0,02 |
0,56 ± 0,03 |
|
|
Zn |
29,9 ± 7,6 |
21,4 ± 0,6 |
16,9 ± 0,3 |
21,5 ± 0,2 |
|
Примечания:
*Указаны неопределенность аттестованного значения (СО чая) и норматив контроля погрешности аттестованного значения (СО зерна ржи).
**Значение концентрации железа приведено в качестве информационного, так как наблюдаются существенные различия между результатами межлабораторных испытаний.
Как следует из данных табл. 5, в большинстве случаев результаты измерения содержания тяжелых металлов в СО чая и зерен ржи, полученные с использованием различных методик пробоподготовки, близки между собой, для них наблюдается перекрывание доверительных интервалов измерения. Исключение составляют Cu в обоих СО и Fe в СО зерен ржи, но и для этих элементов различия в результатах измерения не превышают погрешности измерения методом ИСП-АЭС (40 и 20 % для Cu и Fe соответственно). При сравнении экспериментально измеренных концентраций элементов с их аттестованными значениями следует учитывать тот факт, что аттестованные значения были получены альтернативными ИСП-АЭС методами: методом инструментального нейтронного активационного анализа (СО чая) и атомно-абсорбционным и колориметрическим методами (СО зерен ржи). Наблюдаемые отклонения измеренных концентраций от аттестованных значений допустимы для межметодных систем измерения концентраций химических элементов [8].
Далее были оценены результаты извлечения тяжелых металлов из различных образцов цветков ромашки с использованием трех методик пробоподготовки (табл. 6).
Таблица 6
Содержание тяжёлых металлов в различных образцах цветков ромашки
|
Элемент |
Методика |
Экспериментальное значение |
||||
|
Красногорск-лексредства |
Микроген |
Парафарм |
Иванчай |
РосБио |
||
|
Cd |
Альтернативная |
0,113 ± 0,003 |
0,093 ± 0,003 |
0,309 ± 0,007 |
0,140 ± 0,003 |
0,193 ± 0,007 |
|
EPA |
0,109 ± 0,002 |
0,100 ± 0,004 |
0,291 ± 0,014 |
0,142 ± 0,004 |
0,227 ± 0,004 |
|
|
EP |
0,090 ± 0,002 |
0,087 ± 0,004 |
0,228 ± 0,008 |
0,109 ± 0,002 |
0,169 ± 0,002 |
|
|
Fe |
Альтернативная |
584,4 ± 16,4 |
167,3 ± 7,8 |
819,6 ± 23,7 |
738,9 ± 3,7 |
79,4 ± 3,3 |
|
EPA |
603,8 ± 13,8 |
197,9 ± 16,0 |
854,0 ± 38,7 |
758,4 ± 5,6 |
86,8 ± 3,7 |
|
|
EP |
449,2 ± 13,2 |
139,2 ± 5,6 |
607,7 ± 53,0 |
561,2 ± 9,4 |
68,0 ± 1,3 |
|
|
Ni |
Альтернативная |
1,81 ± 0,06 |
1,32 ± 0,08 |
2,01 ± 0,06 |
1,99 ± 0,01 |
0,68 ± 0,03 |
|
EPA |
1,83 ± 0,04 |
1,51 ± 0,09 |
2,13 ± 0,05 |
2,04 ± 0,02 |
0,80 ± 0,03 |
|
|
EP |
1,36 ± 0,06 |
0,84 ± 0,02 |
1,38 ± 0,06 |
1,49 ± 0,02 |
0,94 ± 0,05 |
|
|
Zn |
Альтернативная |
27,2 ± 0,5 |
24,7 ± 1,6 |
31,7 ± 1,0 |
25,2 ± 0,6 |
24,3 ± 1,6 |
|
EPA |
29,5 ± 2,7 |
26,5 ± 1,5 |
35,8 ± 7,1 |
25,2 ± 0,5 |
29,0 ± 1,6 |
|
|
EP |
20,4 ± 0,5 |
17,5 ± 0,5 |
22,0 ± 1,3 |
18,8 ± 1,7 |
20,0 ± 0,9 |
|
|
Cu |
Альтернативная |
10,5 ± 0,2 |
7,31 ± 0,15 |
10,0 ± 0,4 |
10,51 ± 0,13 |
4,63 ± 0,16 |
|
EPA |
10,2 ± 0,3 |
8,19 ± 0,38 |
10,7 ± 0,8 |
10,53 ± 0,09 |
5,55 ± 0,15 |
|
|
EP |
7,8 ± 0,4 |
5,14 ± 0,18 |
6,8 ± 0,2 |
7,16 ± 0,08 |
3,55 ± 0,05 |
|
|
Cr |
Альтернативная |
2,04 ± 0,09 |
0,85 ± 0,11 |
2,34 ± 0,08 |
2,91 ± 0,06 |
0,56 ± 0,02 |
|
EPA |
2,00 ± 0,09 |
0,79 ± 0,02 |
2,32 ± 0,02 |
2,94 ± 0,01 |
0,74 ± 0,02 |
|
|
EP |
1,58 ± 0,03 |
0,56 ± 0,02 |
1,81 ± 0,04 |
2,26 ± 0,02 |
0,48 ± 0,51 |
|
Как следует из табл. 6, результаты измерения степени извлечения тяжелых металлов из цветков ромашки тремя методиками пробоподготовки близки в пределах погрешности метода ИСП-АЭС. При этом в большинстве случаев не наблюдается перекрывание доверительных интервалов результатов измерения всех элементов с использованием различных методик пробоподготовки: значения концентраций элементов, полученные по альтернативной методике пробоподготовки, выше полученных по фармакопейной методике, но ниже значений, полученных по методике ЕРА. Возможная причина различий в результатах сравнительного элементного анализа СО чая, зерна ржи и испытуемых образцов ромашки по трем методикам пробоподготовки связана со способом построения градуировочной функции: при элементном анализе СО использовался метод добавок, испытуемых образцов цветков ромашки – метод построения калибровочной кривой. Кроме того, различие в типе растительного сырья также могло оказать влияние на способность извлечения тяжелых металлов по определенной методике. Например, относительная погрешность измерения содержания Cd в рисе, пшенице, кукурузе и соевых бобах составляет 5,7; 22; 40 и 17 % соответственно [8]. Содержание мышьяка, свинца и ртути во всех исследованных образцах было ниже предела количественного определения.
Заключение
Разработана более простая и безопасная по сравнению с используемыми в фармакопейном анализе методика микроволновой минерализации цветков ромашки, основанная на использовании исключительно азотной кислоты. По степени извлечения тяжелых металлов из растительного сырья в раствор она сопоставима с методикой ЕРА. Необходима ее дальнейшая валидация с целью применения при контроле качества растительного сырья.
Библиографическая ссылка
Щукин В.М., Северинова Е.Ю., Кузьмина Н.Е., Яшкир В.А., Меркулов В.А. УСОВЕРШЕНСТВОВАНИЕ МЕТОДИКИ ПРОБОПОДГОТОВКИ ПРИ КОЛИЧЕСТВЕННОМ ОПРЕДЕЛЕНИИ ТЯЖЕЛЫХ МЕТАЛЛОВ В ЦВЕТКАХ РОМАШКИ АПТЕЧНОЙ (MATRICАRIA CHAMOMILLA) МЕТОДОМ ИСП-АЭС // Успехи современного естествознания. 2016. № 6. С. 53-58;URL: https://natural-sciences.ru/en/article/view?id=35965 (дата обращения: 14.05.2026).




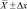 , мг/кг
, мг/кг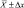 , мг/кг
, мг/кг