Scientific journal
Advances in current natural sciences
ISSN 1681-7494
"Перечень" ВАК
ИФ РИНЦ = 0,976
RESEARCH OF ADSORPTION OF ESTERS OF THE LINEAR STRUCTURE ON THE SURFACE OF GAS COALS
В программном документе «Энергетическая стратегия России на период до 2020 года» предусматривается дальнейшее развитие угольной промышленности и увеличение объемов добычи угля до 430 млн т [3]. Дефицит углей высокой коксуемости, которые применяются в цветной и черной металлургии, производстве искусственных абразивных материалов и в химической промышленности, приводит к увеличению объемов добычи труднообогатимых углей, запасы которых составляют практически половину мировых запасов угля [6]. Однако добываемый уголь во многих случаях не отвечает требованиям потребителей по основным качественным показателям: зольности, влажности, теплотворной способности и спекающим свойствам. Повышение его качества возможно только с применением методов обогащения, совершенствование которых может стать основным направлением развития производственного потенциала угольных бассейнов [3, 6].
В настоящее время единственным эффективным способом обогащения тонких шламов крупностью до «нуля» является пенная флотация [4, 13]. Совершенствование технико-экономических показателей флотации углей во многом определяется применяемым реагентным режимом. Многочисленные исследования флотации труднообогатимых углей направлены на улучшение эффективности и селективности этого процесса благодаря использованию новых реагентных режимов [5]. Одним из наиболее перспективных решений этой задачи является применение реагентов-модификаторов как органического, так и неорганического происхождения, позволяющих увеличить различие в гидратированности поверхности угля и минеральных частиц [2, 8, 9, 10].
Так, применение в качестве реагентов – модификаторов сложных эфиров линейного строения позволяет существенно повысить селективность процесса флотации газовых углей [1, 7, 12]. Причем использование сложных эфиров изомерного строения позволяет более существенно повысить качество концентрата по сравнению со сложными эфирами нормального строения [11, 15].
С целью установления механизма закрепления сложных эфиров линейного строения на поверхности газовых углей были исследованы термодинамические характеристики процесса адсорбции. Изучение адсорбционных свойств сложных эфиров линейного строения проводилось методом газо-адсорбционной хроматографии, которая позволяет не только качественно, но и количественно оценить адсорбцию изучаемых органических соединений на поверхности газовых углей.
Поскольку основными физико-химическими процессами в газо-адсорбционной хроматографии являются процессы сорбции и десорбции, то этот метод позволяет наиболее полно изучить сорбционные процессы, протекающие на границе адсорбат (реагент) – адсорбент (уголь).
Различия в элементном составе, геометрической и электронной структуре молекул органических соединений приводят к их различной сорбируемости угольной поверхностью.
В процессе исследования взаимодействия сложных эфиров линейного строения с поверхностью газового угля были изучены такие важнейшие термодинамические характеристики процесса адсорбции, как изменения свободной энергии (DG), теплоты адсорбции (DН), энтропии (DS), кроме того, были изучены такие параметры, как время удерживания реагента поверхностью угля (τR) и коэффициент асимметрии (ν) (таблица).
Термодинамические характеристики и хроматографические параметры удерживания при адсорбции сложных эфиров на поверхности газового угля
|
Вещество |
– ΔH, кДж/моль |
– ΔG, кДж/моль |
– ΔS, кДж/моль·град |
τR, мин |
ν |
|
Бутилформиат |
26,4 |
8,15 |
0,047 |
2,50 |
4,25 |
|
Изобутилформиат |
23,6 |
5,00 |
0,041 |
1,80 |
2,00 |
|
Бутилбутират |
38,9 |
11,90 |
0,070 |
8,17 |
5,17 |
|
Изобутилбутират |
35,9 |
10,20 |
0,066 |
5,67 |
4,17 |
|
Изобутилизобутират |
35,1 |
9,04 |
0,067 |
3,67 |
3,33 |
|
Изоамилизобутират |
38,2 |
9,17 |
0,075 |
4,33 |
3,67 |
Результаты определения времени удерживания сложных эфиров линейного строения на поверхности газовых углей (таблица) показывает, что с удлинением углеводородного радикала исследуемых соединений величина τR возрастает, что свидетельствует о повышении прочности закрепления. Это связано с увеличением поверхности действия дисперсионных сил углеводородной цепочки. В работе [14] установлено, что время удерживания полярных соединений с увеличением длины углеводородного радикала возрастает не только за счет увеличения дисперсионных сил между углеводородным радикалом и аполярными участками поверхности, но и с повышением специфических сил взаимодействия за счет увеличения электронной плотности на полярном центре. Следует отметить, что наличие изомерии в структуре молекул сложных эфиров линейного строения приводит к снижению величины времени удерживания вследствие уменьшения доли дисперсионных сил взаимодействия углеводородного радикала с угольной поверхностью в силу структурных факторов.
Наблюдаемое при многократном хроматографировании исследованных веществ постоянство времени удерживания для каждого соединения и воспроизводимость величины хроматографического пика указывает на обратимость взаимодействия в системе уголь – реагент. Равенство количества адсорбционного вещества на угле количеству десорбированного вещества, несмотря на разное время удерживания различных соединений, свидетельствует о межмолекулярных взаимодействиях физического характера между поверхностью угля и молекулами реагента.
Важнейшими термодинамическими характеристиками процесса адсорбции молекул органических соединений на угольной поверхности являются изменения свободной энергии (DG), теплоты адсорбции (DН) и энтропии (DS).
По значениям изменений энтальпии (DН) можно судить о прочности и типе связей в системе «адсорбат – адсорбент». Сопоставление термодинамических характеристик процесса адсорбции исследованных соединений газовыми углями, протекающего в условиях изотермического хроматографирования, показывает, что значения изменений энтальпии DН для всех соединений находятся в пределах от – 23,6 до – 38,9 кДж/моль (таблица). Абсолютные значения DН увеличиваются от молекул сложных эфиров с разветвленной цепью к молекулам с прямой цепью, что подтверждает уменьшение прочности закрепления вследствие снижения доли дисперсионных сил взаимодействия углеводородного радикала с угольной поверхностью. Так, например, в ряду бутилбутират – изобутилбутират – изобутилизобутират, характеризующемся увеличением разветвленности углеводородного радикала молекул, наблюдается уменьшение абсолютных значений DН: 38,9 – 35,9 – – 35,1 кДж/моль.
Изменение энергии Гиббса (DG) характеризует способность твердого тела поглощать вещество из окружающей среды. Изменение величины DG от – 5,0 до – 11,9 кДж/моль означает уменьшение запаса свободной энергии угольной поверхности (поверхностной активности) в результате закрепления молекул реагента. Для исследованных соединений наиболее высокие значения DН и DG соответствуют закреплению на поверхности газовых углей сложных эфиров масляной и изомасляной кислоты: бутилбутирата и изоамилизобутирата.
Изменение энтропии (DS) показывает влияние температуры на величину DG и является функцией состояния системы «адсорбат – адсорбент». Отрицательные значения DS в адсорбционном процессе от – 0,041 до – 0,070 кДж/моль·град свидетельствуют об упорядочении системы «уголь – реагент» по мере приближения адсорбата к поверхности и формировании адсорбционного слоя.
Анализ приведенных выше данных показывает, что закрепление молекул сложных эфиров линейного строения на поверхности газовых углей в значительной степени зависит от строения углеводородного радикала исследованных соединений. Так, сложные эфиры изомерного строения характеризуются несколько пониженной адсорбционной способностью и прочностью закрепления на угольной поверхности, это обусловлено, по-видимому, тем, что наличие разветвленности в структуре углеводородного радикала приводит к увеличению расстояния между отдельными атомами молекулы и угольной поверхностью. Кроме того, исследования, проведенные в работе [14], так же показывают, что изомерное строение углеводородных радикалов молекул гетерополярных реагентов снижает величину их адсорбции на угле вследствие уменьшения дисперсионных сил межмолекулярного взаимодействия углеводородного радикала с угольной поверхностью.
С увеличением длины углеводородного радикала внутри гомологического ряда сложных эфиров изомерного строения возрастают значения термодинамических параметров, коэффициенты асимметрии ν хроматографичесого пика, связанного с термодинамическим размыванием зон реагента, а также времени удерживания τR молекул реагентов на сорбционных центрах угольной поверхности, что в целом свидетельствует об увеличении прочности закрепления на углях. Это связано с увеличением поверхности действия дисперсионных сил углеводородной цепочки, обеспечивающей гидрофобизацию угольной поверхности.
Термодинамическое размывание хроматографических зон, на что указывает значение ν > 1 связано с нелинейностью изотермы адсорбции. Экспериментально полученные изотермы адсорбции исследованных соединений имеют характерную выпуклую форму и описываются уравнениями М.М. Дубинина и Л.В. Радушкевича в теории полимолекулярной адсорбции Поляни (рисунок).
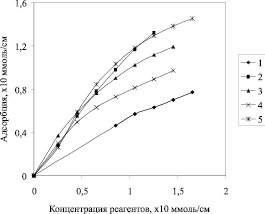
Изотермы адсорбции сложных эфиров на газовом угле: 1 – бутилформиат; 2 – бутилбутират; 3 – изобутилбутират; 4 – изобутилизобутират; 5 – изоамилизобутират
Вид изотермы адсорбции, выражающей зависимость количества поглощенного сорбентом вещества А от его концентрации С, определяется природой адсорбата и адсорбента и характером взаимодействия молекул друг с другом и с твердой поверхностью. Изотерма адсорбции однозначно связана с формой хроматографического пика адсорбируемого вещества.
Все исследуемые вещества имеют выпуклую изотерму адсорбции (рисунок), для которой производная dA/dC c ростом концентрации уменьшается, и скорость движения по адсорбенту малых концентраций веществ будет меньше, чем больших. Это приводит к искажению формы хроматографического пика – восходящая ветвь обостряется, а нисходящая растягивается.
Такая картина наблюдается, как правило, при адсорбции на неоднородной поверхности со сравнительно малым числом высокоактивных сорбционных центров. Основное количество адсорбата закрепляется на менее активных центрах и выходит из колонки с более высокими скоростями, что и определяет крутую восходящую ветвь пика. Десорбция с высокоактивных сорбционных центров происходит медленнее, что приводит к растягиванию нисходящей границы хроматограммы.
Экспериментально полученные изотермы адсорбции сложных эфиров линейного строения (рисунок) имеют характерную выпуклую форму, характеризующую локализованную адсорбцию за счет межмолекулярных сил нехимической природы.
Изотермы реагентов с нормальным строением молекул располагаются выше и величина адсорбции больше, чем у соответствующих структурных изомеров, что указывает на более низкую сорбционную способность веществ с разветвленным строением молекул. Это подтверждается и меньшими величинами времени их удерживания на поверхности газовых углей (таблица). Меньшая прочность закрепления разветвленных молекул обусловлена влиянием структурного фактора, т.к. энергия специфического взаимодействия зависит от расстояния между поверхностью адсорбента и силовыми центрами звеньев адсорбированной молекулы.
Кроме того, следует отметить, что наличие алкильных радикалов приводит к увеличению в структуре молекулы центров с локально сконцентрированными отрицательными и положительными зарядами вследствие смещения электронной плотности + I-типа от метильных групп к углеродным атомам главной цепи, что в свою очередь приводит к некоторому увеличению специфического взаимодействия между молекулами реагентов и угольной поверхностью.
Наличие изомерии в структуре молекул сложных эфиров линейного строения приводит к снижению их адсорбционных способностей вследствие уменьшения дисперсионных сил взаимодействия углеводородного радикала с угольной поверхностью. Однако дисперсионные силы проявляются между адсорбентом и адсорбатом независимо от их природы и строения и относятся к неспецифическому взаимодействию.
Таким образом, снижение доли неспецифического взаимодействия между молекулами изомерного строения и поверхностью газовых углей приводит к повышению избирательности их закрепления и, как следствие, увеличению селективности процесса флотации углей.
Библиографическая ссылка
Муллина Э.Р., Мишурина О.А. ИССЛЕДОВАНИЕ АДСОРБЦИИ СЛОЖНЫХ ЭФИРОВ ЛИНЕЙНОГО СТРОЕНИЯ НА ПОВЕРХНОСТИ ГАЗОВЫХ УГЛЕЙ // Успехи современного естествознания. 2016. № 12-1. С. 26-30;URL: https://natural-sciences.ru/en/article/view?id=36255 (дата обращения: 07.05.2026).



