Scientific journal
Advances in current natural sciences
ISSN 1681-7494
"Перечень" ВАК
ИФ РИНЦ = 0,976
THE OBTAINING OF INTERMETALLIC COMPOUNDS OF HOLMIUM BY ELECTROLYSIS OF MOLTEN ENVIRONMENTS
Магнитные материалы на основе редкоземельных металлов (РЗМ) и металлов триады железа используются для производства постоянных магнитов различного назначения. В последнее время все чаще встает вопрос о направленном синтезе магнитотвердых материалов на основе РЗМ. Однако теоретические основы и принципы разработки таких материалов пока еще отсутствуют, и необходимые данные можно получить, лишь экспериментально изучив характер взаимодействия металлов триады железа с редкоземельными металлами, особенно в областях интерметаллических соединений состава 2:17 и 1:5 [1].
Интерметаллические соединения на основе РЗМ и металлов группы железа можно синтезировать различными методами (СВС, жидкостного бестокового насыщения, контактного обмена, твердофазный синтез, гидридно-кальциевого восстановления и т.д.) [2].
Известен способ получения интерметаллидов гольмия и никеля путем диффузионного насыщения никелевого электрода ионами гольмия в расплаве в KCl-HoCl3 [8-9]. Также авторами [3] исследовано получение интерметаллидов гольмия и никеля диффузионным насыщением металлического никеля гольмием в расплаве KCl-NaCl.
В работе [4] представлены исследования влияний немагнитных и магнитных металлов (Fe, Co) на магнитные свойства гольмия в широком интервале температур, охватывающее твердое состояние, фазовые переходы и жидкое состояние образующих соединений гольмия с индием, кобальтом и железом. Также в работе приводится получение соединений Ho-Co и Ho-Fe сплавлением чистых металлов.
Авторами [5–7] исследовано формирование наноструктурных и интерметаллидных фаз в сплавах систем редкоземельных металлов с 3р-металлами. Показано влияние атомных факторов металлов на состав наноструктур и интерметаллических соединений в системах РЗМ-3р-металл.
Интерметаллические соединения на основе РЗМ и металлов группы железа в настоящее время получают различными методами, обзор которых дан в [2]. Эти методы, также применяемые для получения сплавов, относятся к области металлургии, а не препаративной химии. Это – выплавка в дуговых и индукционных печах, алюминотермическое восстановление кислородных и галоидных соединений, электролитическое выделение кристаллов интерметаллидов из расплавов, гидридно-кальциевое восстановление и др.
Для получения чистых интерметаллидов РЗМ и выделения фаз, получение которых путем прямого сплавления затруднено, можно использовать электролиз расплавленных сред.
Цель работы: разработка электрохимического способа получения порошков интерметаллидов гольмия с металлами триады железа и алюминием в галогенидных расплавах.
Высокотемпературный электрохимический синтез интерметаллидов гольмия с металлами триады железа и алюминия осуществляли в гальваностатическом режиме в расплаве KCl-NaCl-HoCl3-NiCl2 (СoCl2), KCl-NaCl-HoCl3 с растворимым железным анодом, KCl-NaCl-CsCl-HoCl3 с растворимым алюминиевым анодом. Для проведения электролиза в гальваностатическом режиме использовался источник постоянного тока ТЭК-14.
Идентификация полученных образцов проводилась рентгенофазовым методом на рентгеновских дифрактометрах ДРОН-6 (НПП «Буревестник», Россия, Санкт-Петербург) и D2 Phazer (Германия);
Источником ионов гольмия служил безводный хлорид гольмия (III) (99,99 %). Все операции взвешивания безводных хлоридов проводили в перчаточном боксе MbraunLabStar. Обезвоживание шестиводного хлорида никеля (кобальта) NiCl2· 6H2O (СоCl2· 6H2О) до чистого безводного хлорида проводилось с помощью тетрахлорида углерода по общеизвестной методике.
Электрохимический синтез порошков интерметаллидов гольмия и никеля (кобальта) в хлоридных расплавах
В основу электрохимического синтеза интерметаллидов гольмия с металлами триады железа и алюминия положены процессы совместного их электровыделения на катоде из хлоридных расплавов и последующего взаимодействия на атомарном уровне с образованием ультра- и субмикродисперсных порошков различных по составу интерметаллических соединений.
Электросинтез проводили в высокотемпературной кварцевой ячейке в атмосфере инертного газа – аргона при температуре 973 К. Катодом служил вольфрамовый стержень высокой чистоты диаметром 3,0 мм. Анодом и одновременно контейнером для расплава служил стеклоуглеродный тигель с алундовой подложкой.
При электролизе расплавленной смеси KCl–NaCl, содержащей трихлорид гольмия (0,5÷2,5 мол. %) и дихлорид никеля (кобальта) (0,1÷2,5 мол. %) при плотности тока 0,5÷2,0 А/см2 и продолжительности электролиза 60 мин, на вольфрамовом электроде образуется катодный осадок в виде «металло-солевой груши». Получившийся продукт в большинстве случаев не удерживается на катоде, и поэтому под катодом устанавливаем алундовый тигель для сборки осыпавшегося с катода осадка.
Выщелачивание катодного осадка в горячей дистиллированной воде позволяло отделить целевой продукт от солевой фазы. После многократной промывки в дистиллированной воде целевой продукт отделяли от раствора магнитной сепарацией. Полученный осадок сушили в вакуумном сушильном шкафу при температурах 373–423 К. Фазовый состав катодного осадка представлен на рис. 1–2. В зависимости от состава электролизной ванны и параметров электролиза получались смесь фаз металлического никеля (кобальта), интерметаллидов HoNi, HoNi5, HoNi3 (HоСо2, HoСо3, HoСо5, Ho2Со17) и металлического гольмия.
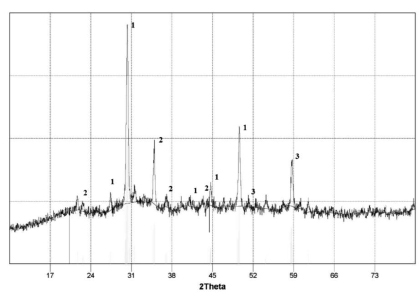
Рис. 1. Рентгенограмма продукта гальваностатического электролиза, полученного из эквимольного расплава KCl-NaCl, содержащего HoCl32,5 мол. % и NiCl2 0,5 мол. % на вольфрамовом электроде. ik = 1,2 А/см2. Т = 973 К. S = 2,43 см2. Стандартные линии: 1 – HoNi, 2 – HoNi5, 3 – HoNi3
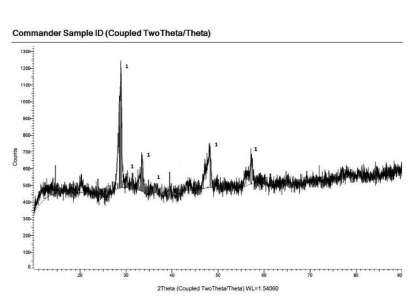
Рис. 2. Рентгенограмма продукта гальваностатического электролиза, полученного из эквимольного расплава KCl-NaCl, содержащего HoCl31,5 мол. % и СоCl2 0,5 мол. % на вольфрамовом электроде. ik = 1,2 А/см2. Т = 973 К. S = 2,43 см2. Стандартные линии: 1 – Co7Ho12
При постоянной плотности тока (1,2 А/см2) содержание интерметаллидов увеличивается как при увеличении концентрации хлорида гольмия в расплаве, так и при увеличении соотношения концентраций хлоридов гольмия и никеля. Когда соотношение концентраций [HoCl3]:[NiCl2] = 1:1, в катодном осадке превалирует фаза металлического никеля. С увеличением этого соотношения доля металлического никеля уменьшается, а содержание интерметаллидов HoNi, HoNi3, HoNi5 возрастает. При условии [HoCl3]:[NiCl2] > 5 в катодном осадке фаза металлического никеля не обнаруживается, а образуется смесь фаз интерметаллидов. Причем фаза с большим содержанием гольмия превалирует. При соотношении концентраций [HoCl3]:[CoCl2] = 1:1 наблюдается аналогичная картина. Увеличение концентрации хлорида гольмия приводит к образованию интерметаллидов и исчезновению фазы металлического кобальта. При условии [HoCl3]:[СоCl2] = 3:1 целевой продукт состоит только из одной фазы Co7Ho12. При концентрациях хлорида гольмия 2,0–2,5 мол. % образуется смесь фаз интерметаллидов гольмия и кобальта.
Электрохимический синтез порошков интерметаллидов гольмия и железа (алюминия) из галогенидных расплавов
Высокотемпературный электрохимический синтез интерметаллидов Ho-Fe и Ho-Al проводили в гальваностатическом режиме в расплаве KCl-NaCl-HoCl3и KCl-NaCl-CsCl-HoCl3 с концентрациями хлорида гольмия 0,5÷3,0 мол. %. Ионы железа и алюминия в расплав вводили анодным растворением металлического железа в виде пластинки и алюминия в виде стержня. Начальная катодная плотность тока менялась в интервале 2,0–4,0А/см2. При гальваностатическом электролизе истинное значение плотности тока известно только в начальный период времени, т.к. в ходе электролиза существенно меняется площадь катода вследствие образования «металло-солевой груши». Но однозначно можно сказать, что с увеличением плотности тока увеличивается дисперсность порошка. Оптимальная продолжительность электролиза 60 мин, температура 973 К.
Фазовый состав полученных в чистом виде порошков интерметаллидов гольмия с железом и гольмия с алюминием определяли рентгенофазовым анализом. Рентгенограммы полученных образцов приведены на рис. 3–4.
Рис. 3. Рентгенограмма продукта гальваностатического электролиза, полученная из расплава KCl-NaCl-НоСl3 на вольфрамовой электроде с растворимым железным анодом. С (НоСl3) = 1,5 мол. %. ik = 2,0 А/см2. Т = 973 К. S = 1,5 см2. Стандартные линии: 1 – HoFe5; 2 – HoFe2
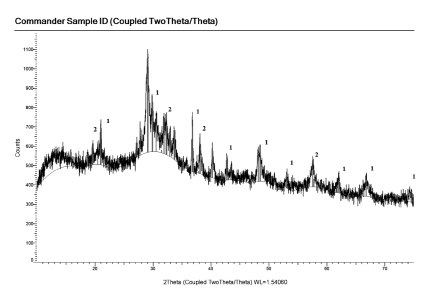
Рис. 4. Рентгенограмма продукта гальваностатического электролиза, полученная из расплава KCl-NaCl-CsCl -НоСl3 на вольфрамовом электроде с растворимым алюминиевым анодом. С (НоСl3) = 1,0 мол. %. ik = 2,0 А/см2. Т = 823 К. S = 1,5 см2. Стандартные линии: 1 – HoAl3; 2 – HoAl2
Эти результаты свидетельствуют о принципиальной возможности электросинтеза интерметаллидов гольмия с железом и алюминием анодным растворением металлического железа и алюминия.
Выводы
1. Показана принципиальная возможность получения интерметаллических соединений гольмия с никелем (кобальтом, железом, алюминием) электролизом из галогенидных расплавов.
2. Рентгенофазовым анализом продуктов гальваностатического электролиза хлоридных расплавов содержащих ионы гольмия и никеля (кобальта) подтверждают образование интерметаллидов гольмия с никелем (HoNi, HoNi5, HoNi3) и гольмия с кобальтом HoСо5, HoСо3, Но2Со17.
3. Показана возможность получения интерметаллических соединений гольмия с железом и гольмия с алюминием анодным растворением железа и алюминия в хлоридных расплавах.
4. Рентгенофазовый анализ полученных образцов интерметаллидов Ho-Fe и Ho-Al показал наличие фаз: HoFe2, HoFe5 и НоAl3, НоAl2, НоAl соответственно.
Библиографическая ссылка
Кушхов Х.Б., Карданова Р.А., Кяров А.А., Маргушева М.М., Маргушева Х.М., Борукаева И.А. ПОЛУЧЕНИЕ ИНТЕРМЕТАЛЛИДОВ ГОЛЬМИЯ ЭЛЕКТРОЛИЗОМ РАСПЛАВЛЕННЫХ СРЕД // Успехи современного естествознания. 2017. № 4. С. 30-34;URL: https://natural-sciences.ru/en/article/view?id=36430 (дата обращения: 16.05.2026).



