Scientific journal
Advances in current natural sciences
ISSN 1681-7494
"Перечень" ВАК
ИФ РИНЦ = 0,976
DEFINITION OF DIFFUSION COEFFICIENTS AND DIMENSIONS OF PARTICLES IN RESTORED DAIRY MIXTURES
Грудное молоко (ГМ) – это полидисперсная многофазная система, включающая в себя молекулярные ионизированные растворы сывороточных белков, тонкую коллоидную систему казеиновых частиц, дисперсную систему молочного жира, минеральные соли и т.д. [1]. Основной принцип создания адаптированных смесей – максимальное приближение коровьего молока к составу и свойствам женского молока и их соответствие особенностям пищеварения и метаболизма ребенка первого года жизни [2]. Предварительная переработка коровьего молока для приготовления адаптированных молочных смесей (МС) приводит к изменению нативного состава молока, в котором основные минеральные компоненты связаны с исходными белками молока и представлены в форме различных коллоидно-дисперсных систем [3]. Получаемая МС представляет собой полидисперсную систему, которая при восстановлении должна образовывать коллоидные дисперсные системы (КДС), которые аналогичны системам ГМ. А именно: фазу истинного раствора (вещества находятся в ионно-молекулярном состоянии), коллоидную фазу (вещества представлены в виде коллоидных частиц – фосфат кальция, белки, а также казеинкальцийфосфатный комплекс – ККФК) и фазу эмульсии (вещества представлены грубодисперсными частицами различной величины в присутствии стабилизаторов, обычно лецитинов). Наибольшую роль в усвоении минеральных веществ играет коллоидная фаза, включение в которую минеральных веществ способствует их лучшему усвоению [3]. Корректировку минерального состава МС проводят в два этапа. На первом этапе снижают общее содержание минеральных веществ путем диафильтрации концентратов сывороточных белков. При этом в равной степени удаляются ионизированные и неионизированные компоненты, в том числе и коллоидный фосфат кальция. На втором этапе минеральный состав восполняют в соответствии с потребностями новорожденных, добавляя недостающие количества ионов калия, натрия, кальция, магния, меди, железа и т.п. в виде цитратов, фосфатов, сульфатов, карбонатов, хлоридов этих металлов [1, 2]. Включение минерального премикса осуществляется на последнем этапе путем смешивания сухих минеральных веществ с готовой сухой молочной смесью. Образование КДС тем или иным способом произойдет только в процессе восстановления молочной смеси. Фосфат кальция малорастворим в воде и в молоке образует типичную неустойчивую коллоидную систему с гидрофобной дисперсной фазой [3]. Его растворимость повышается под влиянием казеина. Мицеллы казеина представляют собой коллоидную фазу смешанного состава, обладающую свойствами гидрофильного и гидрофобного золя. Нахождение казеина и фосфатов кальция и магния в восстановленной МС в виде сложных мицелл имеет большое значение для новорожденного [3]. Так, под действием химозина в его желудке мицеллярный белок легко образует сгусток, который подвергается дальнейшему воздействию пепсина [4]. Кроме того, в составе растворимых мицелл казеина транспортируются очень важные для молодого организма соли кальция и магния. Важен размер частиц вновь образованного, при восстановлении молочной смеси, коллоидного фосфата кальция и магния в комплексе с белками.
Цель исследования – с помощью измеренных коэффициентов проницаемости частиц, содержащих ионы магния и кальция в мембранах из ацетата целлюлозы, оценить коэффициенты диффузии и размеры кальций- и магнийсодержащих частиц диффузанта, восстановленных МС различного состава, ГМ и модельного раствора.
Материалы и методы исследования
Для диффузии использовалась специальная установка с мембранным фильтром из ацетата целлюлозы с диаметром пор 0,45 мкм и фильтром с диаметром пор 4 ± 1 мкм. Для оценки скорости диффузии были взяты четыре типа адаптированных МС: МС1 – нейтральная, МС2 – кисломолочная, МС3 – с пребиотиками, МС4-антирефлюксная от известных производителей. 4,3 г (порционная ложка) молочной смеси разводили в 100 мл теплой дистиллированной воды, охлаждали и помещали во внешний сосуд установки для диффузии. Во внутренний сосуд заливали дистиллированную воду (рис. 1). После 20 ч с мембранным фильтром из ацетата целлюлозы или 1,5 ч в случае с фильтром с диаметром пор 4 ± 1 мкм определялось содержание ионов во внутреннем сосуде. Концентрация ионов кальция и магния определялась титриметрическим методом, содержание фосфатов – спектрофотометрическим методом (спектрофотометр «LEKI SS2109UV»). Динамическую вязкость рассчитывали по скорости ламинарного течения жидкости в тонком капилляре. Для измерения буферной емкости МС по кислоте использовали потенциометрический метод измерения рН восстановленной смеси до и после добавления 1 мл 0,1 н НСl. Статистическая обработка результатов исследования выполнена при достоверности (p ≤ 0,05).
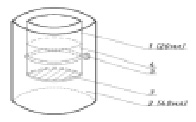
Рис. 1. Установка для оценки скорости диффузии ионов: 1 – камера выявления с дистиллированной водой; 2 – камера для образца МС; 3 – мембрана; 4 – лавсановый материал; 5 – хомутик
Результаты исследования и их обсуждение
Большинство добавляемых минеральных компонентов премикса нерастворимо в воде (карбонат кальция, фосфаты кальция и магния, марганца и др.), поэтому возникает проблема с биодоступностью указанных минеральных компонентов. Формирование КДС возможно как путем измельчения дисперсной фазы в дисперсионной среде (дисперсионный метод), так и укрупнения микрокристаллов за счет веществ, находящихся в фазе истинного раствора (конденсационный метод). С учетом того, что при изготовлении МС необходима высокая гомогенизация компонентов для их лучшего усвоения, формирование дисперсной фазы (мицелл коллоидов) осуществляют конденсационным методом. При этом должны достраиваться имеющиеся микрокристаллы нерастворимых карбонатов, фосфатов, цитратов кальция и магния молекулами белков с образованием аморфных коллоидных частиц.
Для восстановленных МС были измерены физико-химические показатели, косвенно влияющие на способность МС к пассивной диффузии. Это вязкость, рН, буферная емкость по кислоте и осмоляльность. Буферная емкость зависит от концентрации белков, цитратов, фосфатов и минералов. Более высокая в 2–4 раза буферная емкость МС обусловлена более высоким содержанием этих компонентов по отношению к грудному молоку [5]. Осмоляльность характеризует общую минерализацию смеси и не должна превышать осмоляльность грудного молока 280–300 мОсм/кг [6]. При такой осмоляльности заменителей достигается нормальная водно-солевая нагрузка на выделительную систему ребенка. Выбранные для исследования МС являются гипотоничными по отношению к грудному молоку. Осмотическое давление – это свойство коллигативное, зависящее при постоянной температуре только от числа частиц в объеме, меньшее его значение указывает на больший размер частиц и, следовательно, их меньшее количество.
Для МС была измерена скорость пассивной диффузии через мембраны с различным диаметром пор (табл. 2). Увеличение диаметра пор в 10 раз приводит к увеличению скорости диффузии ионов кальция в 8–10 раз, магния в 25–40 раз, а фосфора в 1,5–5 раз.
Таблица 1
Физико-химические свойства МС и ГМ
|
МС/ГМ |
рН |
Вк, ммоль/л |
Вязкость, мПа.с |
Осмоляльность, мОсм/кг |
|
МС1 |
7,19 ± 0,05 |
6,06 ± 0,05 |
1,33 ± 0,01 |
207 |
|
МС2 |
6,05 ± 0,05 |
9,01 ± 0,05 |
1,16 ± 0,01 |
213 |
|
МС3 |
7,12 ± 0,05 |
7,09 ± 0,05 |
2,77 ± 0,01 |
279 |
|
МС4 |
6,70 ± 0,05 |
18,52 ± 0,05 |
27,67 ± 0,01 |
231 |
|
ГМ1 |
6,63 ± 0,05 |
3,88 ± 0,05 |
1,82 |
277 |
|
ГМ2 |
6,92 ± 0,05 |
4,27 ± 0,05 |
1,77 |
282 |
|
ГМ3 |
7,05 ± 0,05 |
4,63 ± 0,05 |
1,86 |
291 |
Таблица 2
Скорость пассивной диффузии элементов через мембраны с диаметром (d) пор 0,45 мкм (*) и 4 ± 1 мкм (**)
|
Скорость диффузии, пкг/с |
||||
|
МС |
d, пор |
Са |
Мg |
Р |
|
МС1 |
* |
4,2 ± 0,1 |
1,1 ± 0,1 |
1,0 ± 0,1 |
|
** |
42,6 ± 0,1 |
41,1 ± 0,1 |
5,0 ± 0,1 |
|
|
МС2 |
* |
3,5 ± 0,1 |
1,4 ± 0,1 |
1,3 ± 0,1 |
|
** |
40,7 ± 0,1 |
31,1 ± 0,1 |
1,6 ± 0,1 |
|
|
МС3 |
* |
3,5 ± 0,1 |
1,0 ± 0,1 |
1,1 ± 0,1 |
|
** |
33,3 ± 0,1 |
41,4 ± 0,1 |
2,2 ± 0,1 |
|
|
МС4 |
* |
3,2 ± 0,1 |
0,8 ± 0,1 |
0,0 ± 0,0 |
|
** |
24,1 ± 0,1 |
18,9 ± 0,12 |
1,2 ± 0,1 |
|
|
ГМ (среднее) |
* |
3,4 ± 0,1 |
0,9 ± 0,1 |
- |
При этом диффузия компонентов МС обусловлена не только пассивным транспортом веществ, находящихся в ионно-молекулярной фазе с минимальными размерами частиц дисперсной фазы, но и за счет диффузии коллоидных частиц. В коллоидно-дисперсном состоянии в молоке находятся сывороточные белки, казеин и большая часть фосфатов кальция. Размеры коллоидных частиц коровьего молока согласно литературным данным составляют (в нм): β-лактоглобулина – 25–50, α-лактоальбумина – 15–20, мицелл казеина 40–300, фосфата кальция – 10–20 [3]. Коллоидная фаза МС изучена мало, но можно проэкстраполировать, что КДС МС представлена аналогичными дисперсными системами. Значительное изменение светопропускания раствора диффузата МС в мембрану с большим диаметром пор, измеренное при различных длинах волн, свидетельствует о пассивном транспорте гидрофильных КДС с небольшой молекулярной массой. Светопропускание МС3 (с пребиотиками) и МС4 (антирефлюксной) характеризуется большими значениями (рис. 2).
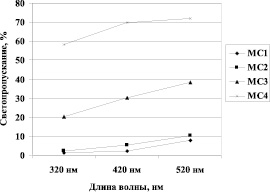
Рис. 2. Светопропускание раствора диффузата восстановленных МС
По вычисленной скорости диффузии были определены коэффициенты проницаемости частиц в мембранах, содержащие ионы кальция и магния. Для описания явлений переноса через биологические мембраны используется уравнение Коллендера – Бернульда dm/dt = –PS(C1 – C2), где Р – коэффициент проницаемости, аналогичный коэффициенту диффузии D. Коэффициент проницаемости в отличие от коэффициента диффузии зависит не только от температуры и природы вещества, но еще и от свойств мембраны и ее функционального состояния. Коэффициенты проницаемости ионов из восстановленных МС и исследуемых проб ГМ представлены в табл. 3.
Таблица 3
Коэффициенты проницаемости ионов из МС и ГМ мембрана 0,45 мкм
|
МС, ГМ |
МС1 |
МС2 |
МС3 |
МС4 |
ГМ1 |
ГМ2 |
ГМ3 |
|
Р Са, нм/с |
29,6 ± 0,1 |
34,8 ± 0,1 |
33,9 ± 0,1 |
21,9 ± 0,1 |
55,7 ± 0,1 |
78,5 ± 0,1 |
55,4 ± 0,1 |
|
Р Mg,нм/с |
46,1 ± 0,1 |
42,3 ± 0,1 |
40,8 ± 0,1 |
50,0 ± 0,1 |
164,0 ± 0,1 |
171,6 ± 0,1 |
150,8 ± 0,1 |
Средний коэффициент проницаемости для МС РСа = 30,1 ± 0,1 нм/с, РMg = 44,8 ± 0,1 нм/с, для ГМ РСа = 62,2 ± ± 0,1 нм/с, РMg = 162,1 ± 0,1 нм/с. Коэффициенты проницаемости для мембраны с диаметром пор 4 ± 1 мкм были в среднем в 10–20 раз больше. Для оценки размеров диффундирующих частиц были взяты результаты диффузии ионов кальция через мембрану с диаметром пор 0,45 мкм. Для биологических мембран связь коэффициента проницаемости с коэффициентов диффузии выражается по уравнению
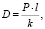
где D – коэффициент диффузии в м2/с, Р – коэффициент проницаемости в м/с, l – толщина мембраны в м, k = С1/С2 – распределение, характеризующее соотношение равновесных концентраций диффундирующего вещества в мембране и в окружающей растворе. Так как измерить концентрацию вещества в мембране не представляется возможным, условно при расчетах за нее была взята концентрация вещества во внутреннем сосуде после диффузии. Рассчитанные коэффициенты диффузии были использованы для оценки размеров продиффундировавших частиц по уравнению Стокса – Эйнштейна:
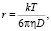
где k – постоянная Планка, η – вязкость в Па.с, D – коэффициент диффузии в м2/с, r – размер частиц в м.
При восстановлении МС важно учитывать сформированность коллоидного комплекса фосфата кальция (магния) с белками, так как от этого будет зависеть степень усвоения кальция и фосфора. Рассчитанные значения размеров частиц, содержащих кальций и магний, диффундирующих через мембрану из ацетата целлюлозы, представлены в табл. 4.
Таблице 4
Размеры частиц диффузатов, содержащих кальций и магний
|
ион |
МС, ГМ |
МС1 |
МС2 |
МС3 |
МС4 |
ГМ, среднее |
модел. р-р |
|
Са |
D. 10-11, м2/с |
6,83 ± 0,01 |
6,84 ± 0,01 |
11,56 ± 0,01 |
6,72 ± 0,01 |
6,81 ± 0,01 |
10,61 ± 0,01 |
|
r . 10-9, м |
2,40 ± 0,01 |
2,75 ± 0,01 |
0,68 ± 0,01 |
0,12 ± 0,01 |
1,77 ± 0,01 |
0,002 ± 0,0001 |
|
|
Мg |
D. 10-11, м2/с |
7,06 ± 0,01 |
6,97 ± 0,01 |
13,45 ± 0,01 |
7,06 ± 0,01 |
8,88 ± 0,01 |
14,35 ± 0,01 |
|
r . 10-9,м |
2,32 ± 0,01 |
2,70 ± 0,01 |
0,59 ± 0,01 |
0,117 ± 0,01 |
1,35 ± 0,01 |
0,001 ± 0,0001 |
Для оценки точности расчетов коэффициентов диффузии была изучена диффузия ионов модельного раствора в мембране из ацетата целлюлозы. Был приготовлен модельный раствор, содержащий ионы калия, натрия, магния и кальция в том же соотношении, что и в МС2. Раствор был помещен во внешний сосуд установки для диффузии. Рассчитанный коэффициент диффузии для иона кальция из модельного раствора составил 1,06 ± 0,01.10-10 м2/с, для иона магния 1,43 ± 0,01•10-10 м2/с, что сопоставимо с литературными данными 7,9•10-10м2/с и 7,1•10-10м2/с [7, с. 144]. Рассчитанные размеры продиффундировавших частиц 2,04 ± 0,01. 10-12 м 1,52 ± 0,01. 10-12 м свидетельствуют о том, что кальций находится в ионной фазе. Размеры частиц, содержащих кальций и магний, продиффундировавших из ГМ и МС, имеют порядок 10-9 м, частицы находятся в коллоидной фазе, об этом свидетельствуют меньшие по сравнению с истинным раствором коэффициенты диффузии порядка 10-11 м2/с. Что также хорошо согласуется с литературными данными, для коллоидов коэффициенты диффузии имеют порядок 10-14–10-11м2/с. МС3 и МС4 согласно данным табл. 4 характеризуются меньшими размерами частиц, диффундировавших в мембрану. Это подтверждается данными спектрофотометрического анализа (рис. 2). Данные МС дают более высокие значения светопропускания растворов из камеры выявления установки для диффузии.
Выводы
1. Рассчитаны скорости диффузии в мембранах с различным диаметром пор, коэффициенты проницаемости и определены коэффициенты диффузии в мембране из ацетата целлюлозы. Оценены размеры кальций- и магнийсодержащих частиц диффузанта, восстановленных МС для детского питания от различных производителей, ГМ и модельного раствора по минеральному составу идентичному по макрокомпонентам одной из исследуемых МС.
2. Коэффициенты диффузии и размеры кальций- и магнийсодержащих частиц диффузанта грудного молока и молочных смесей соответствуют коллоидной степени дисперсности.
Библиографическая ссылка
Ермишина Е.Ю., Белоконова Н.А., Наронова Н.А., Бородулина Т.В. ОПРЕДЕЛЕНИЕ КОЭФФИЦИЕНТОВ ДИФФУЗИИ И РАЗМЕРОВ ЧАСТИЦ В ВОССТАНОВЛЕННЫХ МОЛОЧНЫХ СМЕСЯХ // Успехи современного естествознания. 2018. № 4. С. 23-28;URL: https://natural-sciences.ru/en/article/view?id=36720 (дата обращения: 16.05.2026).



