Scientific journal
Advances in current natural sciences
ISSN 1681-7494
"Перечень" ВАК
ИФ РИНЦ = 0,976
HYDROCHEMISTRY OF THE IRIMNOYE LAKE
Озеро Иримное (народное название Арынное) – типичный водоём замкнутого типа. Озеро входит в пойменно-русловой комплекс нижнего течения реки Иртыш, территориально находится в Уватском районе Тюменской области. Географически озеро расположено на левобережной пойме Иртыша – 58.735380 с.ш., 68.679617 в.д., в отдалении от меженного русла реки на несколько сотен метров (рис. 1). Общая площадь водного зеркала озера составляет 13 га, протяженность водоёма не превышает 2 км, средняя глубина около 1 м, максимальная – до 4 м. В годы высокого паводка озеро соединяется с руслом Иртыша [1]. Питание озера осуществляется за счет атмосферных осадков и подземного стока. Литературных источников о гидрохимических данных воды озера Иримное, полученных в более ранние годы, не обнаружено. Найдены работы по изучению таксономического состава рыбного населения озера, его распределения по площади и глубине озера [1].
Цель исследования: изучение гидрохимических характеристик поверхностной воды в озере Иримное.
Материалы и методы исследования
Полевые исследования на озере Иримное проведены в течение 2008 г. – в январе, феврале и с мая по октябрь. Координаты точек отбора проб воды: 1 – N 58.736888, E 68.672911; 2 – N 58.735359, E 68.678747; 3 – N 58.734746, E 68.685356 (рисунок). Отбор проб воды с глубины 0,3 и 1 м на озере Иримное осуществлялся по ГОСТ Р 51592–2000.
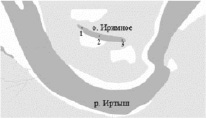
Схема расположения озера Иримное
Из гидрохимических показателей качества поверхностных вод были определены температура, рН, О2, окисляемость перманганатная, Feобщее, CI-, SO42-, NH4+, NO2-, NO3-, жесткость, Ca2+, Mg2+. Исследование ионного состава воды проводилось по общепринятым методикам измерений в аккредитованной лаборатории «Экотоксикология» Тобольской биологической станции Российской академии наук [2]. Измерения рН и температуры воды проведены на анализаторе АНИОН-7050, содержание Feобщее, SO42-, NH4+, NO2- и NO3- на спектрофотометре UNICO-1200. Статистическая обработка экспериментальных данных осуществлена в программе Microsoft Excel с применением коэффициента корреляции Спирмена rs (p < 0,05).
Результаты исследования и их обсуждение
Результаты исследований гидрохимических показателей озера Иримное приведены в табл. 1 и 2. В исследуемый период минимальная температура воды в озере наблюдалась в феврале – минус 0,8 °С на глубине ниже 0,8 м. Максимум температуры воды в поверхностном слое до 0,3 м наступает в июне – 25,7 °С. Изменение вертикального распределения температуры водной толщи составило от 0,1 до 5,6 °С. В сентябре – октябре выявлена разница в 4–5,6 °С между температурами воды в поверхностном слое до 0,3 м и глубиной более 1 м. Верхние слои воды в первую очередь подвержены влиянию внешних факторов (взаимодействию с атмосферой, сгонно-нагонным явлениям), т.е. быстрее охлаждаются в осенний период [3]. Водородный показатель воды в озере нестабилен в течение всего периода исследований. Воду озера Иримное по среднему значению рН, равному 7,6 по вертикали, можно отнести к слабощелочным водам, имеющим диапазон 7,5 … 8,5 единиц рН; по медиане, соответствующей 7,3 единицы рН – к нейтральным водам.
Значения рН воды в озере варьировали от слабокислой реакции (6,5) до сильнощелочной (>9,5). В зимние месяцы (январь, февраль) вода имела нейтральную реакцию. В осенний (сентябрь, октябрь) период в воде наблюдалась слабощелочная реакция, в весенние и летние месяцы – от слабокислой до сильнощелочной. Расчет значений коэффициента корреляции Спирмена между значениями рН и концентрациями магния (и жесткости) выявил сильные статистически значимые прямые связи между ними (табл. 3). В августе 2008 г. вода в озере имела сильнощелочную реакцию, при максимальном значении концентрации магния и увеличении жесткости до 5,1 °Ж. В целом по величине общей жесткости вода относится к мягкой (до 2 °Ж). Средние обратные связи обнаружены между значениями рН и концентрациями железа и окисляемости перманганатной (rs = –0,3 и –0,5) (табл. 3).
Концентрация железа в летние месяцы достигает 1 мг/л, зимой увеличивается до 3,9 мг/л. Данные значения согласуются с данными, полученными для озер Тюменской области [4]. При повышении содержания железа в воде увеличивается окисляемость перманганатная (rs = 0,9). Значение перманганатной окисляемости воды в зимние месяцы – январь и февраль – в среднем составило 20,7 мгО/дм3, и содержание железа в этот период было максимально – в среднем – 2,6 мг/дм3. Высокое значение перманганатной окисляемости воды свидетельствует о том, что в воде озера железо присутствует в большей степени в виде двухвалентного иона Fe (II). Он может окисляться до Fe (III) и выпадать в виде осадка гидроксида железа Fe(OH)3 при низком содержании органических и минеральных веществ, удерживающих преобразование железа из одной формы в другую [5].
Таблица 1
Гидрохимические показатели воды в озере Иримное за январь, февраль, май и июнь 2008 г. (ОП – окисляемость перманганатная, Ж – жесткость, "–" – анализ на данный показатель не проводился)
|
Показатель, единица измерения |
Глубина, м |
январь |
февраль |
май |
июнь |
|||||||
|
1 |
2 |
3 |
1 |
2 |
3 |
2* |
3 |
1 |
2 |
3 |
||
|
t, °С |
0,3 |
0,4 |
0,5 |
0,3 |
0 |
–0,1 |
0,1 |
14,7 |
14,4 |
25,7 |
25,5 |
25,1 |
|
1 |
0,1 |
–0,1 |
0,1 |
–0,8 |
0,1 |
0,4 |
13,7 |
14,3 |
23,8 |
24,6 |
21,4 |
|
|
рН, ед. рН |
0,3 |
7,1 |
7,3 |
7,0 |
6,5 |
7,4 |
7,3 |
8,6 |
8,5 |
7,2 |
7,2 |
6,7 |
|
1 |
7,0 |
6,9 |
6,9 |
7,3 |
7,2 |
7,3 |
8,2 |
8,6 |
7,1 |
7,1 |
6,2 |
|
|
О2, мг/дм3 |
0,3 |
– |
– |
– |
2,9 |
2,8 |
3,8 |
7,1 |
7,5 |
9,6 |
9,7 |
9,0 |
|
1 |
– |
– |
– |
0,6 |
5,3 |
3,5 |
6,4 |
8,7 |
9,5 |
9,3 |
3,4 |
|
|
ОП, мгО/ дм3 |
0,3 |
17,4 |
18,2 |
19,4 |
19,9 |
19,7 |
19,2 |
8,4 |
8,7 |
10,7 |
8,8 |
9,8 |
|
1 |
20,8 |
22,6 |
28,8 |
19,6 |
21,8 |
20,6 |
9,7 |
9,9 |
11,9 |
9,3 |
10,0 |
|
|
Feобщее мг/дм3 |
0,3 |
2,3 |
2,0 |
2,6 |
3,2 |
2,6 |
3,5 |
0,5 |
0,5 |
0,8 |
0,5 |
0,8 |
|
1 |
1,2 |
1,0 |
2,9 |
3,6 |
2,8 |
3,9 |
1,3 |
0,2 |
0,6 |
1,3 |
0,8 |
|
|
SO42-, мг/дм3 |
0,3 |
4,6 |
12,6 |
11,3 |
16,0 |
11,2 |
14,5 |
6,8 |
10,4 |
24,9 |
22,3 |
13,6 |
|
1 |
8,4 |
6,5 |
9,8 |
14,8 |
12,5 |
12,0 |
8,6 |
8,3 |
18,6 |
15,5 |
11,5 |
|
|
CI-, мг/дм3 |
0,3 |
12,8 |
19,2 |
21,0 |
27,8 |
26,9 |
24,2 |
23,4 |
29,5 |
29,4 |
27,2 |
23,8 |
|
1 |
10,0 |
21,0 |
6,4 |
25,1 |
22,4 |
22,4 |
26,5 |
28,8 |
27,4 |
29,2 |
22,6 |
|
|
NH4+, мг/дм3 |
0,3 |
1,1 |
7,9 |
7,6 |
9,1 |
5,7 |
7,2 |
14,3 |
12,6 |
0,6 |
0,6 |
12,1 |
|
1 |
6,7 |
7,7 |
1,1 |
5,8 |
6,7 |
9,3 |
12,7 |
12,9 |
0,5 |
0,4 |
15,3 |
|
|
NO2-, мг/дм3 |
0,3 |
0,02 |
0,04 |
0,04 |
0,02 |
0,02 |
0,02 |
0,02 |
0,02 |
0 |
0,05 |
0,04 |
|
1 |
0,04 |
0,04 |
0,02 |
0,03 |
0,02 |
0,02 |
0,02 |
0,02 |
0,04 |
0,04 |
0,02 |
|
|
NO3-, мг/дм3 |
0,3 |
1,7 |
1,6 |
1,3 |
0,8 |
1,0 |
0,8 |
0,9 |
0,9 |
0,9 |
0,2 |
2,0 |
|
1 |
1,1 |
1,2 |
1,0 |
1,8 |
0,9 |
0,8 |
0,9 |
0,8 |
1,0 |
0,4 |
4,9 |
|
|
Ж, °Ж |
0,3 |
– |
– |
– |
– |
– |
– |
1,2 |
1,4 |
1,4 |
1,4 |
1,1 |
|
1 |
– |
– |
– |
– |
– |
– |
1,5 |
1,1 |
1,2 |
1,3 |
1,3 |
|
|
Ca2+, мг-экв/л |
0,3 |
– |
– |
– |
– |
– |
– |
0,7 |
0,7 |
1,2 |
0,7 |
0,6 |
|
1 |
– |
– |
– |
– |
– |
– |
0,8 |
0,8 |
0,8 |
0,7 |
0,7 |
|
|
Mg2+, мг/дм3 |
0,3 |
– |
– |
– |
– |
– |
– |
6,7 |
7,7 |
2,6 |
8,6 |
6,1 |
|
1 |
– |
– |
– |
– |
– |
– |
8,0 |
4,4 |
5,2 |
7,2 |
7,4 |
|
Примечание.* в точке 1 взять пробу воды было невозможно, так как в районе этой точки кругом были установлены рыболовные сети.
Кислородный режим в поверхностных водах формируется за счет фотосинтеза, обмена с атмосферой, биохимического потребления на дыхание живых организмов [3]. Содержание кислорода неоднородно как по длине и глубине озера, так и по времени отбора проб воды. Определены средние прямые связи концентрации кислорода в воде с ее температурой (табл. 3). В летние месяцы (июнь – июль), когда температура воды достигает 24–25 °С в поверхностном слое, содержание кислорода за счет фотосинтеза достигает до 9,0 … 10,0 мг/дм3. На глубине 1 м его концентрация минимальна в феврале – 0,6 мг/дм3 и максимальна в июне – 9,5 мг/дм3. Соединения азота (нитратный, нитритный и аммонийный ионы) относят к биогенным веществам, участвующим в биологических процессах биоты [6]. Зафиксированные концентрации нитрит- и нитрат-ионов характерны для природных поверхностных вод – 0…0,05 мг/дм3 и 0,2…4,9 мг/дм3 соответственно и подтверждаются в работе [7]. Концентрация ионов аммония в озере значительно превышает предельно допустимые нормы для водных объектов рыбохозяйственного назначения (0,5 мг/дм3). Содержание аммония сильно варьирует как во временном диапазоне, так и по длине озера – от 0,4 до 28,3 мг/дм3. Максимальные средние концентрации аммония в озере отмечены в мае (13,5 мг/дм3 – до 0,3 м и 12,8 мг/дм3 – до 1 м) и в августе (15,3 мг/дм3 и 22,8 мг/дм3 соответственно). Высокое содержание аммония приводит к повышению значения водородного показателя [7]. В мае среднее значение рН воды в озере выросло до 8,5 ед. рН, а в августе – 9,7 ед. рН. Выявлена средняя прямая корреляционная зависимость между концентрацией аммония в воде и рН (rs = 0,3), что согласуется с данными, полученными в работе [8].
Таблица 2
Гидрохимические показатели воды в озере Иримное за июль – октябрь 2008 г. (ОП – окисляемость перманганатная, Ж – жесткость, "–" – анализ на данный показатель не проводился)
|
Показатель, единица измерения |
Глубина, м |
июль |
август |
сентябрь |
октябрь |
||||
|
2* |
3 |
2 |
3 |
2 |
3 |
2 |
3 |
||
|
t, °С |
0,3 |
25,1 |
24,8 |
19,6 |
18,4 |
13,8 |
12,5 |
13,8 |
12,5 |
|
1 |
21,4 |
21,3 |
18,9 |
18,5 |
18,0 |
18,1 |
18,0 |
18,1 |
|
|
рН, ед. рН |
0,3 |
6,7 |
6,5 |
9,8 |
9,7 |
7,7 |
7,8 |
7,8 |
7,2 |
|
1 |
6,2 |
6,1 |
9,8 |
9,6 |
7,7 |
7,7 |
7,7 |
7,8 |
|
|
О2, мг/дм3 |
0,3 |
9,0 |
10,0 |
7,3 |
6,6 |
9,2 |
7,0 |
5,9 |
9,3 |
|
1 |
3,4 |
3,2 |
8,2 |
7,0 |
8,3 |
5,9 |
8,4 |
5,3 |
|
|
ОП, мгО/дм3 |
0,3 |
9,8 |
10,2 |
9,9 |
8,8 |
9,3 |
11,1 |
10,4 |
11,4 |
|
1 |
10,0 |
11,0 |
6,9 |
9,5 |
6,4 |
7,4 |
10,4 |
12,1 |
|
|
Feобщее, мг/дм3 |
0,3 |
0,8 |
0,3 |
0,9 |
0,9 |
0,2 |
0,1 |
1,4 |
0,4 |
|
1 |
0,8 |
0,5 |
0,9 |
0,9 |
0,2 |
0,2 |
0,3 |
0,3 |
|
|
SO42-, мг/дм3 |
0,3 |
13,6 |
11,8 |
13,8 |
3,8 |
7,1 |
12,0 |
9,2 |
6,5 |
|
1 |
11,5 |
11,1 |
21,8 |
18,3 |
7,8 |
11,0 |
7,3 |
6,8 |
|
|
CI-, мг/дм3 |
0,3 |
23,8 |
18,8 |
19,6 |
36,3 |
8,2 |
9,9 |
11,3 |
12,0 |
|
1 |
22,6 |
23,0 |
8,2 |
10,2 |
9,2 |
8,5 |
10,6 |
13,9 |
|
|
NH4+, мг/дм3 |
0,3 |
12,1 |
8,7 |
19,8 |
10,7 |
5,3 |
4,6 |
13,1 |
10,0 |
|
1 |
15,3 |
10,9 |
17,4 |
28,3 |
6,2 |
8,1 |
14,5 |
11,5 |
|
|
NO2-, мг/дм3 |
0,3 |
0,04 |
0,01 |
0,04 |
0,04 |
0,01 |
0,04 |
0,04 |
0,04 |
|
1 |
0,02 |
0,02 |
0,01 |
0,02 |
0,04 |
0,04 |
0,04 |
0,04 |
|
|
NO3-, мг/дм3 |
0,3 |
2,0 |
2,4 |
2,1 |
2,4 |
1,9 |
0,7 |
0,8 |
0,5 |
|
1 |
4,9 |
4,0 |
2,7 |
1,1 |
1,6 |
0,8 |
0,6 |
1,4 |
|
|
Ж, °Ж |
0,3 |
1,1 |
1,1 |
1,7 |
1,6 |
1,2 |
1,3 |
1,2 |
1,1 |
|
1 |
1,3 |
1,2 |
1,5 |
5,1 |
1,2 |
1,3 |
1,1 |
2,5 |
|
|
Ca2+, мг-экв/л |
0,3 |
0,6 |
0,7 |
0,6 |
0,6 |
0,6 |
0,6 |
- |
- |
|
1 |
0,7 |
0,7 |
0,6 |
0,6 |
0,6 |
0,6 |
- |
- |
|
|
Mg2+, мг/дм3 |
0,3 |
6,1 |
5,5 |
13,6 |
11,8 |
7,8 |
9,1 |
- |
- |
|
1 |
7,4 |
6,3 |
11,3 |
55,3 |
7,1 |
8,4 |
- |
- |
|
Примечание. * в точке 1 взять пробу воды было невозможно, так как в районе этой точки кругом были установлены рыболовные сети.
Таблица 3
Коэффициент корреляции Спирмена между гидрохимическими показателями воды озера Иримное (ОП – перманганатная окисляемость, Ж – жесткость)
|
Показатель |
t |
рН |
О2 |
ОП |
Fe |
SO42- |
CI- |
NH4+ |
NO2- |
NO3- |
Ж |
Ca2+ |
Mg2+ |
|
t |
1 |
– |
0,4 |
–0,9 |
–0,8 |
– |
– |
– |
– |
– |
– |
0,5 |
–0,4 |
|
рН |
1 |
– |
–0,5 |
–0,3 |
– |
– |
0,3 |
– |
– |
0,8 |
–0,3 |
0,8 |
|
|
О2 |
1 |
–0,3 |
– |
– |
– |
– |
– |
– |
–0,3 |
0,4 |
–0,6 |
||
|
ОП |
1 |
0,9 |
0,4 |
– |
–0,3 |
– |
– |
–0,3 |
– |
– |
|||
|
Fe |
1 |
0,3 |
– |
–0,4 |
– |
– |
0,3 |
– |
– |
||||
|
SO42- |
1 |
– |
– |
– |
– |
– |
0,7 |
– |
|||||
|
CI- |
1 |
–0,5 |
– |
– |
0,5 |
0,4 |
– |
||||||
|
NH4+ |
1 |
– |
– |
– |
–0,5 |
0,3 |
|||||||
|
NO2- |
1 |
– |
0,3 |
–0,6 |
0,7 |
||||||||
|
NO3- |
1 |
– |
–0,4 |
– |
|||||||||
|
Ж |
1 |
0 |
0,7 |
||||||||||
|
Ca2+ |
1 |
–0,7 |
|||||||||||
|
Mg2+ |
1 |
Примечание. «–» – корреляция статистически не значима.
Так как озеро Иримное является водоемом замкнутого типа, то растворенный аммиак может образовываться в результате жизнедеятельности водной растительности, поступать с атмосферными осадками или в результате локального «свежего загрязнения» – возможного гниения рыбы в рыболовных сетях, установленных в большом количестве (до 7–10 сетей) на данном озере. Рыбное население озера было представлено преимущественно серебряным карасём (Carassius auratus gibelio) – (>90 %), а также золотым карасём (Carassius carassius) [1]. Данные виды рыб являются наиболее устойчивыми к негативным факторам среды, в том числе и заморам в зимнее время, когда содержание кислорода в воде составляет менее 6 мг/дм3. Среднее содержание хлорид-ионов (20,7 мг/дм3) и сульфат-ионов (12,6 мг/дм3) в воде озера имеет природный характер, так как их концентрации находятся в диапазоне значений значительно ниже предельно допустимых концентраций (300 и 100 мг/дм3 соответственно) для водных объектов рыбохозяйственного назначения.
Выводы
Определены средние прямые связи концентрации кислорода в воде с ее температурой. На глубине 1 м его концентрация минимальна в феврале – 0,6 мг/дм3 (зимний замор) и максимальна в июне – 9,5 мг/дм3. Определена слабощелочная реакция воды по среднему значению водородного показателя воды. Наблюдалось повышение значения рН при увеличении концентрации магния, жесткости и аммония в воде озера Иримное. Определены сильные статистически значимые прямые связи между рН и концентрации магния и жесткости, средние – между рН и концентрацией аммония в воде озера. При повышении содержания железа в воде увеличивается окисляемость перманганатная. Значения концентраций аммония, железа и окисляемости перманганатной выше предельно допустимых концентраций для водных объектов рыбохозяйственного назначения.
Cтатья подготовлена при финансовой поддержке ФАНО России в рамках темы ФНИ № 0408-2014-0019 «Миграционные процессы радионуклидов и химических поллютантов в экосистеме водоемов Обь-Иртышского бассейна».
Библиографическая ссылка
Алимова Г.С., Токарева А.Ю. ГИДРОХИМИЯ ОЗЕРА ИРИМНОЕ // Успехи современного естествознания. 2018. № 11-1. С. 79-84;URL: https://natural-sciences.ru/en/article/view?id=36909 (дата обращения: 15.05.2026).
DOI: https://doi.org/10.17513/use.36909



