Scientific journal
Advances in current natural sciences
ISSN 1681-7494
"Перечень" ВАК
ИФ РИНЦ = 0,976
THE STUDY OF THE STRUCTURE OF DINITROTOLUENE WISTERIA USING PHYSICAL AND CHEMICAL METHODS
Изучение влияния строения комплексных соединений на изменение их физико-химических характеристик является актуальным направлением координационной химии. Особую роль играют комплексы, имеющие в своем составе органо-неорганические компоненты. Область применения координационных соединений, в состав которых входят борная, аминоуксусная и лимонная кислоты, достаточна широка. Комплексные соединения на основе бора используются в качестве нетоксичных антипиренов, твердых электролитов, ингибиторов коррозии металлов, антиоксидантов и др. [1, 2]. Авторами модифицирована методика синтеза бидентатных координационных соединений на основе тетракоординированного бора, выделено в кристаллическом состоянии и изучено новое комплексное соединение дицитратоборат глициния (ДЦБГли). Результаты термогравиметрического анализа дают качественную характеристику соединению, позволяют сделать вывод о влиянии аминокислоты в качестве внешней сферы на характер химической деструкции изучаемых ацидокомплексов бора и скорость процесса разложения. Показано, что новое комплексное соединение устойчиво при высоких температурах, а при дальнейшем нагревании происходит образование большого объема негорючих газов с наличием значительного эндотермического эффекта. При исследовании ранее синтезированных комплексов, относящихся к данному типу координационных соединений, данного эффекта не наблюдалось, поэтому авторами сделан вывод о специфическом влиянии глицина на процесс термического разложения тетракоординированного комплекса. Используя сравнительный анализ инфракрасных спектров нового комплексного соединения ДЦБГли и других комплексов бора, было подтверждено предположение о нахождении атома бора в тетракоординированном состоянии. Метод ИК-спектроскопии позволил доказать наличие симметрии в молекуле дицитратобората глициния. Амины известны как летучие ингибиторы коррозии металлов [1, 3], поэтому соли комплексов бора с аминокислотами могут быть перспективны для использования в качестве ингибиторов коррозии комбинированного действия при невысоких температурах (выше 100 °С). Предположительная область применения дицитратобората глициния в качестве антипирена основана на выделении при сжигании большого объема негорючих газов (H2O, NH3, CO2).
Материалы и методы исследования
В работе использовали реактивы: борная кислота «ХЧ», содержание основного компонента более 99 %, L-α-глицин (аминоуксусная кислота) «Ч» ГОСТ 5860-75, лимонная кислота безводная мелкогранулированная «ЧДА» E 330.
Для создания метастабильной системы были использованы пересыщенные растворы кислот, которые вступали во взаимодействие в молярных соотношениях: 0,05 моль (3,09 г) борной кислоты, 0,1 моль (21,03 г) лимонной кислоты и 0,1 моль (7,5 г) L-α-глицина. Для создания определенного индукционного периода кристаллизации борную кислоту растворяли в 30 мл дистиллированной воды при постоянном перемешивании на водяной бане при температуре 50–60 °С. Раствор медленно охлаждали и добавляли лимонную кислоту. Полученную смесь повторно поместили на водяную баню при той же температуре для получения пересыщенного раствора смеси двух кислот. В медленно охлажденный раствор добавляли аминоуксусную кислоту, не прекращая перемешивание системы. Мольное соотношение компонентов составляло 1:2:1 соответственно. Образовавшиеся кристаллы выдерживали в растворе в течение нескольких суток, затем отделяли фильтрованием на воронке Бюхнера, промывали диэтиловым эфиром и сушили в эксикаторе [4].
ИК-спектры регистрировали на спектрометре с преобразованием Фурье Nicolet IR200 (Thermo Scientific) c использованием приставки внутреннего отражения с элементом НПВО – нарушенное полное внутреннее отражение (ATR) из ZnSe с углом падения 45о. Разрешение 4 см-1, число сканов равно 20. Исследования особенностей термической деструкции ДЦБГли проводили на приборе синхронного термического анализа NETZSCH STA-449 F1Jupiter в интервале температур 20–950 °С в среде аргона. Рентгенодифракционные исследования проводили на дифрактометре SMART APEX DUO CCD (MoKα-излучение, графитовый монохроматор, ω-сканирование). Структура расшифрована прямым методом и уточнена МНК в анизотропном полноматричном приближении по F2hkl. Атомы водорода OH и NH3 групп и молекулы воды найдены из фурье-синтеза и уточнены изотропно, остальные атомы водорода помещены в геометрически рассчитанные положения и включены в уточнение в модели «наездника» с Uiso(H) = 1,2Ueq(C). Все расчеты проведены по комплексу программ SHELX версии 2014/1#. Плотность ДЦБГли по гелию измеряли на автоматическом пикнометре ACCU Pic 1340 при температуре 22 °С [4].
При изучении бактерицидной активности новых субстанций в качестве тест-микроорганизмов использовали: Pseudomonas aeruginosa (штамм АТСС 27853) – для оценки бактерицидной активности в отношении грамотрицательных бактерий; Staphylococcus aureus (штамм 906) – для оценки бактерицидной активности в отношении грамположительных бактерий. Минимально подавляющую концентрацию соединения исследовали по МУК 4.2.1890-04 «Определение чувствительности микроорганизмов к антибактериальным препаратам» (методом серийных разведений в мясопептонном бульоне).
Результаты исследования и их обсуждение
Известно, что глицин в кислой среде ионизируется до катиона [5] и может образовывать внешнюю сферу комплексной соли. Тогда реакцию образования ДЦБГли можно представить схемой (рис. 1).
H3BO3 + 2(HOOCCH2)2C(OH)COOH> H[B(C6H6O7)2]· Н2О + 2Н2О (а)
H[B(C6H6O7)2]· Н2О + H2NCH2COOH > H3NCH2COOH+ [B(C6H6O7)2]– · Н2О (б)
Рис. 1. Механизм синтеза дицитратобората глициния: а) образование дилимоноборной кислоты; б) получение дицитратобората глициния
Синтезированный комплекс представляет собой устойчивое на воздухе твердое соединение, растворимое в воде и практически не растворимое в органических растворителях. Для подтверждения индивидуальности синтезированного комплексного соединения проводили ИК-спектрометрию индивидуальных веществ, использованных при синтезе, и полученного соединения. На рис. 2 представлены ИК-спектры нового комплексного соединения – дицитротобората глициния. Анализируя полученную информацию, можно сделать вывод, что в ДЦБГли атом бора находится в тетракоординированном состоянии, аналогично ранее синтезированным соединениям данного класса, что подтверждается наличием полос в области 1189 см-1 и 1195 см-1 соответственно [5]. Особенностью нового комплексного соединения является наличие не только валентных колебаний связи В–О в боркислородном тетраэдре, что подтверждается полосой поглощения при 943 см-1, но и наблюдаемый высокочастотный сдвиг по сравнению с поглащением валентного колебания В–О, что доказывает более прочный характер связи N–B4. Полосы поглощения 1720–1780 см-1 обусловлены валентными колебаниями С=О связи в карбоксильной группе, связанной с атомом бора и свободной соответственно. Смещение относительно соответствующей полосы в спектре исходного реагента в область коротких волн на 35 см-1 связано с образованием связи С–О–В. Полосы поглощения в области 2980 см-1 и 1410–1430 см-1 отвечают валентным колебаниям связи О-Н в карбоксильной группе и деформационным колебаниям связи С-Н соответственно [4, 5]. Валентные колебания связи С-О обусловливают появление максимумов при 1060 и 1130 см-1. Полоса поглощения при 1320 см-1 относится к валентным колебаниям связей С-N во фрагменте глициния NH3+. Полоса при 1510 см-1 принадлежит деформационным колебаниям связи N-H, а 3570 см-1 – к валентным колебаниям связи N-H в NH3+ [3]. Структура синтезированного комплекса изучена методом РСА. Анализ базы Кембриджского центра кристаллографических данных (the Cambridge Crystallographic Data Center (CCDC)) позволяет утверждать, что синтезировано новое комплексное соединение с глицином во внешней сфере. Структурными единицами кристаллов является дицитратоборатанион, катион глицина и молекула воды. Идентификация и нумерация неводородных атомов соединения приведена на рис. 3. Дицитратоборатанион с тетраэдром ВО4 в центре образован путем бидентатой координации атома бора с двумя молекулами лимонной кислоты через атомы кислорода центральной карбоксильной и α-гидроксильной групп.
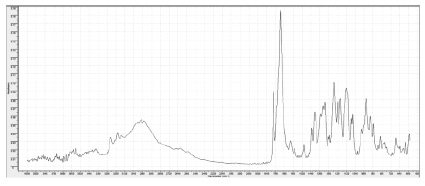
Рис. 2. ИК-спектры дицитратобората глициния (ДЦБГли)
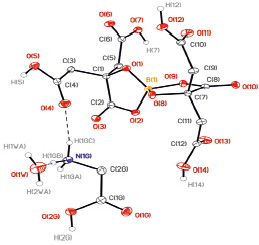
Рис. 3. Общий вид структурных элементов кристаллов ДЦБГли с обозначением и нумерацией атомов (за исключением атомов водорода алифатических цепочек (p = 50 %)
Он имеет псевдоось симметрии, которая проходит через атом бора и делит пополам ребра тетраэдра О(1) – О(8) и О(2) – О(9). Различие двух функциональных групп определяет неоднородность связей В-О и искажение тетраэдра ВО4. Связи В-О(1) и В-О(8) от гидроксильных групп (1,44 – 1,44 A) короче связей В-О(2) и В-О(9) от карбоксильных групп (1,507–1,510 A). Сопряженные с ними связи С(sp3) – O (C(1)-O(1) и С(7) – О(8)) длиннее (1,421–1,426 A) связей C(sp2) – O (С(2) – О(2) и С(8) – О(9)) (1,313 – 1,319 A). Два валентных угла О-В-О, включенных в пятичленные борогетероциклы (О(1)ВО(2) 105, 1 A и О(9)ВО(9) 104,2), меньше остальных четырех углов (ср. 111,9 ± 3,3). В ходе образования дицитратоборатанионов наибольшие изменения в длинах связей наблюдаются в карбоксильных группах молекул лимонной кислоты (по сравнению с чистым веществом).
Внешняя сфера комплексного соединения представлена катионом глициния и одной молекулой кристаллизационной воды Определение плотности ДЦБГли было проведено по методике выполнения измерений МИ 0200851-313-2007 на автоматическом пикнометре Accu Pic 1340 (Micromeritics, США) при температуре 220 °С. Плотность ДЦБГли, рассчитанная теоретически по данным РСА анализа, составила 1,674 г/см3 и мало отличается от значения, полученного с помощью пикнометрического анализа – 1,66 г/см3 (по гелию).
Исследования особенностей термической деструкции ДЦБГли проводили на приборе синхронного термического анализа NETZSCH STA-449 F1Jupiter в интервале температур 200–9500 °С в среде аргона (рис. 4). Наблюдаемый первый пик в области температур 1450 °С характеризует процесс отщепления молекулы кристаллизационной воды [5, 6]. При термическом разложении дицитратобората глициния в интервале температур 170–2100 °С в среде аргона происходит вулканизация с выбросом навески образца из тигля. Данного процесса не наблюдалось при термической деструкции ранее полученных соединений подобного класса.
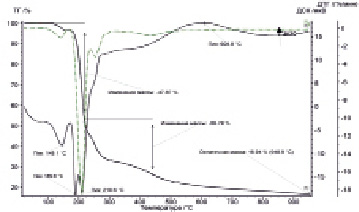
Рис. 4. Термограмма дицитратобората глициния
Процесс разложения глицина при воздействии на него высоких температур протекает в две стадии [6, 7], первая стадия характеризуется резкой потерей массы вещества за счет образования газообразных продуктов. Происходит одновременно два процесса – декарбоксилирование и термическая деструкция, что и способствует наблюдаемому мощному эндотермическому эффекту. На полученной дериватограмме ДЦБГли имеется пик при температуре 2100С, что соответствует процессу разложения глицина, находящегося в стадии ионизации, при этом образуются летучие продукты СО2, NH3, СО в большом объеме. Таким образом, механизм и результаты продуктов термической деструкции зависят от характера аминокислоты, находящейся во внешней сфере соединения. Благодаря ярко выраженному процессу образования негорючих газов, дицитратоборат глициния можно использовать как антипирен при защите изделия от процессов возгорания.
Дополнительно был проведен анализ тест-культур для определения антимикробной активности дицитратобората глициния. Для исследования на биоцидную активность брали следующие микроорганизмы: грамположительные бактерии – Bacillus subtilis АТСС 6633, B. pumilus NCTC 8241, B. mycoides 537, Micrococcus luteus NCTC 8340, Leuconostoc mesenteroides VKPM B-4177, Staphylococcus aureus INA 00761, S. aureus FDA 209P, Mycobacterium smegmatis VKPM Ac 1339, M. smegmatis mc2 155, грамотрицательные бактерии – Escherichia coli ATCC 25922, Pseudomonas aeruginosa ATCC 27853, Comamonas terrigena VKPM B-7571 и грибы – Aspergillus niger INA 00760, Saccharomyces cerevisiae RIA 259. Pseudomonas аeruginosa – грамотрицательная бактерия, является одним из основных возбудителей гнойно-воспалительных процессов.
Распространена повсеместно, чему способствует высокая устойчивость этих бактерий к неблагоприятным условиям внешней среды, выраженная антагонистическая активность и резистентность к широкому спектру природных биологически активных веществ и антимикробных средств, применяемых в медицинской практике. Экологическая безопасность синтезированной соли обеспечивается ингредиентами, входящими в ее состав, а наличие термического разложения дицитратобората глициния в интервале температур 170–210 °С с образованием большого объема летучих продуктов СО2, NH3, СО и выделением воды в парообразном состоянии позволяет расширить область применения в направлении улучшения эффективности огнезащиты, а также получения препаратов комбинированного действия, которые могут защитить объект от биоразрушений и при этом остаются экологически безопасны для человека [5, 7]. Помимо этого, амины применяют в качестве ингибиторов коррозии металлов, следовательно, соли комплексов бора, в состав которых входят соединения с аминогруппой, могут быть перспективны для использования в качестве ингибиторов коррозии при невысоких температурах.
Заключение
Усовершенствована методика получения нового комплексного соединения на основе борокислородного тетраэдра – дицитратоборат глициния с брутто-формулой C14H20BNO17 и молекулярной массой 485,12 г/моль. Представлена эмпирическая формула нового соединения, а также рассмотрен механизм протекания реакции получения дицитратобората глициния. Предложена область применения синтезированной комплексной соли в качестве экологически безопасного соединения, относящегося к группе антипиренов. Рассмотрен вопрос о возможном использовании дицитратобората глициния как ингибитора коррозии комбинированного действия при невысоких температурах, а также вещества, обладающего биоцидными свойствами по отношению к грамположительным и грамотрицательным бактериям. Определена пикнометрическая плотность ДЦБГли по гелию, которая составила 1,66 г/см3. Строение и состав соединения подтверждены данными рентгеноструктурного анализа.
Библиографическая ссылка
Тютрина С.В., Мясникова Н.В., Осина М.А. ИССЛЕДОВАНИЕ СТРУКТУРЫ ДИЦИТРАТОБОРАТА ГЛИЦИНИЯ ФИЗИКО-ХИМИЧЕСКИМИ МЕТОДАМИ // Успехи современного естествознания. 2018. № 11-2. С. 224-229;URL: https://natural-sciences.ru/en/article/view?id=36930 (дата обращения: 17.05.2026).



