Scientific journal
Advances in current natural sciences
ISSN 1681-7494
"Перечень" ВАК
ИФ РИНЦ = 0,976
REDUCTION OF ZINC ION CONTENT IN NATURAL WATERS BY MONTMORILLONITE CLAY
Важной экологической задачей современности является очистка загрязненной воды от ионов тяжелых металлов. Ежегодное поступление загрязняющих веществ во все водоемы приводит к загрязнению не только гидросферы, но и донных отложений, почв. Вода является мобильной средой, которая способствует миграции загрязняющих веществ, в том числе тяжелых металлов, на большие расстояния. Источниками поступления в окружающую среду тяжелых металлов являются естественные и антропогенные факторы. С точки зрения охраны окружающей среды серьезную опасность представляют сточные воды химической, металлургической промышленности, а также гальванических производств, содержащие в своем составе ионы цинка, кадмия, меди, марганца, кобальта, никеля, железа, хрома [1–2].
Природные и сточные воды представляют собой сложные гетерогенные системы, содержащие растворенные, коллоидные и взвешенные в воде неорганические и органические соединения. Ежегодный мониторинг водных ресурсов подтверждает увеличение в природной воде ионов тяжелых металлов [3]. В связи с этим возрос интерес применения эффективных и безопасных технологий очистки сточных и природных вод. Наиболее простыми и эффективными методами очистки природных и сточных вод являются сорбционные.
Перспективным направлением является использование экологически безопасных сорбентов на основе природных глинистых материалов и алюмосиликатов [4–6], которые обладают высокой адсорбционной и ионообменной селективностью к различным соединениям, химически устойчивы и механически прочны.
Целью работы является исследование структуры и адсорбционной способности Кыштырлинской глины с содержанием монтмориллонита в нативной и модифицированных формах к ионам цинка.
Материалы и методы исследования
В качестве адсорбента использовали глину с содержанием монтмориллонита Кыштырлинского месторождения Тюменской области в нативной (природной) и модифицированных формах.
Химический состав глины определяли рентгеноструктурным анализом (РСпА) сканирующим растровым микроскопом JEOLJSM 6510 LV. Состав глины представлен в табл. 1. Точность установления элементного состава ±2 %.
Потери при прокаливании природной Кыштырлинской монтмориллонитовой глины составляют 8,12 %.
Согласно результатам химического анализа в состав входит 54 % диоксида кремния и 20,73 % оксида алюминия, что определяет полукислый характер глины. Водорастворимые оксиды натрия и калия в сумме составляют 3,82 %.
Фазовый состав нативной глины определяли с использованием рентгенофазового анализа (рис. 1). Рентгенофазовый анализ выполняли на дифрактометре Bruker D2 Phaser с линейным детектором Lynxeye (CuKa – излучение, Ni – фильтр).
По результатам рентгенофазового анализа в образцах глины можно выделить следующие фазы: монтмориллонит, гидрослюды, хлорит, кварц и каолинит. Процентный состав фаз представлен на рис. 2.
Таблица 1
Химический состав Кыштырлинской глины
|
Содержание |
SiO2 |
Al2O3 |
Na2O |
K2O |
CaO |
Fe2O3 |
TiO2 |
MgO |
|
% мас. |
54,0 |
20,73 |
0,75 |
3,37 |
0,60 |
9,43 |
1,1 |
1,82 |
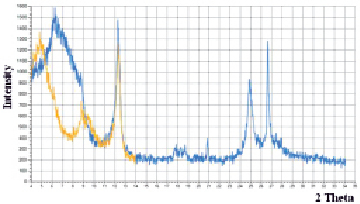
Рис. 1. Рентгенограмма Кыштырлинской нативной глины Тюменской области
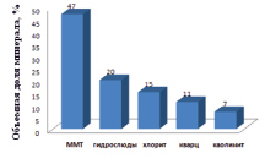
Рис. 2. Фазовый состав монтмориллонитовой глины
Структура минерала монтмориллонита представляет подвижную кристаллическую решетку, в которой чередуются трехслойные пакеты, состоящие из двух тетраэдрических слоев диоксида кремния, между которыми находится октаэдрический слой оксида алюминия. Расстояние между пакетами в зависимости от содержания воды в глине может увеличиваться от 0,4 до 2,0 нм.
На рис. 3 видно, что частицы природной глины имеют размеры менее 1 мкм в виде тонких листочков с неправильными очертаниями.

Рис. 3. Электронно-микроскопический снимок нативной глины Кыштырлинского месторождения Тюменской области
Адсорбция проводилась в статических условиях на нативной и модифицированных формах Кыштырлинской глины при температуре 298 К. Химическая модификация осуществлялась путем добавления к 1 г глины 2 М растворов HCl и NaOH. Методом разбавления из раствора сульфата цинка были приготовлены модельные растворы с концентрациями ионов цинка от 0,03 до 0,15 ммоль/мл. Количество непрореагировавших ионов цинка определяли трилонометрически [7].
Результаты исследования и их обсуждение
По экспериментальным результатам исследования построены изотермы адсорбции ионов цинка на глине в нативной и модифицированных Н- и ОН-формах, представленные на рис. 4. Вид изотермы адсорбции согласно классификации БЭТ [8] соответствует 1 типу. Вид изотермы показывает степень сродства ионов к сорбенту. Изотерма 1 типа отражает мономолекулярную адсорбцию. По изотермам адсорбции определяется максимальная обменная емкость адсорбента и рассчитываются некоторые энергетические характеристики процесса.
Изотермы адсорбции обработали с использованием уравнения Ленгмюра [8]:
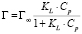
или в линейной форме
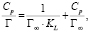
где Г – величина адсорбции, ммоль/г; Г∞ – предельная величина адсорбции, ммоль/г; KL – константа адсорбционного равновесия; Cp – равновесная концентрация, ммоль/мл.
Линейная изотерма Ленгмюра (рис. 5, а) позволяет графически определить две величины: предельную величину адсорбции (Г∞) и константу адсорбционного равновесия (KL). Для этого необходимо провести экстраполяцию прямолинейной изотермы до оси ординат. Отрезок, отсекаемый на оси ординат, соответствует величине 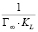 , а тангенс угла наклоны прямой tgα = 1/Г∞ [9]. Расчеты представлены в табл. 2.
, а тангенс угла наклоны прямой tgα = 1/Г∞ [9]. Расчеты представлены в табл. 2.
Полученные результаты (табл. 2) показывают, что чем больше константа адсорбционного равновесия KL, тем сильнее возникает взаимодействие системы адсорбент – поглощаемое вещество, в данном случае ионы цинка. Отсюда следует, что полученные величины адсорбционного равновесия в зависимости от формы глины можно расположить в ряд:
нативная форма (19,87 мл/ммоль) > > Н-форма (66,14 мл/ммоль) > > ОН-форма (207,33 мл/моль).
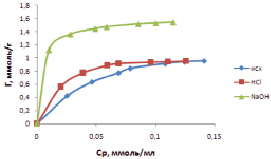
Рис. 4. Изотермы адсорбции ионов цинка при температуре 298 К
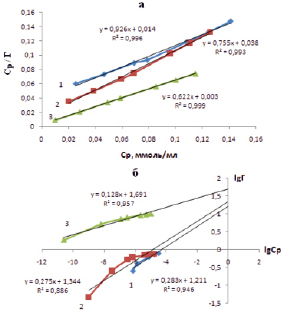
Рис. 5. Изотермы адсорбции в линейных координатах уравнений Ленгмюра (а) и Фрейндлиха (б) ионов цинка на Кыштырлинской глине в нативной (1), Н- (2) и ОН- (3) формах
Для технологических расчетов по очистке воды адсорбционными методами на практике используют уравнение Фрейндлиха [8–9]:
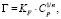
где Г – величина адсорбции, ммоль/г; Cp – равновесная концентрация, ммоль/мл; KF – константа, численно равная емкости адсорбента при остаточной концентрации ионов цинка в растворе, равной единице; n – константа, характеризующая кривизну изотермы в начальной области концентраций. Изотермы адсорбции в координатах Фрейндлиха представлены на рис. 5, б, а результаты расчета констант уравнения Фрейндлиха – в табл. 2.
Таблица 2
Значения адсорбционных параметров адсорбции ионов цинка, рассчитанных с использованием линейной формы уравнений Ленгмюра и Фрейндлиха
|
Модель Ленгмюра |
|||
|
Форма глины |
Г∞, ммоль/г |
KL, мл/ммоль |
R2 |
|
нативная |
1,08 |
19,87 |
0,996 |
|
Н-форма |
1,33 |
66,14 |
0,993 |
|
ОН-форма |
1,61 |
207,33 |
0,999 |
|
Модель Фрейндлиха |
|||
|
Форма глины |
KF |
n |
R2 |
|
нативная |
1,21 |
3,5 |
0,946 |
|
Н-форма |
1,34 |
3,6 |
0,886 |
|
ОН-форма |
1,69 |
7,8 |
0,957 |
Константы уравнения Фрейндлиха позволяют сравнивать активность адсорбента в разных формах по отношению к ионам тяжелых металлов. Из табл. 2 следует, что Кыштырлинская глина, содержащая монтмориллонит в ОН-форме, более активна по отношению к нативной и Н-формам.
Заключение
По результатам работы можно сделать вывод, что природная глина с содержанием монтмориллонита обладает высокими адсорбционными свойствами по отношению к ионам цинка.
Изотермы адсорбции ионов цинка хорошо описываются различными моделями адсорбции.
Определены значения предельной статической адсорбционной емкости Кыштырлинской глины, содержащей монтмориллонит, которая составляет 1,08 ммоль/г (нативная), 1,33 ммоль/г (Н-форма), 1,61 ммоль/г (ОН-форма).
Монтмориллонитовая глина представляет собой перспективный природный адсорбент для извлечения ионов цинка из водных растворов.
Библиографическая ссылка
Пимнева Л.А., Рогов Д.О., Ларионова К.А. СНИЖЕНИЕ СОДЕРЖАНИЯ ИОНОВ ЦИНКА В ПРИРОДНЫХ ВОДАХ ГЛИНОЙ, СОДЕРЖАЩЕЙ МОНТМОРИЛЛОНИТ // Успехи современного естествознания. 2020. № 4. С. 135-139;URL: https://natural-sciences.ru/en/article/view?id=37375 (дата обращения: 14.05.2026).
DOI: https://doi.org/10.17513/use.37375



