Прибрежные территории арктических морей, в частности Белого моря, подвергаются воздействию промышленными предприятиями, водным и автотранспортом, хозяйственной деятельностью человека [1]. Приливно-отливная зона накапливает в себе не только биофильные элементы для питания растения, но также и токсические вещества. При значительных концентрациях токсикантов у растений отмечаются морфофункциональные нарушения, изменения их цитогенетических характеристик (митотической активности), которые могут носить адаптивный характер, а могут свидетельствовать о серьезных нарушениях на ранних этапах формирования организма. В связи с этим встает вопрос об уровне техногенной нагрузки, которую могут выдержать прибрежные территории. Для изучения состояния приливно-отливной зоны используются различные методы: фитоценотический, геоботанический. В известной нам литературе разработанного метода с использованием цитогенетических характеристик для соленых почв нет.
Целью наших исследований была разработка метода оценки влияния загрязнения с использованием цитогенетических характеристик (митотической активности) на растения, произрастающие на соленых почвах приливно-отливной зоны приморских территорий.
Разработка метода
Обоснование выбора диагностического вида. На всех почвах приливно-отливной зоны отмечается высокая соленость, которая поддерживается за счет приливно-отливного цикла прихода морских вод. Соленость морской воды в Белом море около 30 ‰, и сходные значения отмечаются и на всех почвах приморских территорий, которые подвергаются приливно-отливной динамике. Если в морской воде соленость может значительно варьировать, то в почве она высокая и относительно постоянная. Прорастание семян приморских галофитов на таких почвах затруднено. В ранневесенний период семена прорастают за счет таяния снега, ливневых стоков и благодаря опресненным водам в эстуариях рек, эффективно снижающих соленость субстрата [2; 3]. Поэтому требуется разработка специального подхода для использования цитогенетических методов. Предыдущие исследования и данные литературы показали, что более солеустойчивым видом из общепринятых диагностических видов являются растения пшеницы. Выбор тест-объекта зависел от нескольких параметров: растение должно быть солеустойчивым; материал должен быть доступен круглый год; корневая меристема должна содержать большое количество делящихся клеток; хромосомы должны быть достаточно крупными. В связи с этим в качестве диагностического объекта были выбраны семена Triticum aestivum L. сорта Московская 39.
Сбор опытного субстрата. Почвенные пробы были взяты в окрестностях п. Рабочеостровск Кемского района (рисунок).
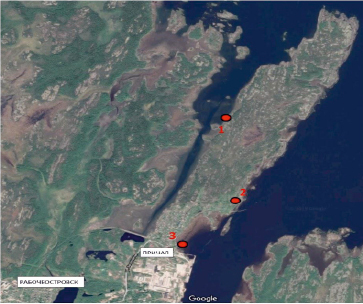
Карта района исследований на западном побережье Белого моря – п. Рабочеостровск (Кемский район). Условные обозначения: 1 – пробная площадь ПП1 (западный берег о. Октябрьской Революции), 2 – пробная площадь ПП2 (200 от Никольской церкви), 3 – пробная площадь ПП3 (порт п. Рабочеостровск) [4]
Для оценки состояния почв были сделаны почвенные прикопки согласно ГОСТ 17.4.3.01-83. [5], а также взяты почвенные образцы на химический анализ. Химический анализ содержащихся тяжелых металлов проводился с использованием оборудования Центра коллективного пользования научным оборудованием Института биологии КарНЦ РАН. Почвенные пробы для проращивания на них растений были высушены, просеяны через сито с диаметром отверстий 2.5 мм. Из-за высокой солености и плотности субстрат перемешивали в соотношении 1:1 с химически нейтральным веществом – обожженным вермикулитом (фракция 3 мм). Использование самого субстрата, а не почвенной вытяжки обусловлено тем, что не все соединения водорастворимы, некоторые токсиканты связаны плотной матрицей анализируемых объектов. Из-за чего более перспективно непосредственное взаимодействие растения и почвы – «токсикант – живой организм» [6; 7].
Выбор контрольного субстрата
В качестве контроля выступал универсальный биогрунт «Живой биогрунт. Универсальный», в составе которого 75 % торфа, 20 % биогумуса, 5 % агроперлита и микроэлементов Zn, Сu, Mn, Mo, B, Fe в количестве, не превышающем предельно допустимые концентрации (ПДК) химических веществ в почве согласно гигиеническим нормативам ГН 2.1.7.2041-06 [8].
Предварительная обработка и проращивание семян
Из-за высокой солености на субстрате, взятом из приливно-отливной зоны, смешанном с вермикулитом, семена диагностического вида пшеницы не прорастали. Поэтому схожие по размеру семена без видимых повреждений [9] заранее на 2 суток были оставлены в дистиллированной воде при температуре 25 °С при 20-часовом фотопериоде. После этого семена с проклюнувшимися корешками (2–3 первичных корешка длиной 1–1,5 см) высаживали в субстрат. Полив опытных растений проводили дистиллированной водой.
Экспериментальная работа выполнена в апреле 2020 г. Было заложено 10 серий опытов (3 точки по 3 пробы на каждой (верхняя часть, средняя и нижняя часть литорали) и 1 проба контроля). Каждая серия длилась 14 дней от момента высадки на субстрат. За 14 дней нам удалось получить достаточное количество корешков пшеницы на исследуемых образцах субстрата.
Работу выполняли на давленых препаратах. Корешки из 70 % спирта переносим в раствор соли Мора на 5–7 минут. Затем в ацетогематоксилин на 15 мин., подогревая раствор с корешками на водяной бане до 40 градусов. Корешки из ацетогематоксилина переносим на стекло с каплей 45 % уксусной кислоты на 2–3 минуты. Затем переносим на стекло с каплей хлоралгидрата и отделяем апикальную меристему корешка в зоне деления длиной 2 мм. Накрываем препарат покровным стеклом и готовим давленый препарат [10], убирая излишки хлоралгидрата фильтровальной бумагой.
Обработка материала. Микроскопирование проводили с помощью микроскопа «CARL ZEISS Primo Star» на 40- и 100-кратном увеличении. На препарате учитывался митотический индекс – процент делящихся клеток от общего числа проанализированных клеток. На каждом препарате в 10 полях зрения просматривали в общей сложности 1000 клеток, находящихся в покое и на определенной стадии митоза. В 10 пробах было просмотрено 10 000 клеток [11].
Статистическая обработка. Статистическую значимость различий контрольной пробы от исследуемых проб оценивали по критерию Стьюдента [12].
Апробация метода. На исследуемой территории были выбраны 3 пробные площади (ПП) с различным предполагаемым уровнем загрязнения тяжелыми металлами.
ПП1 – условно чистая точка.
ПП2 – средне загрязненная точка.
ПП3 – точка с сильным уровнем загрязнения.
В полевых условиях на каждой из трех пробных площадей было заложено по 1 трансекте в направлении от коренного берега до уреза воды. С каждой трансекты были взяты по три варианта проб грунта с уже известным уровнем загрязнения тяжелыми металлами: верхняя часть приливно-отливной зоны, средняя её часть и урез воды. Согласно разработанной методике на взятых почвенных пробах проращивались семена пшеницы. Для полива использовалась дистиллированная вода. В зоне деления апикальной меристемы корешка определяли митотический индекс. Митотический индекс (МИ, ‰) – отношение числа клеток, находящихся в митозе, к общему числу клеток исследуемой ткани апикальной меристемы корня, выражают в процентах [13; 14].
Анализ митотического индекса на пробных площадях с различной степенью загрязнения
Проведенное исследование показало, что значение митотического индекса зависит от уровня загрязнения (таблица).
При анализе отношения числа клеток, находящихся в митозе, к общему числу клеток апикальной меристемы корня на ПП1, ПП2, ПП3 было отмечено, что этот показатель постепенно возрастал от условно чистой точки (ПП1) к ПП2, затем к условно сильно загрязненной ПП3 вне зависимости от того, из какой части литорали была взята почвенная проба. По отношению к контролю митотический индекс на ПП1 в береговой части возрастал в 1,7 раза, на ПП2 – в 2,4 раза, а на ПП3 – в 2,8 раза. Содержание свинца и никеля на ПП1 постепенно снижалось от условно чистой точки до условно сильно загрязненной.
Анализ митотического индекса на пробной площади по трансекте от коренного берега до уреза воды
По мере удаления от коренного берега вглубь моря митотический индекс на всех пробных площадях снизился в среднем на 59 % ± 2,5 (таблица).
На ПП1 по мере продвижения вниз по трансекте митотический индекс уменьшался на 59 %, а содержание железа и никеля обратно пропорционально возрастало в 5,8 и 2,2 раза соответственно. Концентрация свинца снизилась в средней части трансекты и осталась на этом уровне у уреза воды. Региональный фоновый уровень по содержанию железа, никеля и свинца не был превышен.
Митотический индекс на ПП2 от коренного берега до нижней части литорали снизился на 56 %. При этом содержание исследуемых тяжелых металлов оставалось нестабильным. Так, например, концентрация свинца по мере продвижения вглубь моря повышалась, превысив значение в береговой части в 5,5 раз. Содержание никеля оставалось практически стабильным, незначительно понижаясь к средней части трансекты и повышаясь к урезу воды. Содержание железа в средней части литорали снизилось в 1,5 раза относительно почвенной пробы у береговой части, затем незначительно повысилось, так и не достигнув первоначального уровня.
При анализе митотического индекса на ПП3 было отмечено, что показатель средней части литорали снизился в 1,7 раза относительно почвенной пробы взятой из береговой части. В нижней части литорали индекс статистически незначимо повысился в отношении средней части. Содержание металлов – железа и свинца – оставалось стабильным. Данные значимо не различались. Концентрация свинца вглубь моря постепенно снижалась и достигала количества в 3,8 раза ниже концентрации этого металла в береговой части.
Значение митотического индекса ( ‰) и содержание тяжелых металлов (мг/кг) в апикальной меристеме корня диагностического вида пшеницы Triticum aestivum L. в зависимости от положения пробы почвы по трансекте от берега до уреза воды
|
Точки сбора почвенных образцов |
Содержание Fe, мг/кг |
Содержание Ni, мг/кг |
Содержание Pb, мг/кг |
Митотический индекс на ПП (МИ, ‰) |
|
ПП1 Береговая часть Средняя Нижняя часть литорали |
369,5 1780,2 2151,3 |
0,57 0,89 1,28 |
1,28 0,78 0,75 |
13,2 ± 1,4 9,1 ± 1,5 7,9 ± 1,7 |
|
ПП2 Береговая часть Средняя Нижняя часть литорали |
1338,9 874,0 1073,5 |
2,28 1,77 1,92 |
0,09 0,17 0,50 |
18,6 ± 1,4 11,1 ± 1,3 10,5 ± 1,4 |
|
ПП3 Береговая часть Средняя Нижняя часть литорали |
685,5 653,2 554,4 |
0,52 0,59 0,46 |
1,08 0,38 0,28 |
22,1 ± 1,9 12,9 ± 1,3 13,6 ± 1,6 |
|
Контроль |
27 533* |
4,0* |
6,0* |
7,7 ± 1,5 |
|
Региональный фоновый уровень: Fe – 17 500 мг/кг; Ni – 27,5 мг/кг; Pb – 15,5 мг/кг |
||||
Примечание. *Производитель торфогрунта отмечает отсутствие данных микроэлементов или их содержание в количестве, не превышающем предельно допустимых концентраций.
Достоверные различия получены только на ПП1, а на ПП2 и ПП3 эта закономерность отмечается в виде тенденции. При продвижении по трансекте от берега до уреза воды МИ уменьшается. На основании этих данных можно высказать предположение, что чувствительность растений к загрязнению ТМ на разных участках приливно-отливной зоны различается. Если на прибрежных территориях может работать система адаптации (что ускоряет митотические процессы), то на заливных участках ТМ могут вызывать негативные явления на уровне цитогенетических процессов.
При разработке метода были выявлены некоторые особенности: при выборе тест-объекта необходимо учитывать его солеустойчивость, восприимчивость к химическим реагентам. Так, например, более устойчивый, чем пшеница, ячмень совершенно не годился для окрашивания. При обработке корешков ячменя солью Мора они становились непригодными для раздавливания.
Также необходимо учитывать особенности прорастания семян. При культивировании растений необходимо предварительно дать семенам проклюнуться в пресной воде до образования 2–3 корешков длиной 1–1,5 см.
Эти опыты показали, что предложенный нами метод может быть использован для работы с действием тяжелых металлов в условиях загрязнения на уровне анализа цитогенетических процессов.
Работа выполнена с использованием оборудования Центра коллективного пользования научным оборудованием Института биологии КарНЦ РАН при финансовом обеспечении из средств федерального бюджета на выполнение государственного задания (№ 0752-2020-0007).
Библиографическая ссылка
Таскина К.Б. ОЦЕНКА СТЕПЕНИ ЗАГРЯЗНЕНИЯ СОЛЕНЫХ ПОЧВ ПРИЛИВНО-ОТЛИВНОЙ ЗОНЫ С ИСПОЛЬЗОВАНИЕМ ЦИТОГЕНЕТИЧЕСКОЙ ХАРАКТЕРИСТИКИ // Успехи современного естествознания. 2020. № 11. С. 120-124;URL: https://natural-sciences.ru/en/article/view?id=37525 (дата обращения: 25.04.2026).
DOI: https://doi.org/10.17513/use.37525



