Усиленное освоение приморских территорий в Арктическом регионе привело к увеличению антропогенной нагрузки на морские экосистемы в виде загрязнения разными видами органических веществ и тяжелых металлов [1]. Разработка систем фиторемедиации соленых морских вод приморских территорий становится одним из основных направлений теоретических и прикладных исследований в экологии и природопользовании. Фиторемедиация определяется как использование растений для очистки окружающей среды от загрязнителей путем их депонирования и перевода в нетоксичную форму [2]. В литературе имеются примеры использования различных родов галофитов (Zostera, Atriplex, Salicornia) для фиторемедиации морских территорий [3–5].
На приморских территориях зоной контакта суши и моря является литораль. Для нее характерна приливно-отливная динамика морской воды. Два раза в сутки растения то заливаются водой, то осушаются, при этом полностью меняется среда обитания растений и все климатические условия. На литорали успешно произрастают и проходят все этапы развития уникальные растения галофиты, имеющие механизмы адаптации к стрессовым условиям существования [6]. Однако вопрос о возможности поглощения и накопления растениями литорали тяжелых металлов остается открытым.
Цель исследования – оценить условия обитания и накопление тяжелых металлов в растениях астры солончаковой (Aster tripolium L.) на приливно-отливной зоне Белого моря (п. Рабочеостровск).
Материалы и методы исследования
Район исследования
Работа выполнена на побережье Белого моря в районе г. Кемь, п. Рабочеостровск (Кемский район) (рис. 1), в июле 2019 г. Поселок Рабочеостровск расположен в зоне шхерных берегов побережья Белого моря. На западном и восточном берегах острова Октябрьской революции (соединён насыпью с коренным берегом) были заложены пробные площади. На трех пробных площадях (ПП) от линии уреза воды (во время отлива) до зоны контакта штормовых выбросов у коренного берега были заложены три трансекты. На пробных площадях по трансектам было сделано описание растительности, грунтов литорали, собраны растения астры солончаковой, грунт под растениями и пробы морской воды. Названия маршевых почвогрунтов даны по работе М.А. Цейца (2005) [7].
ПП1 – западная часть о. Октябрьской революции – 65 °00'37.3"N 34 °48'10.6"E, расположена на пологом илисто-песчаном берегу с наличием валунно-галечниковых скоплений (размер валунов от 30 до 50 см) в средней части литорали. Соленость морской воды в отлив 24 ‰. От коренного берега до линии уреза воды маршевый примитивный супесчаный оторфованный грунт переходил в маршевый примитивный супесчаный оглеенный грунт и далее – в супесчаный литоральный грунт. Общее видовое богатство изученных сообществ составляет 19 видов [8].
ПП2 – восточный берег о. Октябрьской революции – 64 °59'43.2"N 34 °47'35.0"E. Илисто-песчаный берег довольно завалунен, встречаются как крупные (1,5 м), так и более мелкие валуны (около 60 см). Соленость морской воды в отлив 23 ‰. Грунт песчаный оглеенный литоральный. Общее видовое богатство изученных сообществ составляет 13 видов [8].
ПП3 – район порта – 64 °59'29.5"N 34 °47'19.4"E, расположена на скалистых выступах берегов, обнажающихся в отлив (луды). Поверхность осушки нередко покрыта морскими выбросами и нанесенным приливами мусором (древесные остатки с металлическими гвоздями, пластиковые пакеты, битое стекло и др.). Соленость морской воды в отлив 26 ‰.
Грунт слоистый заиленный песчаный литоральный. Общее видовое богатство изученных сообществ составляет 4 вида [8] (рис. 1).
Объект исследования
Объект исследования – Астра солончаковая (Aster tripolium L.) относится к семейству Астровые (Asteraceae), евроазиатский бореальный вид, являющийся доминантом и субдоминантом различных приморских растительных сообществ (рис. 2). Это распространенный вид приморского галофитного комплекса [9].
Методы исследования
Определение солености воды проводили рефрактометром RHS-10ATC.
Содержание тяжелых металлов определяли атомно-абсорбционным методом (атомно-абсорбционный спектрофотометр АА–7000 (Shimadzu, Япония) на оборудовании Центра коллективного пользования Федерального исследовательского центра «Карельский научный центр Российской академии наук». В работе представлены валовые средние арифметические значения содержания тяжелых металлов в грунтах, корнях, надземных органах, целом растении и морской воде.
Коэффициент биологического поглощения (КБП) металлов рассчитывали как отношение содержания металла в растении к сумме его содержания в воде и грунте. КБП металлов характеризует способность растений поглощать тяжелые металлы из среды. Считается, что если коэффициент больше единицы, то растение активно накапливает металлы. Литоральный грунт собирали непосредственно в зоне корней растений. Растения астры солончаковой отбирали в средней части литорали на каждой пробной площади (n = 5) и делили на корни и надземную часть.
Статистическая обработка данных
Достоверность полученных результатов оценивали с помощью критерия Фишера, регрессионного и корреляционного анализов с учетом объема сравниваемых совокупностей и порога доверительной вероятности 0,95 (программа Statgraphics 2.1 для Windows).
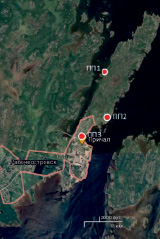
Рис. 1. Пробные площади (ПП1, ПП2, ПП3)

Рис. 2. Астра солончаковая Aster tripolium L.
Результаты исследования и их обсуждение
Содержание элементов в грунтах и морской воде
Морская вода в окрестностях п. Рабочеостровск значительно загрязнена нитратами до 2,1–0,9 ПДК, железом – до 6,4–0,8 ПДК, никелем – до 17,7–14,8 ПДК и свинцом – до 9,8–2,4 ПДК. Наибольшее загрязнение морской воды этими элементами на ПП1. Содержание марганца, цинка и меди в морской воде не превышает предельно допустимых значений. Соленость воды 23–26 ‰.
Литоральные грунты на пробных площадях не загрязнены тяжелыми металлами (табл. 2). Среднее содержание железа в грунте (ПП1–ПП3) было на уровне 13179,39 ± 6968 мг/кг, марганца – 122,29 ± 47 мг/кг, цинка – 31,21 ± 19 мг/кг, меди – 14,36 ± 9 мг/кг, никеля – 12,39 ± 7 и свинца на уровне 7,59 ± 5 мг/кг. Однако можно отметить более высокие уровни металлов в грунтах на ПП3 (район порта), превышающие фоновые значения по меди, свинцу и цинку и равные 0,4 ОДК цинка, 0,9 ОДК меди, 0,8 ОДК никеля и 0,6 ОДК свинца.
Накопление элементов растениями Aster tripolium L.
Установлена положительная связь между содержанием элементов в среде обитания (грунт + вода) и накоплением металлов астрой солончаковой. Коэффициенты корреляции (r) между содержанием металлов в среде и в растениях астры равны для железа 0,51; марганца 0,33; для цинка 0,83; меди 0,90; никеля 0,64 и свинца 0,95. Рассмотрим накопление каждого металла подробнее.
Железо. Астра солончаковая накапливала железо в количестве 15–32 г. Это очень высокие значения содержания железа у растений (ПДК > 0,5 г). Астра – гипераккумулятор железа на литорали Белого моря. При этом максимальное накопление железа установлено на ПП3 (зона порта) и в целом 90 % от общего содержания в растении железа накапливалось в корнях астры. КБП железа больше единицы и равны 1,06–2,50 (табл. 3).
Марганец. Марганец накапливался в растениях астры в значениях 137– 417 мг/кг, на ПП2 до значений ПДК. КБП 0,91–4,76. Основная часть марганца (70 %) также накапливалась в корнях астры (табл. 3).
Цинк. Содержание цинка в растениях было на уровне 30–250 мг/кг, максимально на ПП3 (зона порта), где накопление марганца превышало критический уровень для растений. КБП 1,36–3,94 и 90–50 % металла накапливалось также в подземных органах астры.
Медь. Медь была на уровне 12–70 мг/кг в растениях астры, при этом максимальные значения были установлены также у растений ПП3 (превышение ПДК). КБП 1,78–3,86. Корни астры накапливали 50–80 % всей содержащейся в растении меди (табл. 3).
Никель. Астра солончаковая накапливала очень высокие количества никеля 66–560 мг/кг, максимально на ПП3. Астра – гипераккумулятор никеля на литорали Белого моря. КБП никеля были очень высокие 6,27–24,24. Никель в растениях превышал критический уровень у растений в 6–56 раз. При этом корень также вмещал 90 % всего растительного никеля (табл. 3).
Свинец. 11–478 мг/кг свинца содержалось в растениях астры. На ПП3 превышение критического уровня составило 24 ПДК. Астра – гипераккумулятор свинца на литорали Белого моря. КБП 2,55–27,70. И 90 % растительного свинца накапливали корни астры (табл. 3).
Таким образом, астра солончаковая активно накапливает металлы (КБП > 1). Средний ряд (ПП1–ПП3) накопления металлов Ni (15,84) > Pb (8,21) > Zn (2,93) > Cu (2,82) > Mn (2,08) > Fe (1,71). По абсолютным значениям содержания металлов в растениях можно сделать вывод, что астра – гипераккумулятор железа, никеля и свинца в условиях обитания на литорали Белого моря. Корни растений накапливают 70–90 % всех поступающих в растение металлов по сравнению с надземной частью астры солончаковой.
Астра солончаковая (Aster tripolium L.) доминирует в растительном покрове литорали Белого моря в пределах изученных пробных площадей в окрестностях п. Рабочеостровск [7]. Растения астры обитают в условиях значительного загрязнения морской воды нитратами до 2,1–0,9 ПДК, железом до 6,4–0,8 ПДК, никелем до 17,7–14,8 ПДК и свинцом 9,8–2,4 ПДК (табл. 1). Литоральные грунты не загрязнены тяжелыми металлами. Однако можно отметить, что на ПП3 (зона порта) установлены уровни металлов, превышающие фоновые значения и равные 0,4 ОДК цинка, 0,9 ОДК меди, 0,8 ОДК никеля и 0,6 ОДК свинца (табл. 2).
Таблица 1
Содержание элементов в морской воде в районе пробных площадей приливно-отливной зоны Белого моря (п. Рабочеостровск)
|
Пробная площадь |
NO3- мг/л |
Cl- г/л |
Минерализация г/л |
Fe мг/л |
Mn мг/л |
Zn мг/л |
Ni мг/л |
Cu мг/л |
Pb мг/л |
|
ПП1 |
83,72 |
2,41 |
12,4 |
0,32 |
0,014 |
0,008 |
0,165 |
0,00068 |
0,098 |
|
ПП2 |
43,68 |
1,76 |
7,8 |
0,04 |
0,011 |
0,028 |
0,148 |
0,00001 |
0,024 |
|
ПП3 |
50,25 |
2,24 |
11,8 |
0,05 |
0,004 |
0,003 |
0,177 |
0,00027 |
0,064 |
|
М |
59,21 |
2,13 |
10,67 |
0,14 |
0,01 |
0,01 |
0,16 |
0 |
0,06 |
|
σ |
21,47 |
0,34 |
2,51 |
0,16 |
0,01 |
0,01 |
0 |
0 |
0,04 |
|
Фон* |
– |
> 2,5 |
– |
0,01 |
0,002 |
0,010 |
0,002 |
0,003 |
0,00003 |
|
ПДК** |
39,00 |
– |
– |
0,05 |
0,050 |
0,050 |
0,01 |
0,01 |
0,01 |
М – среднее арифметическое, σ – стандартное отклонение, *Фон – естественный уровень исследуемых показателей морской воды, ** ПДК в морской воде водных объектов рыбохозяйственного значения [10].
Таблица 2
Содержание элементов в грунтах пробных площадей приливно-отливной зоны Белого моря (п. Рабочеостровск)
|
Пробная площадь |
Металл |
Fe |
Mn |
Zn |
Cu |
Ni |
Pb |
|
мг/кг |
|||||||
|
ПП1 |
M |
19119,39 |
150,90 |
21,39 |
6,94 |
10,41* |
3,93 |
|
σ |
4532,39 |
40,84 |
4,77 |
2,60 |
2,49 |
0,95 |
|
|
ПП2 |
M |
7263,17* |
87,63* |
8,91 |
4,91 |
3,85* |
1,67 |
|
σ |
2372,81 |
25,28 |
0,54 |
1,52 |
0,06 |
0,57 |
|
|
ПП3 |
M |
13155,60 |
128,35 |
63,33* |
31,23* |
22,90* |
17,18* |
|
σ |
5124,40 |
23,44 |
10,15 |
7,81 |
5,80 |
3,50 |
|
|
Фон ДО1 |
– |
– |
62 |
18 |
30 |
15 |
|
|
ОДК2 |
46500 |
1500 |
150 |
35 |
30 |
30 |
|
1Фоновые значения содержания тяжелых металлов в донных отложениях (ДО) морей.
2ОДК – ориентировочно допустимые концентрации для незагрязненных донных осадков по SFT [11].
*данные, представленные со звездочкой, достоверно различаются по ПП согласно Fisher’s LSD test. (p ≤ 0,05).
Поступление загрязняющих веществ в Белое море происходит с течениями крупных рек Северо-Запада России (Кемь, Северная Двина, Кереть, Онега, Нижний Выг, Верхний Выг) [11]. Так, объем сбрасываемых сточных вод в поверхностные водные объекты бассейна Белого моря в 2019 г. составил 73,87 млн м3 (в 2018 г. – 70,13 млн м3), в том числе 14,98 млн м3 приходится на сбросы горнодобывающего металлургического предприятия АО «Карельский окатыш». Основные загрязняющие вещества выбросов АО «Карельский окатыш» – сернистый ангидрид, железо, никель, марганец, свинец, цинк. Согласно данным Государственного доклада о состоянии окружающей среды Республики Карелия, наибольшую массу в составе загрязняющих веществ, сбрасываемых в водоемы бассейна Белого моря в 2019 г., составляют: лигнин сульфатный (3014,88 т), калий (1982,43 т), нитраты (1446,41 т), магний (601,51 т), натрий (524,35 т), железо (30,51 т), нефтепродукты (11,92 т), никель (898,64 кг) [1].
Растения Aster tripolium L. активно накапливают тяжелые металлы из среды, о чем свидетельствует КБП > 1 (табл. 3). Средний ряд (ПП1–ПП3) накопления металлов Ni (15,84) > Pb (8,21) > Zn (2,93) > Cu (2,82) > Mn (2,08) > Fe (1,71). Растение Aster tripolium – гипераккумулятор железа, никеля и свинца, так как накапливает очень высокие уровни железа (15–32 г/кг), никеля (66–560 мг/кг) и свинца (11–478 мг/кг), особенно на ПП3 (зона порта). Содержание железа в тканях астры в тысячи раз превышает содержание других элементов. Считается, что если растения накапливают металл до значений более чем 1000 мг/кг, то его относят к гипераккумуляторам, а если до значений < 500 мг/кг – то к негипераккумуляторам или вторичным аккумуляторам этого металла [13].
Таблица 3
Содержание тяжелых металлов (М – среднее арифметическое значение), мг/кг, и коэффициент биологического поглощения металлов (КБП) в целом растении, надземных органах и корнях Aster tripolium L. приливно-отливной зоны Белого моря (п. Рабочеостровск)
|
Элемент |
Fe |
Mn |
Zn |
Cu |
Ni |
Pb |
|
мг/кг |
||||||
|
ПП1 |
||||||
|
М все раст |
20284 ± 700 |
137,17 ± 50,11 |
29,17 ± 7,23 |
12,38 ± 3,00 |
66,30 ± 15,14 |
10,25 ± 3,12 |
|
М надз |
2556 ± 300 |
49,23 ± 33 |
13,98 ± 9,00 |
5,40 ± 2,21 |
12,53 ± 4,65 |
1,28 ± 0,50 |
|
М корень |
17728 ± 1500 |
87,94 ± 21 |
15,19 ± 5,10 |
6,97 ± 1,58 |
53,77 ± 7,02 |
8,98 ± 1,22 |
|
КБП раст |
1,06 |
0,91 |
1,36 |
1,78 |
6,27 |
2,55 |
|
КБП надз |
0,13 |
0,33 |
0,65 |
0,78 |
1,18 |
0,32 |
|
КБП корень |
0,93 |
0,58 |
0,71 |
1,00 |
5,08 |
2,23 |
|
ПП2 |
||||||
|
М все раст |
15503 ± 2000 |
417,42 ± 25,36* |
41,57 ± 15,10 |
18,94 ± 2,01 |
95,15 ± 10,23 |
11,23 ± 1,00 |
|
М надз |
1155 ± 256 |
29,62 ± 3,58 |
24,39 ± 5,12 |
7,11 ± 1,15 |
17,93 ± 3,70 |
1,36 ± 0,05 |
|
М корень |
14347 ± 1470 |
387,79 ± 70,25 |
17,18 ± 3,18 |
11,83 ± 2,00 |
77,22 ± 3,15 |
9,87 ± 2,00 |
|
КБП раст |
2,13 |
4,76 |
4,65 |
3,86 |
23,80 |
6,61 |
|
Окончание табл. 3 |
||||||
|
Элемент |
Fe |
Mn |
Zn |
Cu |
Ni |
Pb |
|
мг/кг |
||||||
|
КБП надз |
0,16 |
0,34 |
2,73 |
1,45 |
4,48 |
0,80 |
|
КБП корень |
1,98 |
4,42 |
1,92 |
2,41 |
19,32 |
5,81 |
|
ПП3 |
||||||
|
М все раст |
32905 ± 2589* |
162,26 ± 15,20 |
249,41 ± 35,00* |
70,52 ± 15,12* |
559,45 ± 63,00* |
477,71 ± 30,30* |
|
М надз |
1471 ± 300 |
37,52 ± 7,20 |
21,00 ± 3,58 |
5,32 ± 1,00 |
6,01 ± 1,06 |
2,69 ± 0,63 |
|
М корень |
31433 ± 5000 |
124,74 ± 10,60 |
228,41 ± 25,80 |
65,20 ± 7,78 |
553,44 ± 80,10 |
475,01 ± 45,20 |
|
КБП раст |
2,50 |
1,26 |
3,94 |
2,26 |
24,24 |
27,70 |
|
КБП надз |
0,11 |
0,29 |
0,33 |
0,17 |
0,26 |
0,16 |
|
КБП корень |
2,39 |
0,97 |
3,61 |
2,09 |
23,98 |
27,54 |
|
ПДК1 |
> 500 |
300-500 |
>100 |
20-100 |
10-100 |
20-300 |
* данные, представленные со звездочкой, достоверно различаются по ПП согласно Fisher’s LSD test. (p ≤ 0,05)
1 – предельно допустимая концентрация содержания элементов в растениях, мг/кг [12].
Ранее нами было показано, что растения Plantago maritima L. и Triglochin maritima L., обитающие на литорали Белого моря в районе п. Кереть, также накапливают железо до уровней 13–22 г/кг соответственно [14]. Есть факты, что галофиты Salicornia europaea, Suaeda maritima, Salsola soda и Halimione portulacoides с засоленных морских территорий могут накапливать до 2,3 г/кг железа всем растением и в корнях 1,3 г/кг [6]. Хорошо известно, что клеточная стенка растений может депонировать тяжелые металлы [6, 14]. Возможно, связывание атомов железа клеточной стенкой корней и листьев астры солончаковой может повышать её жесткость, обеспечивая повышение прочности органов в условиях наибольшей приливно-отливной динамики моря.
Корни растений Aster tripolium L. накапливают 70–90 % всех поступающих в растение металлов по сравнению с надземной частью астры солончаковой. Хорошо известно, что именно корневая система и ее ткани – первый барьер на пути загрязняющих веществ [3, 15]. Адаптация растений на уровне организма направлена на иммобилизацию металлов в корнях, чтобы защитить от токсического действия металлов репродуктивные органы и семена [15]. Следует отметить, что астра солончаковая – корневищное растение, накапливает металлы в корне в течение всей жизни растения, в то время как наземная часть растений отмирает каждый год и её минеральные элементы питают грунты литорали и берега в виде выбросов.
Таким образом, в условиях загрязнения среды обитания нитратами, железом, никелем и свинцом на литорали Белого моря растения-галофиты Aster tripolium L. активно накапливают металлы, в основном корнями, и могут рассматриваться как гипераккумуляторы железа, никеля и свинца.



