Scientific journal
Advances in current natural sciences
ISSN 1681-7494
"Перечень" ВАК
ИФ РИНЦ = 0,976
STRUCTURE OF HUMIC ACIDS OF DRY-STEPPE SOILS OF ZABAIKALYA
Гуминовые вещества представляют собой полидисперсные макромолекулы сложного строения [1]. Среди органических веществ гуминовые кислоты отличаются наибольшей биохимической устойчивостью [2]. Однако их состав и структура изменчивы во времени и в пространстве, отражая условия гумусообразования.
Почвенный гумус выполняет важную роль в плодородии почв, поэтому изучение основных характеристик гумуса, структуры гуминовых кислот необходимо для комплексной оценки плодородия.
Известно, что молекула гуминовой кислоты состоит из ядерной и периферической частей. Ароматическая часть молекулы сформирована более устойчивыми фрагментами. Боковые фрагменты характеризуются неустойчивыми химическими связями с ядерной частью, являясь питательным ресурсом для микроорганизмов почвы.
Цель исследования: выявить особенности структуры макромолекул гуминовых кислот каштановых почв Забайкалья.
Материалы и методы исследования
Объекты исследования – препараты гуминовых кислот, выделенные из каштановых почв (0-20 см): ГК-1с – Селенгинское среднегорье; ГК-2у – Удинская котловина, ГК-3и – Иволгинская котловина.
Препараты ГК были выделены по методу Д.С. Орлова [3].
Элементный состав проанализирован на приборе CHNS/O Series II фирмы Perkin Elmer (США) в Институте общей и экспериментальной биологии СО РАН (г. Улан-Удэ). ИК-спектры определены на инфракрасном спектрофотометре «ISF-25» (Bruker).
13С-ЯМР-спектры сняты на спектрофотометре UNIT–500. В зависимости от интенсивности сигналов 13С-ЯМР-спектров методом количественного анализа выявлен фрагментарный состав С в препаратах ГК каштановых почв.
Методы инфракрасного (ИК), ядерного магнитного резонанса (ЯМР) позволяют получить информацию о структуре макромолекулы ГК, а также об определенном нахождении разных функциональных групп и молекулярных фрагментов [4-6].
Каштановые почвы Забайкалья являются самыми теплообеспеченными в регионе с суммой температур выше 10 °С 1700-1800 ° и наибольшим биологически активным периодом – в среднем 111 дней. Они формируются нa различных породах: в основном на песках, супесях, легких суглинках. В основном каштановые почвы имеют легкий гранулометрический состав, а также часто содержат в почвенном профиле много камней и щебня плотных пород.
Растительный покров забайкальских сухих степей имеет своеобразную криоксерофильность. Средообразующей способностью характеризуются Artemisia frigida (Willd.), Artemisia gmelinii (Web. et Stechm.), Koeleria gracilis (Pers.), Carex duriuscula (С.А. Меу) и др.
Растительность Забайкалья своеобразная, обусловленная наложением широтной зональности на высотную поясность при выраженных горно-котловинных инверсиях и экспозиционных эффектах. Основными особенностями климата региона являются: высокий приход солнечной радиации (до 3000 час/год), незначительное количество осадков и неравномерность их выпадения, резкие колебания температуры воздуха, проявляющиеся в значительных амплитудах колебаний среднесуточных и среднемесячных температур.
Подземная растительная масса (BNP) сухих степей густо переплетает гумусово-аккумулятивный горизонт вследствие недостатка увлажнения и элементов питания. Корневая масса образует мощную дернину, последняя является своего рода биологическим экраном, который удерживает многие элементы питания, аккумулируя их в верхних слоях почвы. BNP для каштановых почв в слое 0-20 см достигает 200 ц/га [7].
Величина чистой первичной продукции составляет в каштановой почве в среднем 1,3-1,5 кг/м2·год, из которых на надземную массу приходится до 9-10 %, а на подземную 94-95 %. Выявлены большие различия в весовом соотношении надземной и подземной частей фитоценозов, которые составляли 1:14,7 – 1:23,5, что связано с невысоким продуцированием надземной растительной массы растительностью сухостепных экосистем.
Суровые почвенно-климатические условия затрудняют рост и развитие растительности, в результате чего образуется своеобразная адаптированная растительность с определенным качественным составом (высокое содержание лигнина, низкое – азота, фосфора, кальция и магния). Незначительное поступлению свежего органического вещества обусловлено низкой биологической продуктивностью растительных ассоциаций.
Известно, что биомасса, образующаяся в течение короткого вегетационного периода, первоначально накапливается в верхних слоях почвы, тем самым создает ежегодное накопление органического вещества [8-10].
В исследуемых каштановых почвах в условиях криоаридного климата значительно сокращены периоды гумификации и минерализации растительных остатков, что является благоприятным условием для более длительного сохранения слабогумифицированных растительных остатков и неспецифических соединений [7].
На элементный состав гуминовых кислот оказывает существенное влияние химический состав растительности, произрастающей на каштановых почвах. В сухостепных почвах региона азотный фонд беден, растительность обеднена азотом и содержит его 1,43 % в ANP и 1,52 % в BNP.
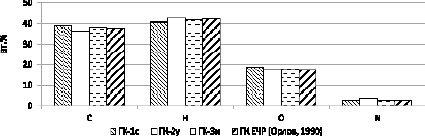
Рис. 1. Элементный состав каштановых почв. Условные обозначения: ГК-1с – препарат ГК каштановой почвы центральной части Селенгинского среднегорья, Селенгинский район; ГК-2у – препарат ГК каштановой почвы Удинской котловины, Заиграевский район; ГК-3и – препарат ГК каштановой почвы Иволгинской котловины, Иволгинский район, ГК ЕЧР – препарат ГК чернозема европейской части России по Д.С. Орлову (1990)
Исследуемые каштановые почвы характеризуются следующими показателями: небольшая (до 22-23 см) мощность горизонта А, низкое содержание углерода органического Сорг. 0,8 %, N обнаружено до 0,10 % в 0-20 см слое почвы, наличие карбонатного горизонта, отсутствие по профилю гипсового горизонта, легкий гранулометрический состав, рН нейтральная, вниз по профилю переходящая в щелочную, суммарное количество катионов Са2+ и Mg2+ составляют почти 20 ммоль/100 г почвы. Эти почвы отличаются значительным количеством кальция и магния (2,2 и 1,9 %).
Результаты исследования и их обсуждение
А. Элементный состав ГК
В экспериментальных образцах ГК каштановых почв отмечено содержание углерода от 36,3 до 38,9 ат. %. Водорода содержится 40,7-42,7 ат. %, азота 2,5-3,7 ат. %. Следует отметить, что данные по элементному составу гуминовых кислот каштановых почв сопоставимы с данными европейских аналогов.
Степень бензоидности (СБ) позволяет учесть бензоидные структуры, которые входят в состав ядерной части макромолекулы гуминовой кислоты [11]. Максимальная степень бензоидности обнаружена в образце ГК-1с – 20 %, что соответствует по шкале СБ среднему уровню. Показатель в препарате ГК-3и равен 13 % и ГК-2у – 10 %, что является низким уровнем ароматизации макромолекулы гуминовой кислоты. Степень бензоидности каштановых почв региона невелика, это связано с тем, что простые соединения, которые образуются в результате разложения органического вещества, активно участвуют в формировании алифатической части макромолекулы ГК. К примеру, у почв немерзлотного ряда формируются гуминовые кислоты, получающие незначительное количество материала для построения алифатической части макромолекулы, что связано с увеличением длительности периода с положительными температурами. Высокая степень бензоидности (до 45 %) обусловлена тем, что в процессе гумификации отщепляется больше боковых цепочек.
Элементный состав препарата ГК-2у, полученного из сильнодефлированного варианта каштановой почвы, нехарактерный таковому в аналогичных почвах. Это, по-видимому, связано с тем, что данные почвы характеризуются большей степенью прогревания и иссушения в короткий период весной и летом, а также подвержены дефляции, содержание углерода низкое (36,3 ат. %). Содержание углерода в элементном составе показало, что не происходит достаточное усложнение строения ГК, в результате чего макромолекула ГК менее обуглерожена. Это связано с процессами дефляции и иссушения, которые препятствуют конденсации молекул и оказываются со значительным содержанием водорода и азота в своем составе, где соотношение H:С=1,17. Природно-климатические условия региона исследования обусловливают развитие криоксерофитной лигнинофицированной растительности и специфической криоаридной микрофлоры, которые являются причиной их низкой обуглероженности.
Предположительно, что в таких суровых условиях процессы ароматизации, формирующие гуминовые кислоты, заторможены и ослаблены. На строение и состав гуминовых кислот оказывают влияние также химические и биологические условия состава органических остатков, а также процессы дефляции. Достаточно низкая биологическая активность исследуемых почв способствует снижению интенсивности минерализации неспецифических веществ и накоплению алифатических боковых углеродистых цепей.
Относительно высоко содержание азота в гуминовых кислотах. В препарате ГК-2у содержание азота достигает 3,7 ат. %. Величина C:N в среднем составляет 13 %. К примеру, в одноименных почвах европейской части России показатель соответствует 17-18 % [11]. В алифатической части молекулы ГК находится большая часть азота, следовательно, белки и аминосахара аммонифицируются и нитрифицируются довольно слабо. Не исключено и относительное повышение содержания азота при понижении углерода.
Выявленные различия в элементном составе исследуемых препаратов гуминовых кислот с результатами, полученными другими авторами, с одноименными почвами более теплых фаций связаны со вторичным влиянием внешней среды [12].
Коэффициенты вариации ГК сухостепных почв между собой, а также в сравнении с аналогичными почвами более теплых аналогов невысокие для С, Н, N – 2,01-3,53 %, немного выше для N – 17,61 %.
Выявлено, что в криоаридных условиях, при длительном промораживании и высушивании почвенного профиля сухостепных почв, формируются низкоконденсированные с развитыми боковыми алифатическими цепями макромолекулы гуминовых кислот.
Б. Инфракрасные спектры поглоще- ния ГК
Информацию о конкретном расположении отдельных групп, а также набор основных атомных групп и типов связей можно определить по инфракрасным спектрам (ИК-спектры). Инфракрасные спектры препаратов гуминовых кислот каштановых почв выявляют общие закономерности построения макромолекулы ГК.
Выявлено, что самая высокая интенсивность полос поглощения определена для групп: гидроксильных, карбоксильных и метоксильных. О доминировании ядерной или периферической частей в ГК судят по разной интенсивности отдельных полос. В препаратах гуминовых кислот выявлены интенсивные полосы поглощения, относимые к скелетным колебаниям гидроксильных групп, которые имеют полосы поглощения 3400 см-1; а также метиленовым группам с областью поглощения 2920 см-1. На доминирование в образцах вышеперечисленных групп показывают также полосы поглощения в области 1375-1480 см-1 (рис. 2).
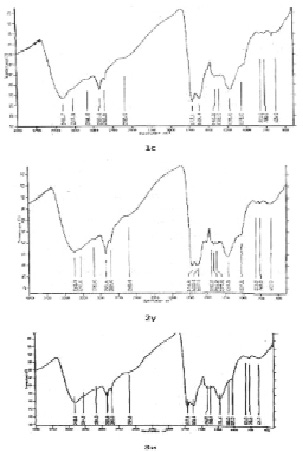
Рис. 2. ИК-спектры ГК каштановых почв
ГК исследуемых препаратов характеризуются сильными поглощениями:
1) относимые к скелетным колебаниям карбоксильных групп 1700 см-1;
2) относимые к скелетным колебаниям ароматических, карбонильных, хинонных групп 1625-1610 см-1.
В ИК–спектрах всех экспериментальных образцов ГК четко отражена полоса, характерная для карбоксильной группы. Отмечено наличие полос поглощения, характерных для третичных, вторичных и первичных групп спиртов (1150-1050 см-1).
О высоком содержании азота свидетельствуют полосы поглощения, характерные для амидов (1650 см-1). Полосы поглощения от 1622,0–1626,9 и 1512,0-1515,0 см-1, характерные для ароматических фрагментов, имеют малую интенсивность. Интенсивность поглощения в области 1620 см-1 уменьшается в следующем порядке: ГК-3и → ГК-1с → ГК-2у.
Выявлено наличие бензольных колец с двумя и более незамещенными атомами водорода, о чем говорят спектры с низкой интенсивностью в области поглощения 860-730 см-1.
Выявлена небольшая роль алканов в строении макромолекул ГК, о чем свидетельствует наличие полос с невысокой интенсивностью поглощения метильных метиленовых групп.
Анализ ИК-спектров показал, что в исследуемых препаратах ГК отмечены все группы С, где более развита боковая часть и отмечено пониженное количество ароматических компонентов, что свидетельствует о невысокой устойчивости гумуса каштановых почв Забайкалья.
В. Оценка спектров 13С-ЯМР
Структурные особенности гуминовых кислот получены в результате расчета количественных данных фрагментного состава ГК каштановых почв из спектров ЯМР.
В результате исследования выявлено, что в образцах содержится высокое количество С алкильных групп – до 31,9 (ГК-3и); а также значительное количество С метоксильных групп – до 8,3 (ГК-2у).
Содержание углерода –СООН групп низкое – 12,5 % (160-168 и 170-180 м.д.), что обусловлено невысоким темпом биологической и биохимической активностей исследуемых каштановых почв.
Содержание углерода, связанного с группой фенола, определили по разности данных в диапазонах Сар и СН3О, ее количество составило в среднем 3,5 %.
Количество Слигн. в препаратах исследуемых образцов составляет до 3 %. На состав макромолекул ГК оказывает влияние высокая лигнинофицированность растительности, так как лигнин растительных остатков является первоисточником гумусовых веществ. Максимальное содержание С группы хинонов обнаружено в препарате каштановой почвы ГК-1с (2,8 %), самое низкое – в ГК-3и (0,9 %).
Показатель общая ароматичность (fa) наименьший для препарата ГК-2у и составляет 35,2 % (106-140, 140-160 м.д.), соответственно в ряду исследованных почв данный препарат характеризуется низким содержанием ядерного С. У образца ГК-3и fa составляет 37,7 %. Общая ароматичность у препаратов ГК-2у также невысока. Соотношение H:C убывает в ряду ГК-2у (1,2) → ГК-3и (1,1) → ГК-1с (1,0).
Соотношение в составе гуминовых кислот гидрофильных и гидрофобных компонентов является важной характеристикой макромолекул гуминовых кислот. Функциональные группы, включающие в свой состав кислород, такие как СОН, СООН, С=0, СалкО, относятся к гидрофильным компонентам, их содержание составляет в среднем 43,7 %. Салк, СарС, Н относят к гидрофобным компонентам.
Таким образом, высокое содержание функциональных групп, включающих в свой состав кислород, предопределяет более разветвленную периферическую часть ГК каштановых почв Забайкалья.
Криоаридные условия степей Забайкалья вносят коррективы в химическую структуру гуминовой кислоты, сохраняя при этом относительную устойчивость и основные черты его структуры, которые характерны сухостепным почвам. При нарастании индекса аридности, а также длительном промораживании и высушивании почвенного профиля каштановых почв формируются ГК с низким уровнем конденсации.
Заключение
Элементный состав гуминовых кислот каштановых почв показал, что ГК имеют развитую периферическую структуру. В препаратах гуминовых кислот отмечено содержание углерода 36,3-38,9 ат. %, водорода содержится 40,7-42,7 ат. %, азота 2,5-3,7 ат. %. В целом следует отметить, что элементный состав гуминовых кислот сохраняется и сопоставим с таковым каштановых почв более теплых фаций.
В каштановых почвах содержание кислых функциональных групп низкое и находится в пределах 4,0-5,0 ммоль/г почвы, тогда как этот показатель в ГК одноименных почв европейской части России 6,0-7,0 ммоль/г. Все это свидетельствует о неразвитой ароматической структуре молекулы гуминовой кислоты.
Следствием этого является низкая реакционная способность, это объяснятся длительным воздействия холода, а также процессов дефляции. Низкоконденсированные ГК с развитыми алифатическими цепями образуются в результате: промораживания почвенного профиля на длительное время, короткого биологически активного периода, а также от иссушения поверхностных слоев почвы.
Работа выполнена по теме госзадания № 121030100228–4.
Библиографическая ссылка
Чимитдоржиева Г.Д., Чимитдоржиева Э.О. СТРУКТУРА ГУМИНОВЫХ КИСЛОТ СУХОСТЕПНЫХ ПОЧВ ЗАБАЙКАЛЬЯ // Успехи современного естествознания. 2021. № 12. С. 89-94;URL: https://natural-sciences.ru/en/article/view?id=37741 (дата обращения: 07.05.2026).
DOI: https://doi.org/10.17513/use.37741



