Scientific journal
Advances in current natural sciences
ISSN 1681-7494
"Перечень" ВАК
ИФ РИНЦ = 0,976
STUDY OF THE GENETIC DIVERSITY OF GLOBULIN PROTEINS IN CHICKPEA (CICER ARIETINUM L.) GENOTYPES
Электрофоретические компоненты запасных белков в семенах злаковых и бобовых культур передаются из поколения в поколение как генетически детерминированный признак, не изменяются и остаются стабильными в зависимости от почвенно-климатических и условий возделывания, используются как универсальные генетические маркеры и сохраняют свою научную актуальность в изучении генетического разнообразия и в ускорении процесса селекции [1].
Так, часть ДНК, связанная с областью какого-либо гена или генов в геноме, является маркером. Маркеры делятся на три типа: морфологические, биохимические и ДНК-маркеры. Молекулярные маркеры классифицируются на две группы: не связанные с полимеразной цепной реакцией (RFLP) и связанные (RAPD, AFLP, SSR) [2]. С помощью молекулярных маркеров можно обеспечить более четкое выявление генетического материала in vitro. С использованием различных маркеров были обнаружены генетические вариации в последовательностях ДНК [3]. Генетическая вариация и приспособляемость к условиям окружающей среды у сортов нута высока. Также большое влияние на процессы, связанные с эволюцией сортов, оказала человеческая деятельность. К ней относятся одомашнивание, выращивание и иммиграция [4]. Несмотря на то, что это очень важно, в некоторых исследовательских работах признавалось, что содержание белка в зерне у различных сортов нута различно и генетически обусловлено. Накопление белка в зерне нута управляется 3–7 генами. Вдобавок генетически это может создать изменчивость в составе белка зерна в сортах нута [5]. Использование биохимических и молекулярных маркеров представляет преимущество перед использованием других маркеров, например фенотипических. Репродуктивность делает эти маркеры особенно привлекательными [6]. В составе зерен нута, выращенного на разных почвах, содержание альбуминов, глобулинов, глютелинов и проламинов в значительной мере различается. Гупта, используя электрофорез в SDS полиакриламидном геле, представил разницу в молекулярном весе полосок белка, различные варианты белков зерна, то есть глобулины, глютелины, альюумины и проламины наблюдались в различных вариантах. Метод электрофореза в полиакриламидном геле (SDS-PAGE) используется для разделения белков [7]. В оценке бобовых растений использовался SRAP [8, 9]. Для оценки генетического разнообразия маркеры SRAP применяются редко [10–12]. В исследовании генетической вариации нута впервые были использованы SRAP маркеры. Для оценки генетической изменчивости в нуте используются эти маркеры.
Используя SDS-PAGE, был определен полиморфизм глобулинов, проламинов и глютелинов в генотипах нута. Вообще, в зернах бобовых растений альбумины составляют 20–35 %, глобулины – 43–55 %, проламины – 0,73–2,70 % и глютелины – 11,84–32,21 % [13]. Из них альбумины растворяются в воде, глобулины – в солях, проламины – в спирте, а глютелины – в щелочи. Альбумин и глобулин вместе составляют 63–90 % от общего белка зерна. Растворимая в солях фракция (глобулины) составляет 45–50,3 % от общей массы. Среднее значение, составляющее 47,7 % растворимой фракции, является основной белковой фракцией. Исследуемый белок нута считается водорастворимой фракцией. Альбумины со своим средним значением составляют 31,2–35,5 % от общей растворимой фракции. Третьими самыми распространенными белками зерна, содержание которых варьирует между 15,1 и 20,5 %, являются глютелины [14].
В данной исследовательской работе преследовалась цель идентификации, паспортизации и изучения генетического разнообразия местных и интродуцированных генотипов нута.
Материалы и методы исследования
В исследовательской работе были использованы местные и интродуцированные из ICARDA образцы нута. В 2021 г. на Апшеронской опытной базе Института генетических ресурсов НАНА было посеяно 76 образцов, полевые испытания проводились во II–III-й декаде ноября.
Электрофоретический анализ белка глобулина проводился в отделе «Биохимическая генетика и технология» Института генетических ресурсов НАНА. Экстракцию и электрофоретический анализ в полиакриламидном геле (A-PAGE) запасных белков глобулинов из зерен образцов нута проводили с помощью нового метода, усовершенствованного на основе модифицированного метода Ф.Ф. Поперелян. Так, после измельчения образца нута и его экстракции дважды в 500 мкл 70 %-ного спирта и центрифугирования каждый раз при 3500 об./мин, экстракт промывали дважды в 500 мкл растворе 0,03 %-ного уксуса и ацетона и каждый раз после размешивания механической мешалкой его центрифугировали при скорости 3500 об./мин. После добавления к полученному в четвертый раз экстракту 500 мкл 9-молярного раствора уксус-мочевины, проводили анализ на аппарате вертикального электрофореза в глицин-ацетатном буфере (pH – 3,5).
После того, как паттерны пронумеровали, их сравнивали друг с другом в каждой зоне, а затем осуществляли нумерацию всех паттернов без учета повторов. Так, если какой-то определенный паттерн повторялся в образцах, этому паттерну новый номер не присваивался, и так проделывалось со всеми паттернами. Частота встречаемости каждого паттерна образцов нута по всем зонам вычислялась на основании индекса генетического разнообразия Нея по нижеследующей формуле [15] :
Н = 1 – ∑Рi2 ,
где H – индекс генетического разнообразия; Pi – частота каждого паттерна в зонах.
Кластерный анализ был построен с применением метода UPGMA.
Результаты исследования и их обсуждение
Одним из основных маркеров, используемых в генетической идентификации растений, являются белковые маркеры. Впервые в Азербайджане с помощью модифицированного метода, примененного для бобовых растений, был осуществлен анализ вертикального электрофореза в A-PAGE белков глобулинов, а полученные электрофореграммы условно поделили на 4 зоны: их назвали ω-, ϒ-, β- и α-глобулины. Белки с большим молекулярным весом локализованы в ω-зоне, а белки с малым молекулярным весом – в α-зоне. Белки глобулины зерен образцов нута по сравнению с белками фасоли и сои более полиморфны, и их спектры интенсивнее. Однако белки глобулины резко отличались от показателей запасных белков глиадина и глютена из зерен пшеницы (рис. 1 и 2).
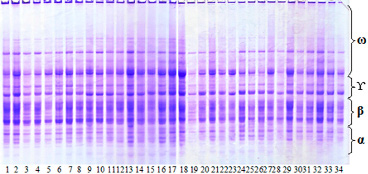
Рис. 1. Электрофореграммы белка глобулина из зерен образцов нута:
1– Flip 13-70c; 2 – Flip 13-151c; 3 – Flip 13-153c; 4 – Flip13-154c; 5 – Flip 13-194c; 6 – Flip13-227c; 7 – Flip13-234c; 8 – Flip13-240c; 9 – Flip13-247c; 10 – Flip13-250c; 11 – Flip13-251c; 12 – Flip13-253c; 13 – Flip13-258c; 14 – Flip13-261c; 15 – Flip13-277c; 16 – Flip13-278c; 17 – Flip13-282c; 18 – Flip13-308c; 19 – Flip13-314c; 20 – Flip13-320c; 21 – Flip13-330c; 22 – Flip13-335c; 23 – Flip13-336c; 24 – Flip13-338c; 25 – Flip13-340c; 26 – Flip13-343c; 27 – Flip13-356c; 28 – Flip13-358c; 29 – Flip13-364c; 30 – Flip13-369c; 31 – Flip13-376c; 32 – İLC-482c (st); 33 – Flip 82-150c; 34 – Flip 88-85c
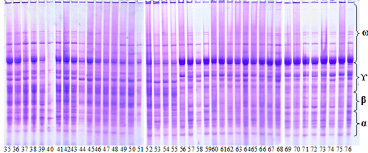
Рис. 2. Электрофореграммы белка глобулина, выделенного из зерен генотипов нута.
35 – Flip93-93c; 36 – st.Nərmin; 37 – Flip11-12c; 38 – Flip11-104c; 39 – Flip11-21c; 40 – Flip10-338c; 41 – Flip11-167c; 42 – Flip11-76c; 43 – Flip11-175c; 44 – Flip11-70c; 45 – Flip10-332c; 46 – Flip11-125c; 47 – Flip11-05c; 48 – Flip11-208c; 49 – Flip 93-93c; 50 – Flip11-32c; 51 – Flip11-66c, 52 – Flip11-205c; 53 – Flip11-140c; 54 – Flip11-08c, 55 – Flip11-198c; 56 – Flip11-11c; 57 – Flip11-209c; 58 – Flip11-215c; 59 – Flip11-45c; 60 – Flip11-72c; 61 – Flip11-210c; 62 – Flip10-318c; 63 – Flip11-16c; 64 – Flip11-58c; 65 – Flip11-138c; 66 – Flip10-345c; 67 – Flip 88-85c; 68 – Flip11-105c; 69 – Flip11-01c; 70 – İLC-482c; 71 – Flip11-216c; 72 – Flip 82-150c; 73 – Flip11-214c; 74 – Sultan, 75 – Flip11-190c; 76 – Flip11-15c
Среди исследованных образцов нута было обнаружено 23 спектра и 42 паттерна и, судя по частоте встречаемости паттернов, образуемых электрофоретическими спектрами, между ними обнаружен полиморфизм. В ω-зоне электрофореграмм запасных белков глобулина было обнаружено 7 спектров и 11 различных паттернов. В этой зоне ω-4 паттерн обнаружен в 43 образцах с частотой встречаемости 43,0 %, ω-1 паттерн – в 33 образцах с частотой встречаемости 20,0 % и ω-8 паттерн с частотой встречаемости 1,0 %. ω 4s среди всех спектров составлял самую высокую частоту встречаемости 100 %, ω3 спектр – составлял среднюю – 60,0 % , а ω1 спектр – низкую частоту встречаемости – 5,0 %.
В ϒ-зоне электрофореграмм запасных белков глобулинов наблюдалось 5 спектров и 16 паттернов. ϒ-3 паттерн обладал частотой встречаемости 43 %, ϒ-8 паттерн – 11 %, а ϒ-7 паттерн – 1 %. Среди всех спектров ϒ3s обладал самой высокой частотой встречаемости –91,0 %, ϒ4s – средней частотой встречаемости – 71 % и ϒ2s низкой – 33,0 %. В β-зоне электрофореграмм обнаружено 6 спектров и 7 паттернов. β-2 паттерн составлял частоту встречаемости 53,0 %, β-1 паттерн – 24,0 % и β-6 паттерн – самую низкую частоту встречаемости, 1 %. Была обнаружена самая высокая частота встречаемости 100 % у β4S, средняя – 87,0 % – у β3S и низкая – 28,0 % – у β6S. В α-зоне электрофореграмм было отмечено 5 спектров и 8 паттернов. α-3 паттерн составлял частоту встречаемости 36,0 %, α-1 паттерн – 29,0 %, а α-6 паттерн – 1,0 %. α2s обладал максимумом частоты встречаемости 100 %, α4S – средней частотой встречаемости 76,0 %, а α5S – низкой частотой встречаемости 45,0 %. Применив формулу Нея, между генотипами был подсчитан индекс генетического разнообразия для каждой из четырех зон. В результате проведенных подсчетов было установлено, что ϒ-зона обладала более высоким генетическим разнообразием (H = 0,786), ω-зоны (H = 0,757) и α-зоны (H = 0,761) – относительно низким генетическим разнообразием, а у β-зоны (H = 0,651) наблюдали самое низкое генетическое разнообразие (рис. 3).
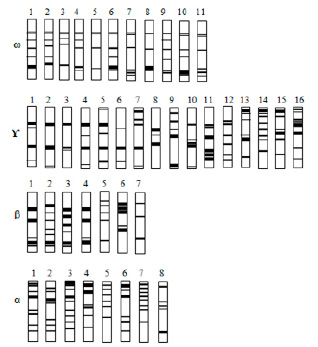
Рис. 3. Идиограмма различных паттернов ω-, ϒ-, β- и α-зон, обнаруживаемых в образцах нута

Рис. 4. Дендрограмма, отражающая генетическое расстояние между различными образцами нута на основе полиморфизма электрофореграмм белков глобулинов
После экстракции и проведенного электрофоретического анализа запасных белков глобулинов образцов нута полоски (электрофоретический спектр) между генотипами были пронумерованы на основании метода нумерации «1» и «0». Находящиеся в том же месте полоски пронумерованы на основании бинарной номенклатуры цифрой «1», а те места, где в соответствующей области полосок нет, пронумерованы цифрой «0». Используя компьютерную программу UPAGMA для определения генетической близости образцов, была построена дендрограмма, и посредством маркеров белков глобулинов изучена генетическая близость генотипов нута. Как видно из рис. 4, генотипы за номером 71, 72, 73, 74, 75 и 76 на дендрограмме классифицированы в первом кластере, образцы 52, 53, 54 – во втором, образцы за номером 69 и 70 – в третьем, номера 60 и 61 – в четвертом, а генотипы за номером 65 и 67 – в пятом кластере, и другие образцы классифицированы по два, по три, по четыре и остальные по одному кластеру. На основании полученных результатов можно прийти к заключению, что для выбора родительских форм и ускорения процесса селекции при проведении гибридизации между образцами нута, находящимися по генетическому расстоянию далеко друг от друга, целесообразно осуществление селекции с помощью маркеров.
Заключение
Проводился электрофоретический анализ в Acid-PAGE запасных белков глобулинов в зерне 76 местных и интродуцированных образцов нута Cicer Arietinum. Изучение генетического разнообразия на основе запасных белков глобулинов охарактеризовалось определением 23 спектров и 42 различных паттернов в местных и интродуцированных образцах нута. Наряду с этим были вычислены индексы генетического разнообразия электрофореграмм глобулинов (H-) образцов нута по зонам. Для определения генетической близости была использована компьютерная программа UPGMA, с помощью построения дендрограммы была определена генетическая близость генотипов нута на основе маркеров белков глобулинов.
Библиографическая ссылка
Салманова М.Р., Садыгов Г.Б., Керимов А.Я., Садыгова С.Б., Калбиева Е.Э. ИССЛЕДОВАНИЕ ГЕНЕТИЧЕСКОГО РАЗНООБРАЗИЯ БЕЛКОВ ГЛОБУЛИНОВ В ГЕНОТИПАХ НУТА (CİCER ARİETİNUM L.) // Успехи современного естествознания. 2023. № 4. С. 21-26;URL: https://natural-sciences.ru/en/article/view?id=38019 (дата обращения: 29.05.2026).
DOI: https://doi.org/10.17513/use.38019



