Официально принятая концепция оценки риска возникновения рака при радиоактивном облучении основана на линейной беспороговой теории воздействия облучения на организмы. Основное положение этой теории заключается в том, что ядерная ДНК является главной мишенью поражающего действия радиации. Воздействие даже одной частицы на ядро всего лишь одной клетки может инициировать рак. Очевидно, что количество облученных клеток пропорционально числу прошедших частиц, т.е. полученной человеком дозе. Это концепция возникла при изучении когорт, подвергшихся значительному воздействию радиации (шахтеры урановых рудников, жертвы атомной бомбардировки Хиросимы и Нагасаки). Однако при изучении воздействия малых доз радиации были получены противоречивые данные, которые не могут быть описаны в рамках линейной беспороговой теории.
Некоторые авторы считают, что влияние малых доз облучения полезно, другие - опасно. Примером первого подхода является широко известное и часто цитируемое исследование Б. Коэна, охватившее 80% населения США. Он определял параметры линейной зависимости смертности от рака легких от среднего уровня радона в округах США. В результате была получена обратная зависимость - чем больше уровень радона, тем меньше смертность. Коэн предполагает, что это связано со стимулированием механизмов защиты клеток малыми дозами радиации. В частности, было показано, что предварительное облучение клеток человеческих лимфоцитов малыми дозами радиации предохраняет их от хромосомных повреждений при последующем облучении большими дозами. При этом наблюдается повышенный синтез ферментов репарации, которые отвечают за восстановление структуры ДНК.
Второй подход связан с предположением, что воздействие малых доз радиации приводит непропорционально большому числу мутаций. Это может происходить в том случае, когда поврежденная клетка (причем необязательно повреждать именно ядро, повреждение цитоплазмы не менее значимо) инициирует мутации в соседних клетках через клеточные соединения. Было показано, что облучение 10% популяции клеток приводит к такому же выходу мутаций, как и повреждение 100% клеток. Это может привести к более быстрому, чем линейный, росту заболеваемости от дозы облучения.
В Новгородской области существуют предпосылки для изучения корреляции уровня онкологических заболеваний и интенсивности природной радиации.
Были собранны радиологические данные, характеризующие интенсивность природных источников радиации в отдельных населенных пунктах Новгородской области. Была собрана статистика смертности от онкологических заболеваний по Новгородской области за 90 годы (порядка 10 000 случаев). Создана оригинальная база данных, на основе которой получены предварительные результаты. Главный вывод заключается в том, что с ростом интенсивности излучения природных источников радиации растет и уровень смертности населения от онкологических заболеваний.
В докладе приведена зависимость уровня смертности от рака (на 100 000 населения) в населенных пунктах Новгородской области от среднего значения плотности потока радона с поверхности почвы, мБк х с-1х м-2.
Естественная радиоактивность водных источников также связана с присутствием растворенного радона, его содержание в воде можно оценить по суммарной объемной активности альфа-излучающих радионуклидов, Бк/л. Также приведена зависимость уровня смертности от рака в населенных пунктах Новгородской области от уровня альфа-активности.
Данные были обработаны программой Statistica 5.0 линейной функцией с использованием метода наименьших квадратов для выявления тенденции. Обе кривые показывают положительную корреляцию между природной радиоактивностью и уровнем смертности от онкозаболеваний.
Национальный институт исследования рака, США, разработал программы для обработки результатов эпидемиологических исследований распространенности рака среди населения - DevCan и SatScan.
DevCan позволяет рассчитать вероятность умереть от рака для гипотетической когорты из 10 миллионов новорожденных, прослеженной от возникновения до затухания, для пятилетних возрастных интервалов, последний интервал открытый. Входные данные для этого - количество населения, умерших от рака и умерших от всех причин для населения данной территории, сгруппированные по пятилетним возрастным группам. Полученные вероятности позволяют оценить число людей, которые умрут от рака в течение всей жизни на данной территории а также сравнивать территории между собой. При этом определение вероятности для гипотетической когорты связано со значительными затруднениями при корректном определении вероятностей для реального населения.
Математической основой алгоритма расчета вероятностей в программе DevCan является решение дифференциального уравнения вида
![]()
где ![]() - количество населения в момент времени
- количество населения в момент времени ![]() ,
, ![]() - вероятность умереть в единицу времени. При этом используется предположение, что уменьшение населения в связи со смертностью от рака пропорционально численности населения. Решение уравнения имеет вид
- вероятность умереть в единицу времени. При этом используется предположение, что уменьшение населения в связи со смертностью от рака пропорционально численности населения. Решение уравнения имеет вид
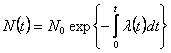
где в момент времени ![]()
![]() ,
, ![]() - начальная популяция. Вообще говоря,
- начальная популяция. Вообще говоря, ![]() является ступенчатой функцией, причем каждое ее значение определяется из наблюдаемых данных. Тогда решение принимает вид
является ступенчатой функцией, причем каждое ее значение определяется из наблюдаемых данных. Тогда решение принимает вид
![]()
где ![]() ,
, ![]() .
.
Обработка данных по районам Новгородской области с помощью DevCan позволила расположить районы по убыванию пожизненной вероятности умереть от рака, причем разница между районами с самой высокой и низкой вероятностями лежит в пределах 95% доверительных интервалов. Также видна тенденция к превышению вероятности в Старорусском районе по сравнению со среднеобластной, что может служить косвенным доказательством влияния радиоактивных источников на уровень онкологических заболеваний, т.к. Старорусский район относится к числу наиболее радиационно опасных.
SatScan позволяет определить кластеры территорий с повышенным и пониженным уровнями смертности от рака. Входными данными для этой программы являются количество населения, умерших от рака и географические координаты ряда соседних территорий. Можно также проводить корректировку данных, вводя дополнительные переменные такие как пол, возраст, известный относительный риск и т.п. SatScan использует модель, при которой количество умерших в каждой территории считается распределенным по Пуассону. Нулевая гипотеза заключается в том, что количество умерших пропорционально количеству населения. Затем перебираются все возможные случаи расположения центра кластера и его размеров (до некоторой определенной пользователем границы), вычисляется наблюдаемое и ожидаемое количество случаев в кластере и вне него, вычисляется функция правдоподобия, которая максимизируется по всем возможным кластерам. Кластер, в котором это функция имеет максимум, наименее вероятно возник случайно. Ранг правдоподобия подвергается проверке с помощью метода Монте Карло, когда ранг правдоподобия, полученный из реального множества данных сравнивается с рангом для множества данных, разыгранных по методу Монте Карло по нулевой гипотезе.
При обработке данных на уровне районов Новгородской области, были получены два наиболее вероятных кластера с повышенным уровнем смертности от рака: первого порядка (Крестецкий, Окуловский, Валдайский, Парфинский, Маловишерский) и второго порядка (Холмский, Поддорский, Маревский).
Работа поддержана Федеральным агентством по образованию, проект № 510.
Работа представлена на конференцию студентов, молодых ученых и специалистов «Секция молодых ученых, студентов и специалистов, научная конференция»,Тунис, 12-19 июня 2005 г. Поступила в редакцию 29.04.2005 г.


