Овес посевной (Avena sativa L.) - однолетнее травянистое растение семейства злаковых. Зерно овса содержит белки, жиры, углеводы (крахмал, клетчатку), минеральные вещества. Овес посевной применяется в диетическом питании в виде овсяной крупы и хлопьев, а также как загуститель и стабилизатор (овсяная камедь) [4]. В народной медицине готовят препараты как для приема внутрь, так и в виде ванн, используют как тонизирующее, мочегонное, желчегонное, антисклеротическое, жаропонижающее и противовоспалительное средство. Использование травы овса посевного в питании человека ограничено.
Целью нашей работы было изучение химического состава травы овса посевного для исследования возможности применения его в качестве пищевой добавки.
По литературным данным в траве овса посевного в большом количестве содержатся аминокислоты, а в зерновках - до 9% крахмала [1,3]. Для идентификации этих соединений используются типовые реакции: взаимодействие крахмала с иодом и реакция аминокислот с нингидрином [2,5].
В настоящем исследовании нами была использована трава овса посевного молочной зрелости, из которой готовили извлечение 70% спиртом этиловым с последующей идентификацией компонентов и их количественным определением. С целью определения веществ флавоноидной природы с одной частью извлечения проводили реакцию с цинковой пылью и кислотой хлороводородной концентрированной. Появление розового окрашивания подтвердило наличие флавоноидов.
Вторую часть извлечения исследовали методом тонкослойной хроматографии в системе хлороформ - метанол - вода (52:28:7). Хроматограмму проявляли в УФ-свете (365 нм) и затем обрабатывали 5% спиртовым раствором алюминия хлорида. Обнаружены пятна флавоноидов ярко-желтого цвета с Rf 0,44 и 0,57.
В водном извлечении, приготовленном нагреванием сырья на водяной бане при 60°С, обнаружен крахмал по образованию синего окрашивания с 0,1 М раствором иода.
Положительная реакция с нингидрином подтвердила наличие аминокислот в траве овса посевного. Последующее изучение состава водного извлечения проводили методом хроматографии в тонком слое сорбента на пластинках «Сорбфил» в системе растворителей спирт бутиловый - кислота уксусная ледяная - вода (4:1:1).Затем хроматограмму высушивали, обрабатывали 1% раствором нингидрина в спирте этиловом и нагревали в сушильном шкафу в течение 10 минут. В результате обнаружены три пятна аминокислот розового цвета со значениями RS относительно кислоты глютаминовой: 0,85; 1,00; 1,65. Выбор свидетеля - кислоты глютаминовой - обусловлен тем, что она содержится в сырье в наибольшем количестве.
Нами разработаны условия спектрофотометрического определения аминокислот в траве овса посевного. Исследования проводили на спектрофотометре СФ-56 в кюветах с толщиной слоя 10 мм. Выбирали оптимальное количество 1% раствора нингидрина, концентрацию раствора натрия карбоната (0,25%, 0,05% и 0,025%) и его объем, а также время нагревания на водяной бане. Кроме того, установлено положение максимума светопоглощения (570-590 нм) и пределы концентраций подчинения закону Бугера-Ламберта-Бера (0,01-0,06 мг/мл). Результаты выбора оптимальных условий реакции с нингидрином приведены в таблице 1.
Таблица 1
Оптимальные условия реакции с нингидрином
|
Условия реакции |
Показатели |
|
1. Концентрация раствора натрия карбоната |
0,25% |
|
2. Объем раствора натрия карбоната |
1 мл |
|
3. Объем 1% раствора нингидрина в 95% этаноле |
2 мл |
|
4. Время нагревания |
10 минут |
|
5. Концентрация стандартного раствора кислоты глютаминовой |
0,05% |
|
6. Максимум светопоглощения |
570-590 нм |
|
7. Пределы подчинения закону Бугера-Ламберта-Бера |
0,01-0,06мг/мл |
Для построения калибровочного графика в мерные колбы вместимостью 50 мл помещали 1, 2, 3, 4, 5, 6 мл 0,05% стандартного раствора кислоты глютаминовой (РСО), добавляли 1 мл 0,25% раствора натрия карбоната, 2 мл 1% раствора нингидрина в 95% спирте этиловом, нагревали 10 мин на кипящей водяной бане, охлаждали, доводили водой до метки. Измеряли оптическую плотность на спектрофотометре СФ-56 при длине волны 570 нм в кювете толщиной 1 см относительно воды. Методика определения суммы аминокислот в траве овса посевного Около 1 г (точная навеска) измельченного сырья помещают в коническую колбу вместимостью 200 мл со шлифом, прибавляют 100 мл 70% спирта этилового. Колбу закрывают пробкой, взвешивают с погрешностью 0,01 г, присоединяют к обратному холодильнику и нагревают на водяной бане в течение 1 часа. Затем колбу охлаждают до комнатной температуры, взвешивают, доводят массу до первоначальной 70% спиртом этиловым, извлечение фильтруют.
2 мл извлечения помещают в мерную колбу вместимостью 50 мл, прибавляют 1 мл 0,25% раствора натрия карбоната, 2 мл 1% раствора нингидрина в спирте 95% и нагревают 10 минут на кипящей водяной бане, охлаждают, доводят водой до метки. Параллельно в мерную колбу вместимостью 50 мл помещают 1 мл раствора РСО кислоты глютаминовой (0,05%) и поступают, как указано выше. Оптическую плотность полученных растворов измеряют на спектрофотометре при 570 нм в кювете с толщиной слоя 10 мм относительно воды. Содержание суммы аминокислот в сырье в процентах (Х) в пересчете на кислоту глютаминовую рассчитывают по формуле:
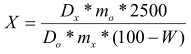 , где
, где
Dx - оптическая плотность испытуемого раствора,
D0 - оптическая плотность раствора РСО кислоты глютаминовой,
m0 - навеска РСО кислоты глютаминовой, г,
mx - навеска сырья, г,
W - потеря в массе при высушивании сырья, %.
Таблица 2
Результаты определения суммы аминокислот в траве овса посевного
|
Dx |
Навеска, г |
Найдено, % |
Метрологические характеристики |
|
0,141 |
1,0150 |
0,96 |
Х = 0,97 |
|
0,152 |
1,0098 |
1,03 |
Σ(Х-Х)2 = 0,0076 |
|
0,131 |
0,9931 |
0,91 |
S = 0,039 |
|
0,140 |
0,9854 |
0,98 |
Sx = 0,0159 |
|
0,139 |
0,9904 |
0,97 |
Δ = 0,41 |
|
0,143 |
0,9998 |
0,99 |
ε = ±4,22% |
Выводы
Изучен химический состав травы овса посевного. Качественными реакциями обнаружены аминокислоты, крахмал и флавоноиды.
Разработана методика спектрофотометрического определения суммы аминокислот по реакции с нингидрином. Установлено, что в траве овса содержится до 1% аминокислот в пересчете на кислоту глютаминовую.
СПИСОК ЛИТЕРАТУРЫ
- Казаков А.Л., Хацуков Б.Х. Биологически активные вещества целебных и пищевых растений и их фармакологическая активность.- Нальчик: Изд. КБНЦ РАН, 2000. - 68 с.
- Методы биохимического исследования растений под ред. А.И. Ермакова. - Л.: Агропромиздат, 1987. - 430 с.
- Молчанов Г.И., Молчанова Л.П., Гулько Н.М., Молчанов А.Г., Сулков И.Ф. Съедобные целебные растения. Изд. Ростовского университета, 1994. - С. 202.
- Растительные ресурсы. Рос. Академия наук. - С-Пб.: Наука, 1994. - С. 117.
- Химический анализ лекарственных растений под ред. Н.И. Гринкевича, Л.Н. Сафронича. - М.: Высш. школа, 1983. - 176 с.
Библиографическая ссылка
А.Ю. Куль, М.Ф. Маршалкин, М.В. Гаврилин, И.Я.Куль ИЗУЧЕНИЕ ХИМИЧЕСКОГО СОСТАВА И СПЕКТРОФОТОМЕТРИЧЕСКОЕ ОПРЕДЕЛЕНИЕ АМИНОКИСЛОТ В ТРАВЕ ОВСА ПОСЕВНОГО // Успехи современного естествознания. 2002. № 2. С. 6-9;URL: https://natural-sciences.ru/ru/article/view?id=13954 (дата обращения: 03.06.2026).



