Согласно проведенным исследованиям, в настоящее время по частоте возникновения желчнокаменная болезнь выходит на первое место среди заболеваний пищеварительной системы. В России частота желчнокаменной болезни находится на уровне среднеевропейских показателей – около 10 %. Заболеваемость населения Тверской области по отдельным классам болезней: болезни органов пищеварительного тракта (таблица и диагр. 1).
Болезни органов пищеварения
|
Год |
2000 |
2005 |
2007 |
2008 |
2009 |
2011 |
|
Тыс. чел. |
37431 |
35032 |
44461 |
46076 |
58037 |
55380 |
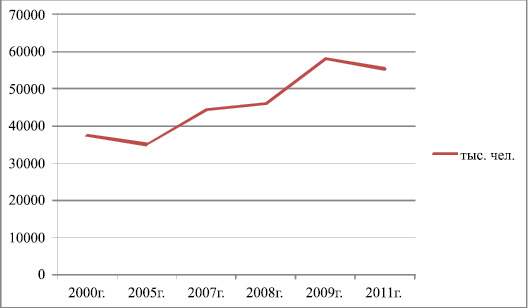
Диаграмма 1
Заболеваемость населения (по основным классам болезней) по некоторым регионам Центрального Федерального округа в 2010 году: в Тверской области на 1000 населения всего: 922,9, из них 40,8 – болезни органов пищеварительного тракта, т.е. 4,42 %. [1] Отметим только, что это лишь число зарегистрированных случаев желчнокаменной болезни (ЖКБ). В большинстве случаев болезнь на начальных стадиях протекает бессимптомно и обнаруживается случайно при ультразвуковом исследовании органов брюшной полости по поводу сопутствующего заболевания. Поэтому, реальное число больных ЖКБ значительно больше. Течение ряда заболеваний сопровождается холелитиазом. При циррозах печени желчные камни выявляют у 30 % больных. Высказывается мнение, что лица с HbsAg имеют повышенный риск образования желчных камней. Заболевания тонкой кишки с локализацией патологического процесса в терминальном отделе приводят к нарушению энтерогепатической циркуляции желчных кислот и, как следствие, к дисхолии. При болезни Крона с преимущественной локализацией в терминальном отделе тонкой кишки частота камнеобразования достигает 26,4 %. При этом нет различия в частоте формирования желчных камней между мужчинами и женщинами, а также характерной для ЖКБ возрастной зависимости [16]. На степень риска камнеобразования влияют локализация и обширность резекции тонкой кишки по поводу различных заболеваний. Субтотальная и тотальная гемиколэктомия также увеличивает риск образования желчных камней. При синдроме нарушенного всасывания тяжелой степени (глютеновая энтеропатия, резекции тонкой кишки, болезнь Крона и др.) изменяются все основные виды обмена, в том числе и всасывание желчных кислот, что способствует камнеобразованию.
После 40 лет желчные камни находят у 32 % женщин и 16 % мужчин, при этом в 30 % случаев отмечают инфицирование желчи. В основе камнеобразования лежит нарушение равновесия между стабилизаторами желчи (желчные кислоты и лецитин) и количеством растворенных в ней веществ (карбонат кальция, билирубин и холестерин). Матрицей для камнеобразования являются белки желчи, кристаллы холестерина или билирубина. Одним из наиболее значимых и идентифицированных пронуклеаторов является муцин-гликопротеиновый гель. Следует отметить, что в норме муцин постоянно секретируется слизистой оболочкой желчного пузыря, однако его секреция повышается при наличии литогенной желчи. К белкам, ускоряющим осаждение холестерина, кроме муцина относят N-аминопептидазу, кислый α1-гликопротеин, иммуноглобулины, фосфолипазу С; к антинуклеаторам – аспирин и другие НПВС. Аполипопротеины А1 и А2 замедляют осаждение холестерина. При этом похудание сопровождается увеличением содержания муцина и кальция в пузырной желчи и тем самым способствует образованию желчных камней. [2, 6, 7, 16]
Желчные камни – плотные конкременты, образующиеся в желчном пузыре и желчных протоках. Они бывают размером от песчинки (рис. 1) до куриного яйца (рис. 2).

Рис. 1. Множественные, мелкие желчные камни смешанного типа

Рис. 2. Множественные, крупные желчные камни с темным ядром

Рис. 3. Множественные, крупные желчные камни однородной структуры
В центре камня в большинстве случаев находится холестерин, реже – слущенный эпителий стенки пузыря, пропитанный солями кальция, магния, пигментом и белками [6, 9].
По составу желчные камни делятся на холестериновые, пигментно-холестериновые, сложные холестерино-пигментные-известковые, пигментные и известковые [10].
Холестериновые камни состоят в основном из холестерина с незначительной примесью белка, извести и пигментов. Эти камни чаще округлой формы, белесовато-желтоватого цвета, гладкие, легкие, плавают в воде, легко горят и сгорают без остатка. Чистый холестериновый камень может превратиться в пигментно-холестериновый и холестерино-пигментно-известковый, однако центральная часть его всегда состоит из чистого холестерина. Сложные холестерино-пигментно-известковые камни – наиболее частый вид желчных камней. Они имеют цвет от белесовато-сероватого до черного. Ядро их состоит из пигментов и холестерина. Пигментные камни чаще всего образуются вследствие застоя желчи в печени, внепеченочных желчных путях. Они множественные, мелкие, диаметром до 1-1,5 см, мягкой консистенции, на разрезе гомогенны, буровато-черного цвета. Зачатки этих камней образуются во внутрипеченочных желчных ходах в виде белковой основы, желчных пигментов и незначительной примеси известковых солей [8, 9]. Известковые камни – плотные белесоватые бугристые образования. Эти камни встречаются очень редко [6, 7, 8, 9].
Известно, что желчные камни обладают кумулятивными свойствами, т.е. способны накапливать вещества, содержащиеся в окружающей среде даже в незначительных количествах [2, 8]. В настоящее время в подавляющем большинстве случаев диагностирования желчнокаменной болезни назначается оперативное лечение, и конкременты, изъятые из желчного пузыря, становятся доступными для исследования лишь по прошествии операции, поэтому их химическому анализу практически не уделяется внимания. В то же время, их состав мог бы служить дополнительным диагностическим тестом при определении характера нарушения обмена веществ и определения постоперативного лечения прооперированных пациентов, что может помочь в поиске новых, нехирургических методов лечения или предотвращения желчнокаменной болезни.
К числу веществ, способных растворять выпадающие в водных средах осадки, а также предотвращать их выпадение, относятся комплексоны. [11] Химические и физические свойства комплексонов хорошо изучены, однако мало исследована их биологическая активность.
Комплексоны – органические вещества (главным образом аминополикарбоновые кислоты и их соли), образующие с ионами металлов стойкие водорастворимые комплексы.
Комплексы с ионами кальция, магния и других металлов безвредны для человека и других живых существ и растворимы в воде. Самым известным из комплексонов является этилендиаминтетрауксусная кислота (ЭДТУК). В последние десятилетия наряду с ЭДТУК в возрастающих масштабах используется ее более новый экологически безопасный аналог – этилендиаминдиянтарная кислота (ЭДДЯК).
На первом этапе представленного исследования была предпринята попытка растворения желчных камней в растворах комплексонов: ЭДТУК и ЭДДЯК, подщелоченных NaOH до рН=5,6. Навески желчных камней, по внешнему виду отнесенных к трем разным типам, помещали в 0,05М растворы ЭДТУК и ЭДДЯК (рис. 4).

Рис. 4. Желчные камни в растворах комплексонов:1.1, 1.2, 1.3 – раствор ЭДТУК; 2.1, 2.2, 2.3 – раствор ЭДДЯК
Как и предполагалось, холестерино-пигментные камни ни через 7 дней, ни через месяц не претерпели видимых изменений (рис. 5).

Рис. 5. Холестерино-пигментные камни в растворах ЭДТУК (1.1) и ЭДДЯК (2.1) через месяц
Уменьшились в размерах или распались на части лишь смешанные камни со значительной минеральной составляющей (рис. 6).

Рис. 6. смешанные камни в растворах ЭДДЯК(2.2, 2.3) через месяц
При этом возник вопрос о том, какова частота образования конкрементов с неорганической составляющей и какие металлы, способные хелатироваться комплексонами, входят в их состав. С этой целью по стандартным методикам была определена зольность образцов желчных камней тридцати пациентов, прооперированных в Первом хирургическом отделении Областной клинической больницы (ОКБ) г. Твери в октябре 2010 года.

Рис. 7. Зольные остатки желчных камней
Зольность образов представлена на диаграмме 2.
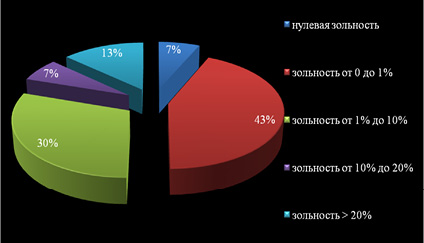
Диаграмма 2. Уровень зольности образцов желчных камней (ω, %)
Зольные остатки (рис. 7) были растворены в концентрированной азотной кислоте и проанализированы методом комплексонометрического титрования на содержание Ca2+, Mg2+ [12]. Конкременты с высоким содержанием Ca2+, Mg2+ были растворены в растворе лимонной кислоты. Растворимость желчных камней смешанного типа с высоким содержанием минеральной составляющей в растворе лимонной кислоты оказалась выше чем в растворах комплексонов, но в то же время раствор лимонной кислоты имеет сильнокислую среду (рН), поэтому его использование в качестве растворителя не представлялось возможным для расстворения желчных камней у больных ЖКБ.
Лимонная кислота, являющаяся естественным метаболитом и важнейшим звеном цикла тканевого дыхания, давно известна и хорошо изучена. В присутствии кальция лимонная кислота образует с ним устойчивый комплекс – цитрат кальция, который растворим в воде, и легко усваивается организмом человека. Выведение кальция и его соединений, магния и других металлов из состава камней приводит к их распаду [2, 3].
Быстрый метаболизм и поглощение тканями лимонной кислоты, сильнокислая pH среды раствора, большая потребность в ней других тканей – делают невозможным доставку лимонной кислоты до печени и желчного пузыря для растворения желчных камней, поэтому она не могла использоваться ранее для эффективного лечения ЖКБ.
Предлагаемая нами, липосомальная форма лимонной кислоты позволяет доставить лимонную кислоту практически в неизмененном виде до клеток печени и, соответственно, до желчи. Липосомальные препараты представляют собой липидные везикулы размером порядка 100 нанометров из одного или нескольких слоев фосфолипидов, содержащие действующее лекарственное начало и водную фазу. Липосомы относятся к системам пассивной адресной доставки, так как обладают высокой тропностью (более 80 %) к органам ретикулоэндотелиальной системы (РЭС), т.е. к печени и селезенке. Такая форма позволяет применять препарат как через желудочно-кишечный тракт (ЖКТ), так и парентерально, так как не меняет pH среды, защищает слизистые ЖКТ от кислой среды лимонной кислоты за счет фосфолипидной оболочки.
При любом виде введения (перорально или парентерально), липосомы стремительно доставляют вещество в тропные органы (печень – через 15 мин.) и постепенно распадаются уже в клетках органа, что обеспечивает быстрое и пролонгированное действие вещества. В клетке печени липосома распадается и высвобождает лимонную кислоту. часть лимонной кислоты используется непосредственно самой клеткой для процессов клеточного метаболизма, часть – поступает в желчь и с ней в желчный пузырь. Также, часть фосфолипидов, образующих липосомы, при распаде в клетках печени не разрушаются, а встраиваются в поврежденные участки клеточной стенки, обеспечивая тем самым гепатопротекторный эффект, обновляют клеточную стенку, достраивают поврежденные участки.
Массовые доли металлов ( %), обнаруженных в желчных камнях с зольностью >1 %, (№ 16–№ 30) представлены на диаграмме 3.
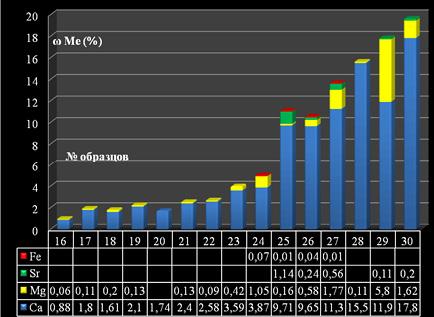
Диаграмма 3. Содержание металлов в желчных камнях с зольностью >1 %
Образцы с зольностью >10 % были проанализированы на содержание Sr2+. Присутствие Ca2+ было обнаружено в 28 образцах из 30-ти, Mg2+ – в 27, Sr2+ – в 5-ти. Все 28 образцов с зольностью >0 были проанализированы на содержание железа. Этот металл был обнаружен и количественно определен фотометрически (фотометр КФК-3) в форме роданидного комплекса лишь в 4-х образцах желчных камней. В конкрементах из всех 4-х обнаруженных металлов преобладает Ca2+ , в меньшем количестве содержится Mg2+. В конкрементах с высокой зольностью содержатся десятые доли процента Sr2+ (лишь в 1-м образце >1 %), что может служить доказательством гипотезы о выведении части Sr2+, поступающего с пищей (0,8-3 мг/сут.) не только через почки, но и с желчью.[4] По-видимому, в некоторых случаях желчные камни могут кумулировать Sr2+.
Железо, обнаруженное в 4-х образцах, содержится в сотых долях процента.
На следующем этапе исследования был проведен анализ органической составляющей камней с помощью методов ИК-спектроскопии (инфракрасной спетроскопии). Инфракрасная спектроскопия с использованием специального прибора (Thermo scientific iS10 Nicolet с приставкой Smart iTR с кристаллом ZnSe) является одним из методов исследования состава сложных многокомпонентных веществ, биосубстратов и биологических жидкостей которые не требуют предварительной длительной подготовки исследуемой пробы.
Образцы высушенных желчных камней растирали в агатовой ступке до получения однородной смеси (рис. 8).

Рис. 8. Растертый в агатовой ступке желчный камень
Полученные на спектрах пики совмещены с возможным химическим составом. Анализ спектров показал (рис. 9) наличие холестерина, характеризующегося большими растяжениями полос О-Н групп 3365,4 см-1, С-Н валентные колебания 2933 см-1, СН симметричное растяжение СН3 2899 см-1, СН симметричное растяжение СН2 2865 см-1, СН изгиб СН2 1462 см-1 связан с деформацией кольца холестерина. Кальция билирубинат имеет характерные полосы 1254 см-1, это характерные растяжения СОС, ССН в плоскости изгиба 1222. 5 см-1. Пики на 984 свидетельствуют о наличии виниловых полимеров, например, билирубина. Наличие апатитов характеризуется пиками 1228 см-1. Апатиты относятся к классу фосфатов. Карбонаты кальция – 1438 см-1, СО изгиб в СаСО3 – 838 см-1. Карбонаты кальция имеют три естественных полиморфных состояния: кальцит (1438 см-1), арагонит(699 см-1), фатерит(740 см-1). Фосфаты – 1248 см-1. Наличие амид I подтверждается в области 1650 см-1, амид II 1544 см-1. Наличие Амидных связей, свидетельствует о присутствии в составе исследуемой пробы белковых структур. Спектральные характеристики моногидрата оксалата кальция найдены в камнях на 882 см-1[13, 15]. Полученные спектры дают возможность охарактеризовать желчные камни по преобладанию в их составе тех или иных веществ и разработать в дальнейшем приемлемую тактику консервативного лечения ЖКБ.
Так, например, при больших пиках холестерина на спектре целесообразно использовать для консервативной терапии ЖКБ препараты производных желчных кислот (ХДХК, ДХК). А при наличии пиков минеральных компонентов консервативная терапия этими препаратами противопоказана. Исходя из вышесказанного, разработка липосомальной формы лимонной кислоты – как растворителя желчных камней смешанного типа, откроет в будущем широкие возможности для консервативного лечения ЖКБ при диагностировании минеральных и смешанных камней со значительной минеральной составляющей.
Концентрация вещества определяется по площади пика [14].
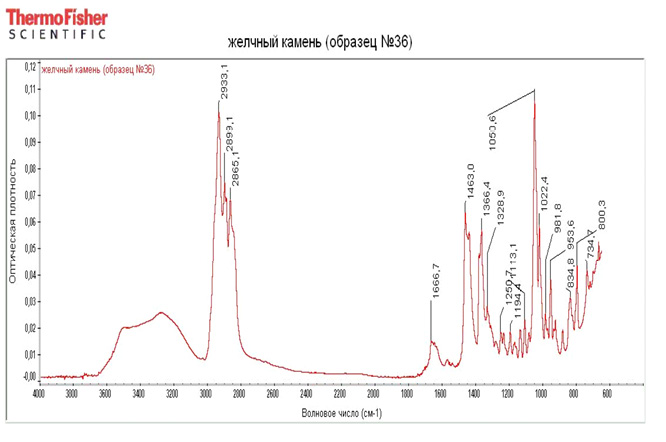
Рис. 9. инфракрасный спектр образца желчного камня № 36 с обозначенными пиками. Число сканов пробы: 64. Число сканов сравнения: 64. Разрешение: 4,000 см-1. Усиление: 8,0. Скорость зеркала: 0,4747. Диафрагма: 80,00. Проведена коррекция базовой линии
Таким образом, 50 % проанализированных нами желчных конкрементов с зольностью <1 % – холестериновые камни. Их образование связано с нарушением холестеринового обмена в организме. Консервативное лечение при таком типе ЖКБ возможно препаратами производных желчных кислот. Неорганическая составляющая желчных камней помимо Ca2+ и Mg2+ может содержать ионы Fe и Sr, что может служить доказательством теории о кумулятивных свойствах желчных камней и гипотезы о выведении Sr не только через почки, но и через билиарный тракт. Способность комплексонов растворять минеральную составляющую желчных камней может быть исследована в качестве одного из компонентов препарата для консервативного лечения ЖКБ при камнях смешанного типа со значительной минеральной составляющей. Растворяющая способность лимонной кислоты при воздействии на желчные камни смешанного типа с незначительной минеральной составляющей может быть использована для разработки препарата липосомальной формы лимонной кислоты с пассивной адресной доставкой лимонной кислоты до органов РЭС (печень и селезенка) и ее преимущественной концентрацией в печени и соответственно в желчи. Создание такого препарата позволит использовать консервативную терапию при большом числе случаев ЖКБ со смешанным типом камней и существенно уменьшит число оперативных вмешательств по поводу ЖКБ.
Разработка и исследования липосомальной формы лимонной кислоты – предмет следующего этапа исследований в этом направлении.
Библиографическая ссылка
Азатян К.А., Алексеев А.В., Зубарева Г.М. ИССЛЕДОВАНИЕ СОСТАВА ЖЕЛЧНЫХ КАМНЕЙ И СПОСОБОВ ИХ РАСТВОРЕНИЯ // Успехи современного естествознания. 2013. № 9. С. 12-17;URL: https://natural-sciences.ru/ru/article/view?id=32754 (дата обращения: 16.05.2026).



