Известно, что расходы на лечение миеломной болезни велики, а смертность при миеломе, тем не менее, высокая, лечение малоэффективное [13, 16, 19, 21]. Слизистая оболочка полости рта подвергается высокой антигенной нагрузке, при этом в первую очередь вредным влияниям подвергаются кератиноциты, а от их функциональной лабильности зависит уровень резистентности организма к повреждаемым агентам [17]. В настоящее время практически отсутствуют данные об изменениях клеточного состава эпителиальных пластов слизистой оболочки протезного ложа и иммунного контроля этого процесса в условиях протезирования у больных миеломой, отсутствуют данные о механизмах остеонекроза челюстей на фоне приёма бисфосфонатов [6, 11, 26]. На современном этапе имплантирование зубов у стоматологических больных на фоне миеломы имеет абсолютное противопоказание при остеонекрозе челюстей [9]. При этом клиническая картина характеризуется появлением оголённых альвеолярных костей, зияющей и длительно незаживающей лункой зуба в случае его удаления, болезненной инфильтрацией, различной степенью нарушения физиологической функции [5]. Это связано с токсичностью бисфосфонатов, которая проявляется через механизм воздействия бисфосфонатов после проникновения в костную ткань и взаимодействие с кристаллами гидроксиапатита; создание высокой концентрации в лакунах резорбции и вокруг остеокластов, нарушение формирования цитоскелета остеокластов; снижение секреции лизосомальных ферментов остеокластами; подавление передачи межклеточных сигналов; ингибирование миграции остеокластов и их резорбтивной способности, подавление адгезии опухолевых клеток, а также нарушение формирования цитоскилета остеокластов [2, 7]. Бисфосфонаты оказывают целенаправленное воздействие на костную ткань в зонах, имеющих высокую скорость резорбции и регенерации [18]. Они тормозят резорбцию кости путем уменьшения активности и количества остеокластов за счет влияния на их способность к адгезии, подвижности, цитологической структуры, дифференциации длительности жизни [11]. Также бисфосфонаты оказывают стимулирующее влияние на остеобласты и макрофаги [20]. В исследованиях in vitro было установлено, что золедроновая кислота, подавляя пролиферацию и индуцируя апоптоз, оказывает непосредственное противоопухолевое действие на клетки миеломы человека и рака молочной железы [15]. Кроме этого, бисфосфонаты приводят к снижению кровотока в костной ткани, через эффект ингибирования ангиогенеза путем накопления HIF1a и снижения экспрессии VEGF [8, 27, 28]. В ряду этих препаратов можно выделить Зомету – препарат золедроновой кислоты, бисфосфонат IV поколения, противорезорбционная активность которой превыщает первые бисфосфонаты более чем в 1000 раз. При этом совершенно не учитывается тот факт, что при остеонекрозе челюстей слизистая оболочка над поверхностью кости нарушена полностью, отсутствует не только покровный эпителий, но и собственная пластинка [1]. Всё это свидетельствует, прежде всего, о том, что идёт тяжёлое нарушение эпителиально-мезенхимных взаимоотношений, взаимного индукторного и ингибиторного альянса клеточных ансамблей и нарушение барьерных свойств эпителия в зоне патологического процесса [9]. В доклинический период остеонекроза челюстей явления эпителиальной деструкции, некроза и апопотоза проходят незамеченными [22, 27]. Но именно они могут быть причиной инфицирования и деструкции костной ткани, а не только очаги плазмацитопоэза и влияние запуска реминерализации кости из-за влияния фосфорных соединений [29]. Как профессиональные вредности, так и всюду в медицине, где патология (рак молочной железы, рак простаты, наркология) связана с применением фосфорсодержащих препаратов, отмена лекарственных средств должна быть не в связи с появлением болевого синдрома и некротических проявлений в костной ткани челюстей, а построена на основе объективных диагностических критериев.
Несмотря на то, что больные миеломой выявляются с частотой 4-5 случаев на 100000 населения, (в США 50000 больных миеломой) проблема механизмов патогенеза и профилактики остеонекрозов челюстей и эффективной стоматологической помощи, продления жизни на качественном уровне является одной из актуальнейших задач [3, 26]. При этом в авангарде разработки профилактических в отношении осложнений мероприятий оказываются иммуногистохимические методы диагностики, которые имели бы значение не только для научных разработок, но и реализовывались в практическом здравоохранении [12].
Таким образом, изучение всех составляющих иммунного гомеостаза слизистой оболочки полости рта больных миеломой чрезвычайно важно для понимания его механизмов, планирования лечебных мероприятий и реабилитации стоматологических больных на фоне миеломы при использовании как традиционных, так и новых методов протезирования, включая дентальную имплантацию.
Цель исследования: повышение качества и эффективности стоматологического консервативного и хирургического лечения больных миеломой путём оптимизации диагностического ресурса, врачебной тактики, профилактики и устранения осложнений терапии.
Материалы и методы исследования
Материалом для исследования послужили биоптаты слизистой оболочки протезного ложа десны больной миеломой, в возрасте 56 лет, наблюдающейся у стоматолога в течение 10 лет. После удаления пластмассового протеза пациентка обследована согласно протоколу с заполнением медицинской карты стоматологического больного формы № 043/у. При клиническом осмотре использовали индекс гигиены полости рта Силнес–Лое, индекс подвижности зубов Миллера, индекс кровоточивости десен Мюллемана с целью определения степени выраженности воспалительных явлений в пародонте. При клиническом обследовании регистрировали наличие очагов гиперемии, отечности протезного ложа. Для оценки состояния тканей пародонта использовались пробу Шиллера–Писарева. Весь спектр клинических обследований слизистой оболочки протезного ложа проводился в динамике – в процессе удаления у пациентки ортопедической конструкции из пластмассы, удаления по клиническим показаниям зуба и подготовки протезного ложа десны к имплантированию.
Для гистологического исследования при удалении зуба и его корня, имплантации во время проведения микрохирургических пародонтологических операций по клиническим показаниям иссекались фрагменты слизистой оболочки десны объемом 0,3мм3. Забор материала производился через 1, 3, 6 месяцев после удаления ортопедической конструкции и введения импланта, всего изучено 6 биопсий, изготовлено 62 среза.
Основным методом морфологического исследования явилось иммуногистохимическое фенотипирование на основе кластеров дифференцировки (Cluster of Differentiation – CD) СD5 и выявление активности белка р53, известного как белка антионкогена, индуктора апоптоза. Интенсивность пролиферативных процессов в эпителиальной пластинке оценивалась по митотическому индексу посредством маркера Ki-67: количество митозов на 100 клеток. Иммуноморфологическое исследование проводили в лаборатории патоморфологии университета г. Ниигата (Япония).
Кроме того, при анализе биопсий использовалась рутинные методики (окраска гематоксилином и эозином) Victoria blue по классическим протоколам исследований.
Изучение гистологических срезов и мазков-отпечатков осуществлялось с помощью микроскопа Olympus BX52 с оригинальным программным обеспечением для морфометрии.
Морфометрическая обработка полученных данных, проверка статистической значимости различий между группами по параметрам распределения и сравнение групп выборок проведено с применением методов вариационной статистики, параметрических и непараметрических методов корреляционного анализа.
Результаты исследования и их обсуждение
При изучении срезов биоптатов слизистой оболочки десны на фоне миеломы установлено, что слизистая оболочка гипертрофирована, гиперемирована, инфильтрирована не только в пределах соединительнотканной пластинки, но лейкоцитарная инфильтрация наблюдается в эпителиальной пластинке, достигая верхних слоёв шиповатого слоя (рис. 1а, б). При окрашивании методом Victoria blue установлено, что коллагеново-волокнистая составляющая соединительной ткани десны на фоне миеломной болезни ослаблена, в дерме присутствует незначительное количество коллагеновых волокон, при этом достоверно отмечается усиление эластического волокнистого каркаса кровеносных сосудов (рис. 2 в, г). В наших данных, как и по результатам Saito M. et al. (2014), это свидетельствует о том, что в патогенетической цепи изменений слизистой оболочки на фоне миеломной болезни в собственно соединительнотканной пластинке происходят качественные изменения с уменьшением и замещением коллагеново-волокнистого компонента на эластический [23]. Это может играть роль адаптации структур слизистой оболочки на изменяющиеся барьерные свойства поверхностных структур десны для предупреждения микробной контаминации в кровеносные сосуды и миграции лейкоцитов из просвета сосудов. По нашему мнению, такая перестройка способна оказывать влияние на сосудистые реакции в условиях имплантирования, а также опосредованно вследствие изменившихся условий проницаемости сосудистой стенки на противорезорбционную активность бисфосфонатов.
Наши исследования показали, что CD5 клетки располагаются в рыхлой волокнистой соединительной ткани сосочкового слоя слизистой оболочки десны, и лишь в небольшом количестве среди кератиноцитов (рис. 2 а-г). Учитывая то, что лимфоцитарный рецептор (T1) – мембранный белок , экспрессирован на поверхности T-лимфоцитов и B-лимфоцитов подгруппы B-1а, регулирует пролиферацию T-лимфоцитов, миграция CD5 преимущественно в соединительнотканную пластинку свидетельствует о нарушении пролиферации лимфоцитов в необходимом для запросов иммунитета направлении, а, следовательно, и адекватной дифференцировки, так как следствием выселения CD5 из эпителиального пласта является выключение его участия в повышении выживаемости T- и B-лимфоцитов подгруппы B-1а [14, 25]. CD5 относится к скавенджер-рецепторам суперсемейства SRCR и обеспечивает модулирование сигнального пути антигенного рецептора, что является причиной последующих индукционных влияний для усиления воздействия неблагоприятных факторов при неправильном перераспределении иммуноцитов. В результате того, что CD5 является ингибиторным рецептором, снижая FasL, способствует тому, что ингибирование активности каспазы 8 не происходит в полной мере. По нашим данным, в связи с нарушением представительства CD5 в эпителиальных пластах, в целом нарушается и антиген представление, т.к. мембранный белок CD5 является рецептором для PAMP (патоген-ассоциированных молекулярных образов).
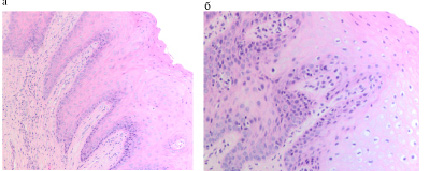
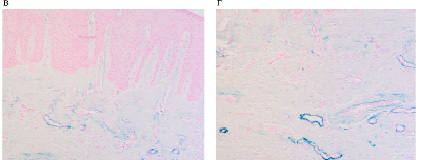
Рис. 1. Слизистая оболочка женщины 56 лет больной миеломой: а, б – утолщение слизистой оболочки, гипертрофия, гиперемия, инфильтрация. Отмечается окрашивание эластических волокон в пределах мелких кровеносных сосудов сосочкового и в большей степени немногочисленных сосудов сетчатого слоя. Микрофото. А,б-окр. гематоксилин-эозином; в, г-окр. Victoria вlue. Ув. а, б, в Х200; г Х400
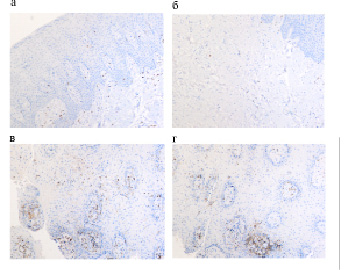
Рис. 2. Слизистая оболочка протезного ложа десны больной миеломой. Иммунная гистохимия. СD5 располагаются преимущественно в собственной пластинке слизистой оболочки десны. Микрофото. Ув. х400
При изучении сравнительной характеристики пролиферативной активности кератиноцитов в срезах биоптатов контроля и биптатов слизистой оболочки на фоне миеломной болезни выявлено усиление пролиферативной активности не только клеток базальных слоёв, но и высокая активность гена белка Ki-67 в слоях шиповатого слоя, прилежащих к базальной мембране.
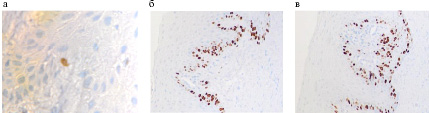
Рис. 3. Десна группы контроля (а) и десна на фоне миеломной болезни (б, в). Отмечается усиленная пролиферативная активность кератиноцитов на фоне миеломной болезни
Повышение пролиферативной активности свидетельствует о снижении барьерных свойств эпителиоцитов, необходимости замещения покровных клеток новыми. Остаётся открытым вопрос о возможности полноценной дифференцировки и специализации кератиноцитов для выполнения полноценной регенерации с закрытием дефекта и выполнением защитных свойств.
На основании результатов морфологического исследования биоптатов слизистой оболочки протезного ложа пациентов контрольной группы была составлена модель, характеризующая нормальное состояние локального иммунного гомеостаза у практически здоровых людей в сравнении со слизистой оболочкой биоптатов больной миеломой, взятых в динамике наблюдения (табл. 1).
Таблица 1
Показатели иммунного гомеостаза слизистой оболочки протезного ложа в норме и при миеломе -
|
Возраст |
Кол-во клеток в поле зрения (M±m) |
Распределение эластических и коллагеновых волокон |
МИ |
|
CD5 |
|||
|
56 в норме |
0,80±0,02 |
Равномерно в соединительной ткани |
5,18±0,18 |
|
56 лет на фоне миеломы |
3,8±0,06 |
Немногочисленны в соединительной ткани, преобладают вокруг кровеносных сосудов |
3,2±0,09 |
*Доверительный интервал р<0,01.
Выводы
1. В патогенетических процессах в слизистой оболочке больных миеломной болезнью принимают участие CD5 клетки, миграция которых за пределы эпителия в соединительную ткань снижает дифференцировку лимфоцитов, снижает эффективность антигенпредставления и нарушает индукцию иммунного ответа. 2. Морфологические изменения сопровождаются увеличением эластического компонента соединительной ткани вокруг кровеносных сосудов и уменьшением его в окружающей сосуд ткани. 3 Выявлена роль иммунокомпетентных CD5 клеток слизистой оболочки полости рта как важного прогностического критерия в патогенезе миеломной болезни. 4. Материалы исследования являются основой для разработки дополнений в алгоритмы обследования стоматологических больных на фоне миеломной болезни, нуждающихся в ортопедическом лечении, что реально способствует повышению качества оказываемой ортопедической помощи и эффективности работы врача стоматолога. 5. По результатам исследования обоснована необходимость комплексной диагностики локального иммунного статуса у стоматологических пациентов.
Работа выполнена при поддержке научного фонда ДВФУ, в рамках государственного задания 2014/36 от 03.02.2014 г. и Международного гранта ДВФУ (соглашение № 13-09-0602-м от 6 ноября 2013 г.).
Библиографическая ссылка
Рева И.В., Рева Г.В., Ямамото Т., Усов В.В., Русакова Е.Ю., Толмачёв В.Е., Ким А.Р., Бочаров В.С., Калинин О.Б., Разумов П.В., Калинин И.О., Грахова Н.В. ПАТОГЕНЕТИЧЕСКИЕ АСПЕКТЫ ОСТЕОНЕКРОЗА ЧЕЛЮСТЕЙ ПРИ МИЕЛОМНОЙ БОЛЕЗНИ // Успехи современного естествознания. 2014. № 12-4. С. 345-351;URL: https://natural-sciences.ru/ru/article/view?id=34609 (дата обращения: 07.05.2026).



