В последнее время полифенолы, в частности флавоноиды, привлекают внимание исследователей своим разносторонним фармакологическим влиянием на организм животных и человека.
Проведен корреляционный анализ «структура химического вещества – биологическая активность» в ряду синтезированных производных халконов и 3-феноксикумаринов на основе современной системы с использованием математического алгоритма. Рассмотрена связь биологической активности вещества с его структурой с точки зрения вклада неизменной части молекул (ядра) и вклада заместителей с учетом их положения.
Между биологической активностью вещества и его структурой имеется, как известно, функциональная связь в статистическом смысле [1]. Для описания зависимости «структура – активность» применяются регрессионные методы, основанные на статистическом анализе результатов эксперимента, целью которого является получение математической модели активности с некоторыми характеристиками вещества на такие составляющие, как вклады ядра (неизменной части рассматриваемых веществ) и заместителей с учетом их положения. Для этого используют новые современные системы, позволяющие осуществить прогноз спектра биологической активности вещества на основе его структурной формулы, включая фармакологические эффекты и механизмы действия [7]. Поэтому в нашей работе использована программа PASS (http://www.ibmh.msk.su/PASS) – Prediction of Activity Spectra for Substances (программа для предсказания спектра биологической активности веществ) [7], позволяющий прогнозировать большое число вероятных видов биологической активности вещества на основе его структурной формулы с использованием единого описания химической структуры и универсального математического алгоритма установления зависимостей «структура – активность». Средняя точность прогноза составляет около 95 %.
Сущность этой программы заключается в изучении связи активности вещества с его физико-химическими параметрами. Биологическая активность описывается в PASS С&Т качественным образом («да»/«нет»). Выдаваемые результаты прогноза помимо названий активности включают в себя оценки вероятностей (Ра) «быть активными» и вероятность (Рi) «быть неактивной», имеющие значения от 0 до 1. Поскольку эти вероятности рассчитываются независимо, их сумма не равна единице.
Используемый в PASS математический алгоритм был отобран путем целенаправленного анализа и сравнения эффективности для решения подобных задач большого числа различных методов. Показано, что данный алгоритм обеспечивает получение устойчивых в статистическом смысле зависимостей «структура – активность» и, соответственно, результатов прогноза. Это очень важно, поскольку включенные в обучающую выборку данные всегда обладают определенной неполнотой как в отношении охвата всех химических классов веществ, имеющих конкретный вид активности, так и в отношении изученности каждого отдельного вещества на все возможные виды активности.
Алгоритм оценки деятельности спектра на основе метода Bayesian [7] имеет ряд важных особенностей. Для каждого вида деятельности Аk, которые могут быть предсказаны PASSом исходя из структуры молекулы, представляют набор дескрипторов многоуровневых окрестностей атомов (МОА) {D1, D2,…, Dm}, они рассчитываются по следующим значениям:
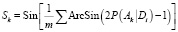
где Р (Аk) – предварительная вероятность соединения с деятельностью вида Аk; Р (Аk/Di) – условная вероятность деятельности рода Аk, если дескриптор D присутствует в наборе дескрипторов молекулы. Для каждого вида деятельности, если для всех дескрипторов молекулы Р (Аk/Di) = 1, то Вk = 1, если для всех дескрипторов молекулы Р (Аk/Di) = 0, то Вk = – 1, если отношения между дескрипторами молекулы и деятельности Аk не существует, и Р (Аk) ~ Р (Аk/Di), то Вk ~ 0.
Самое простое частота оценки вероятностей Р (Аk), Р (Аk/Di) имеет вид:
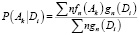
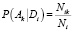
где N – общее число соединений базы SAR; Nk – число соединений, содержащихся в деятельности > Аk активности спектра; Ni – число соединений, содержащихся в дескрипторе Di описания структуры; Nik – число соединений, содержащийся как деятельность Аk и дескриптор Di.
В версии PASS 1,703, а затем и оценки вероятностей Р (Аk), Р (Аk/Di) рассчитывается как:
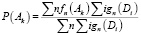 (1)
(1)
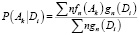 (2)
(2)
где ƒn (Ak) – общая функция соединения n, принадлежащий к набору соединений, содержащихся в деятельности Ak спектра действия, ƒn (Ak) равна 0 или 1; gn (Di) – мера соединения n, принадлежащий к множеству соединений, содержащихся в дескрипторе Di описания структуры, теперь gn (Di) равен 0, или, если mn количество дескрипторов для молекулы n, и в этом случае Σi gn (Di) ≡ 1.
Оценки (1) и (2) вероятностей Р (Ak), Р (Аk/Di) не только повышает точность прогнозирования алгоритм, но и открывает новые возможности.
Алгоритм прогнозирования:
Для соединения по предсказанию создаются структурные дескрипторы. Для каждого вида деятельности рассчитываются следующие значения:
uj = αiArcSin{ri(2pij – 1)},
u0j = αiArcSin{ri(2pj – 1)},
sj = Sin(uj/m), s0j = Sin(u0j/m),
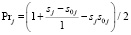 .
.
Рассматривается связь биологической активности вещества с его структурой с точки зрения вклада неизменной части молекул уже изученных веществ (в дальнейшем ядра) в наблюдаемую активность и вклада заместителей i с учетом их положения j. Кроме того, очевидно, не может быть два заместителя в одном и том же положении.
Проверка критерия:
Для каждого вида деятельности рассчитываются оценки Е1j (СРj) и Е2j (СРj). Рассчитывается отрезок точки СРj*, которая обеспечивает равенство:
E1j(CPj*) = E2j(CPj*)
Максимальная погрешность прогнозирования (МЕР) является:
MEPj = E1j(CPj*) = E2j(CPj*)
Результаты прогноза:
Вероятность того, чтобы быть активным является
Paj = E1j(Prj)
Вероятность быть неактивным является
Pij = E2j(Prj)
В результате прогноз представлен в виде перечня видов деятельности, соответствующих Ра и Рi, сортируется в порядке убывания разности (Ра – Рi) > 0.
Следует иметь в виду, что существует фундаментальное ограничение: любое наблюдение, оценка, расчет ограничивается только точностью.
Это программа имеет свои определенные достоинства и недостатки.
Достоинством такой модели является ее простота. Рассмотренные выше математические методы анализа «химическая структура – активность» направлены на поиски предсказания биологического действия вещества на основе его химического строения и подбора такого метода, который смог бы дать подход к пониманию механизма действия лекарства. Математический подход, используемый в PASS С&Т, выбран Д.А. Филимоновым в результате сравнительного анализа 300 различных методов [8]. Имеется опыт [6, 9] применения методов квантовой химии для изучения взаимосвязи между биологическим действием и химическим строением некоторых производных флавоноидов и изофлавонов.
Другим перспективным направлением является: выявление новых эффектов и механизмов действия для старых веществ; выбор наиболее перспективных соединений для высокопроизводительного скрининга из множества доступных образцов; определение анализов, которые являются более актуальными для конкретного соединения.
Недостатком метода при прогнозировании более активных веществ является некоторая неопределенность при выборе структуры новых веществ, если все его дескрипторы являются новыми, и поэтому они не входят в обучающую выборку.
Учитывая все достоинства и недостатки рассмотренного метода анализа системы «структура вещества – биологическая активность», проведена работа по использованию программы PASS [7], разработанной в НИИ биомедицинской химии РАМН. Для некоторых синтезированных изофлавоноидов (1-8) [2–5, 10–12] была установлена возможность наличия у них несколько видов фармакологического действия, не требующая дополнительных экспериментов. Следовательно, эти вещества (1-8) могут служить основой для разработки лекарственных препаратов комплексного действия.
С помощью этой программы мы предлагаем рассмотреть связь биологической активности вещества с его структурой с точки зрения вклада неизменной части молекул уже изученных веществ (в дальнейшем ядра) в наблюдаемую активность и вклада заместителей с учетом их положения. Это будет показана на примере конкретных анализов «структура – активность» в сочетании с методами включении факторов, учитывающих совместное наличие двух заместителей или метода варьирования исходными данными, позволяющими получить оценки вкладов ядра и составляющих (заместителей с учетом их положения). Такие модели связи активности веществ с их конкретными структурами оказались адекватными результатами эксперимента.
При оценке вкладов ядра и заместителей с учетом их положения в активность веществ для решения системы линейных алгебраических уравнений использована разработанный алгоритм и соответствующая программа.
При изучении связи активности изофлавоноидов с вкладами ядра и заместителей с учетом последних исследовали структуры вида:
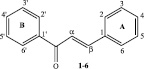
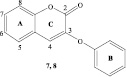
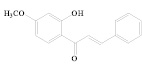
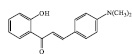
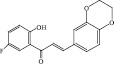
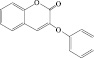
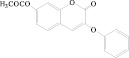
Для изучения взяты шесть структурных производных 2’-замещенных халконов и две структуры 3-феноксикумаринов, обладающие широким спектром биологического действия и низкой токсичностью. В качестве заместителей рассматриваются функциональные группы: 1-ОН, 2-ОСН3, 3-Cl, 4-N(CH3)2, 5-ОСН2С6Н5, 6-F (1-6) и 7-ОСОСН3 (8) (таблица).
В качестве показателей биологического действия соединений (1-8) рассматриваются нижеследующие активности (таблица), разработанные по программе PASS.
Для оценки вкладов ядра и составляющих в аддитивную модель к результатам эксперимента применен метод наименьших квадратов с учетом взаимного наличия заместителей -ОН и -ОСН2С6Н5 в положении 2’ кольца В соединений 1-6 и С=О в положении 2 кольца С – 8 (таблица). При сравнении значения Ра вычисленных активностей было обнаружено, что они незначительно отличаются между собой по типу заместителей с учетом их положения.
Анализируя рассчитанные данные вклада ядра и типов заместителей с учетом их положения в биологическую активность производных халконов (1-6) [1, 5, 6, 9] и феноксикумаринов (7, 8) [4, 5, 12] в таблице, необходимо отметить, что весомый вклад в активность вносит само ядро и функциональные группы -ОН, -ОСН3, и -ОСОС3, повышенная активность свыше 80 %. Здесь главными фармакологическими точками являются отрицательно заряженные атомы кислорода карбонила, несущего частичный положительный π-заряд, и атом кислорода, находящийся у С2’ (1-6) и С3 (7, 8), играющие важную роль в биологическом эффекте [9].
Немаловажное влияние на активность оказывают тип и положение заместителя. Электронодонорные заместители (-ОН и -ОСН3) С2’; С4’; С4 (1-6) оказывают положительный эффект, значительно повышая активность (до 77-83 %). Электроноакцепторные заместители (ОСОСН3, ОС6Н5) в положении С7, С3 (7, 8) также оказывают положительный эффект, тогда как в положении 7 заместитель ОСОСН3 увеличивает активность до 88 %. Приведенные данные полезны для прогнозирования новых структур с более высокой активностью.
Принимая во внимание величину вклада каждого заместителя в определенном положении изофлавоноидного ядра на биологическую активность, можно сделать некоторые предложения относительно взаимосвязи между строением и названными активностями в ряду изофлавоноидов. Легко заметить, что появление в положении С2’, изофлавоноидного ядра электронодонорных заместителей –ОН (1-5) или –ОСН2С6Н5 (6), и в положении С4’, С5’, С4, (1-3, 6) – заместителей –ОСН3, оказывающих положительный мезомерный эффект (+М эффект) на сопряженную с ним карбонильную группу гетерокольца, несколько снижает активность изофлавоноидов по показателям. С другой стороны, появление сложноэфирной группы (ОСОСН3) или феноксигуппы (ОС6Н5) в положении С7, С3 лишает свободную электронную пару фенольного атома кислорода возможности участвовать в передаче +М эффекта на карбонил, что приводит к увеличению активности по обоим показателям.
|
Соединения |
Activity Prediction Pa Pi for Activity: |
|
1 |
2 |
|
1
1-(2’-Гидрокси-4’-метокси-фенил)-3-фенил-пропенон |
0.772 0.006 Antihypoxic 0.714 0.087 Antiseborrheic 0.773 0.005 Beta-carotene 15,15’-monooxygenase inhibitor 0.790 0.004 Carminative 0.835 0.003 Choleretic 0.755 0.007 Cytoprotectant 0.923 0.005 Feruloyl esterase inhibitor 0.708 0.029 Fibrinolytic 0.792 0.010 Hypercholesterolemic 0.781 0.009 Leukotriene C antagonist 0.754 0.007 Leukotriene C4 antagonist 0.880 0.023 Membrane integrity agonist 0.935 0.005 Mucomembranous protector 0.717 0.062 Myocardial ischemia treatment 0.720 0.007 Sigma receptor agonist 0.754 0.054 Transcription factor inhibitor 0.730 0.012 Vascular (periferal) disease treatment |
|
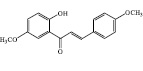
2
1-(2’-Гидрокси-5’-метокси-фенил)-3-(4-метокси-фенил)-пропенон |
0.761 0.008 Antihypoxic 0.789 0.004 Beta-carotene 15,15’-monooxygenase inhibitor 0.814 0.004 Carminative 0.823 0.003 Choleretic 0.752 0.008 Cytoprotectant 0.937 0.004 Feruloyl esterase inhibitor 0.788 0.011 Hypercholesterolemic 0.782 0.009 Leukotriene C antagonist 0.793 0.005 Leukotriene C4 antagonist 0.857 0.034 Membrane integrity agonist 0.930 0.005 Mucomembranous protector 0.720 0.059 Myocardial ischemia treatment 0.758 0.005 Sigma receptor agonist 0.748 0.059 Transcription factor inhibitor 0.705 0.018 Vascular (periferal) disease treatment |
|
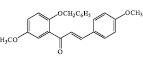
3
1-(2’-Бензилокси-5’-метокси-фенил)-3-(4-метокси-фенил)-пропенон |
0.702 0.008 Antiallergic 0.769 0.005 Antiasthmatic 0.721 0.018 Antihypoxic 0.762 0.005 Carminative 0.783 0.005 Cytoprotectant 0.885 0.010 Feruloyl esterase inhibitor 0.735 0.031 Hypercholesterolemic 0.829 0.006 Leukotriene C antagonist 0.832 0.004 Leukotriene C4 antagonist 0.764 0.078 Membrane integrity agonist 0.872 0.017 Mucomembranous protector 0.727 0.054 Myocardial ischemia treatment 0.756 0.020 Pulmonary hypertension treatment 0.703 0.019 Vascular (periferal) disease treatment |
|
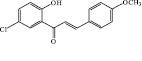
4
1-(2’-Гидрокси-5’-хлор-фенил)-3(4-метокси-фенил)-пропенон |
0.714 0.051 Amyotrophic lateral sclerosis treatment 0.711 0.021 Antihypoxic 0.728 0.004 Choleretic 0.843 0.020 Feruloyl esterase inhibitor 0.777 0.014 Hypercholesterolemic 0.857 0.034 Membrane integrity agonist 0.890 0.013 Mucomembranous protector 0.706 0.072 Myocardial ischemia treatment 0.740 0.006 Sigma receptor agonist |
|
Продолжение таблицы |
|
|
1 |
2 |
|
5
1-(2’-Гидрокси-фенил)-3-(4’-диметиламино-фенил)-Пропенон |
0.778 0.005 Antihypoxic 0.803 0.018 CC chemokine 2 receptor antagonist 0.799 0.030 Feruloyl esterase inhibitor 0.792 0.065 Membrane integrity agonist 0.911 0.008 Mucomembranous protector 0.809 0.027 Taurine dehydrogenase inhibitor 0.774 0.043 Transcription factor inhibitor |
|
6
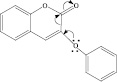
3-(2,3’-Дигидробензо [1,4]диоксин-6-ил)-1-(5’-фтор-2’-гидрокси-фенил)-пропенон |
0.917 0.004 CYP1A substrate 0.920 0.009 Membrane integrity agonist 0.903 0.004 CYP1A1 substrate 0.809 0.003 Cytochrome P450 inhibitor 0.791 0.005 CYP1A2 substrate 0.787 0.014 Aldehyde oxidase inhibitor 0.771 0.016 Membrane integrity antagonist 0.755 0.009 Vascular (periferal) disease treatment 0.746 0.017 Apoptosis agonist 0.722 0.006 Free radical scavenger 0.772 0.016 Mucomembranous protector 0.712 0.005 Cell adhesion inhibitor 0.701 0.027 Oxidoreductase inhibitor 0.727 0.071 Transcription factor inhibitor |
|
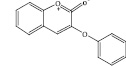
7
3-Фенокси-2Н-хромен-2-он |
0.917 0.010 Membrane integrity agonist 0.902 0.003 CYP2B5 substrate 0.880 0.003 CYP2A11 substrate 0.889 0.023 Methylenetetrahydrofolate reductase (NADPH) inhibitor 0.858 0.008 Cathepsin G inhibitor 0.850 0.003 Aryl-alcohol dehydrogenase (NADP+) inhibitor 0.838 0.005 Protoporphyrinogen oxidase inhibitor 0.832 0.010 Pulmonary hypertension treatment 0.825 0.005 Cholestanetriol 26-monooxygenase inhibitor 0.820 0.007 Nitrate reductase (cytochrome) inhibitor 0.806 0.003 Scytalone dehydratase inhibitor 0.815 0.014 Lipid metabolism regulator 0.802 0.004 P-benzoquinone reductase (NADPH) inhibitor 0.798 0.004 CYP2A3 substrate 0.803 0.011 Aldehyde oxidase inhibitor 0.805 0.042 Mucomembranous protector 0.778 0.024 Glucan endo-1,6-beta-glucosidase inhibitor 0.766 0.013 Oxidoreductase inhibitor 0.797 0.051 Hematotoxic 0.748 0.006 CYP2A2 substrate 0.763 0.023 Monodehydroascorbate reductase (NADH) inhibitor 0.741 0.004 CYP2A1 substrate 0.767 0.033 Cardioprotectant 0.772 0.039 Arylacetonitrilase inhibitor 0.748 0.015 Neurotoxin 0.740 0.009 Kinase inhibitor 0.731 0.004 CYP2F1 substrate 0.733 0.013 Neurotransmitter antagonist 0.734 0.019 Apoptosis antagonist 0.714 0.007 2,3-Dihydroxyindole 2,3-dioxygenase inhibitor 0.720 0.014 Vascular (periferal) disease treatment 0.714 0.010 Neurotrophic factor enhancer 0.737 0.035 Glutathione thiolesterase inhibitor 0.709 0.009 Spasmolytic, urinary 0.707 0.010 Nerve growth factor agonist 0.729 0.036 Manganese peroxidase inhibitor 0.712 0.031 2-Hydroxymuconate-semialdehyde hydrolase inhibitor 0.713 0.036 Cholesterol synthesis inhibitor 0.705 0.032 Antineurotoxic 0.707 0.037 Alkane 1-monooxygenase inhibitor 0.727 0.083 Antiseborrheic 0.704 0.074 Myocardial ischemia treatment |
|
Окончание таблицы |
|
|
1 |
2 |
|
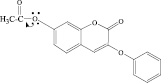
8
7-Ацетокси-3-фенокси-2Н-хромен-2-он |
0.894 0.003 CYP2B5 substrate 0.889 0.007 Lipid metabolism regulator 0.892 0.018 Membrane integrity agonist 0.883 0.013 Antiseborrheic 0.818 0.013 Myocardial ischemia treatment 0.797 0.004 CYP2A11 substrate 0.821 0.034 Mucomembranous protector 0.795 0.009 Oxidoreductase inhibitor 0.769 0.017 Hypercholesterolemic 0.748 0.015 Fibrinolytic 0.741 0.010 Vascular (periferal) disease treatment 0.730 0.007 CYP2A2 substrate 0.756 0.036 Cardioprotectant 0.740 0.023 Protoporphyrinogen oxidase inhibitor 0.721 0.009 Kinase inhibitor 0.729 0.024 Pulmonary hypertension treatment 0.756 0.054 Transcription factor inhibitor 0.709 0.017 Neurotransmitter antagonist |
Библиографическая ссылка
Исмаилова Г.О., Юлдашев Н.М., Эшкулов Д.И., Каримова Ш.Ф. КОРРЕЛЯЦИОННЫЙ АНАЛИЗ «СТРУКТУРА ХИМИЧЕСКОГО ВЕЩЕСТВА – БИОЛОГИЧЕСКАЯ АКТИВНОСТЬ» В РЯДУ СИНТЕЗИРОВАННЫХ ПРОИЗВОДНЫХ ХАЛКОНОВ И 3-ФЕНОКСИКУМАРИНОВ // Успехи современного естествознания. 2015. № 9-3. С. 496-502;URL: https://natural-sciences.ru/ru/article/view?id=35621 (дата обращения: 30.03.2026).