Оксидные фазы алюминия находят широкое применение в катализе, технологиях очистки воды, при модифицировании полимерных материалов [1, 6], в медицинской отрасли [4]. Синтез оксидов алюминия осуществляется различными способами: осаждением из солей, золь-гель методом, гидролизом алкоголятов алюминия, гидротермальным окислением алюмогелей, лазерной абляцией, механохимическими методами, а также окислением металлического алюминия и др. Данными методами получают разнообразные по морфологии и фазовому составу оксиды алюминия: наноусы, наноцветки, нанопроволоку, нановолокна, наностержни, нанотрубки, нанолисты, нанопластинки и т.д. [1].
Перспективными структурами являются полые сферы на основе оксигидроксидов алюминия. Гидротермальный метод их получения из различных прекурсоров при температуре 160 °С, а также эволюция морфологии в зависимости от времени обработки (2 и 24 часа), описаны в работе [3]. В работах [8, 2] также рассматривается гидротермальный синтез полых сфер при температурах 160 °С и выше, проводившийся в течение 3–24 часов.
Метод окисления нанопорошка алюминия водой, является одним из перспективных способов получения микро- и наноструктур оксидов алюминия [5]. Одним из преимуществ данного метода является то, что он не требователен к точному контролю параметров реакции. Так, окисление начинается при нагревании водной суспензии до 40–60 °С. В результате реакции происходит полное окисление алюминия с образованием нанолистов псевдобемита [9].
В большинстве случаев окисление водой наночастиц алюминия рассматривается как перспективный метод получения водорода, и гораздо меньше внимания уделяется продуктам окисления [7]. В связи с этим целью работы является изучение особенностей окисления водой наночастиц Al и Al/AN.
Материалы и методы исследования
В качестве исходных продуктов для синтеза наноструктур на основе оксигидроксидов алюминия использовали нанопорошки Al и Al/AlN. Нанопорошки были получены электрическим взрывом алюминиевого проводника в атмосфере аргона и в атмосфере азота, при давлении газовых сред 5·105 Па и пассивированные медленным напуском воздуха.
Окисление водой нанопорошков проводили в термоизолированном сосуде. Для этого навеску порошка массой 1,0 г помещали в 100 мл дистиллированной воды и нагревали до 60 °С. Для исследований промежуточных продуктов окисления методом ПЭМ, из реакционной среды на различных стадиях процесса отбирали пробы объемом 5 мкл.
Просвечивающая электронная микроскопия (ПЭМ) проводилась на электронном микроскопе JEOL JEM-2100. Продукты окисления нанопорошков также исследовали с помощью интегрированного в микроскоп энергодисперсионного рентгеновского спектрометра X-Max в режиме картирования. Исследование фазового состава продуктов окисления проводилось на рентгеновском дифрактометре Shimadzu XRD 6000 на Cu Kα излучении. Удельную поверхность и распределение пор по размерам определяли по изотерме сорбции азота на анализаторе удельной поверхности Sorbtometer-M в статических условиях.
Результаты исследования и их обсуждения
Исходные частицы Al имеют сферическую форму и средний размер 98 нм (рис. 1, а). При электрическом взрыве проводника в атмосфере азота, образуется композит Al/AlN с соотношением 30/70 % масс. Данные частицы имеют преимущественно ярко выраженную огранку и средний размер 86 нм (рис. 1, в). Пассивация порошка на воздухе приводит к образованию на поверхности частиц оксидной пленки. Согласно данным ПЭМ, толщина оксидной пленки Al составляет 4 нм (рис. 1, б), толщина оксидной пленки Al/AlN составляет около 1 нм (рис. 1, г). По данным точечного элементного анализа, ограненные частицы являются нитридом алюминия, в сферических частицах присутствует преимущественно алюминий.
Было установлено, что полное окисление водой нанопорошков в данных условиях происходит за 40 минут. Окисление водой сопровождается экстремальным изменением рН (рис. 2, кривые 1) и температуры реакционной среды (рис. 2, кривые 2). Характер кривых изменения рН и температуры позволяет выделить следующие стадии окисления нанопорошков: I – индукционный период, в котором не происходит изменения рН; II – монотонный рост рН реакционной среды; III – саморазогрев реакционной среды, сопровождающийся кратковременным снижением рН; IV – достижение максимального уровня рН.




Рис. 1. Изображения наночастиц Al (а, б) и Al/AlN (в, г), полученные методом ПЭМ
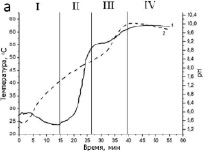
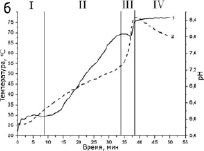
Рис. 2. Кинетические кривые 1 – рН, 2 – температуры при окислении нанопорошка Al/AlN (а), и Al (б)








Рис. 3. ПЭМ-изображения промежуточных продуктов реакции Al (а-г) и Al/AlN (д-з) с водой через 25 мин (а, д), 35 мин (б, е), 38 мин (в, ж), 40 мин (г, з)
Для понимания механизма реакции исследовали промежуточные продукты реакции нанопорошков с водой. Для этого отбирали пробы суспензии из реактора на разных стадиях процесса и изучали их с помощью ПЭМ. На рис. 3 представлены характерные изображения продуктов окисления наночастиц Al и Al/AlN водой на различных стадиях: на 25 минуте – на второй стадии процесса (рис. 3, а, д), в интервале между 35 и 38 минутами процесса – начало и окончание стадии с наибольшей скоростью окисления (рис. 3, б, е, в, ж, соответственно), через 40 минут – замедление реакции, прекращение газовыделения, достижение максимального значения рН (рис. 3, г, з).
Во время индукционного периода (стадия I) не наблюдается изменений рН, реагирующие наночастицы не отличаются от исходных наночастиц. На стадии II происходит формирование островков аморфного оксида алюминия на поверхности наночастиц (рис. 3, а, д). По данным ПЭМ, размер островков составляет 5–30 нм. В начале III стадии окисления, на поверхности частиц образуются тонкие пластинчатые структуры бемита (рис. 3, б, е). В ходе III стадии достигается максимальная скорость и температура реакции, в центре алюминиевой частицы наблюдается частично прореагировавшее алюминиевое ядро (рис. 3, в). Образование полостей при реакции наночастиц Al/AlN с водой не наблюдается (рис. 3, ж). На ПЭМ-изображениях видно, что размер нанолистов бемита на поверхности реагирующих частиц увеличивается и достигает 100–250 нм.
В результате полного окисления водой наночастиц алюминия образуются полые сферы размером 400–800 нм. Оболочку полых сфер составляют нанолисты с планарным размером 100–300 нм и толщиной 2–8 нм. Размер полостей внутри сфер приблизительно равен 80–150 нм, то есть размеру наночастиц алюминия, которые использовались в качестве прекурсора (рис. 3, г). При окислении водой наночастиц Al/AlN полых сфер не образуется. Морфология частиц представляет собой агломераты нанолистов размером до 1 мкм. Планарный размер отдельных нанолистов достигает 300 нм при толщине 2–8 нм.

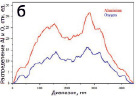
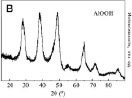

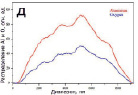
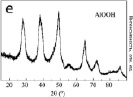
Рис. 4. ПЭМ-изображения (а, г), ЭДС анализ (б, д) и РФА (в, е) продукта окисления Al и Al/AlN, соответственно
На рис. 4 представлены результаты ПЭМ-ЭДС и РФА синтезированных образцов. Как видно из рис. 4, б, в центре реагирующей частицы интенсивность спектра Al и O по центру частицы снижается. Это подтверждает наличие полости в центре частицы.
В случае окисления Al/AlN, частица не имеет полости в своем объеме. Образовавшаяся структура является сплошным агломератом нанолистов (рис. 4, г–е).
По данным РФА при окислении нанопорошков образуется псевдобемит (рис. 4, в, е). Удельная поверхность продуктов окисления Al составила 284,7 м2/г, Al/AlN – 296,3 м2/г. Образцы имеют щелевидные поры шириной от 4 до 20 нм.
Таким образом, показано, что при практически одинаковых условиях окисления из наночастиц алюминия образуются полые сферы, покрытые оболочкой из нанолистов псевдобемита. При окислении водой Al/AlN полых сфер не образуется. Решающую роль при формировании полой сферы играет оксидная пленка, которая с одной стороны является границей полости, образованной за счет растворения алюминиевого ядра. С другой стороны оксидная пленка выступает темплатом для формирования нанолистовой оболочки.
Заключение
Показано, что окисление водой наночастиц Al и Al/AlN можно разделить на 4 стадии по изменению рН реакционной среды. С помощью анализа промежуточных продуктов, реакции Al и Al/AlN с водой методом просвечивающей электронной микроскопии показан процесс эволюции образующихся наноструктур псевдобемита. Методом ПЭМ и ПЭМ-ЭДС показано, что при окислении наночастиц Al водой образуются полые сферы с оболочкой из нанолистов псевдобемита. Также установлено, что продуктами окисления наночастиц Al/AlN в аналогичных условиях являются агломераты AlOOH без полостей. Образование полых сфер при окислении алюминиевых наночастиц обусловлено наличием более толстой оксидной пленки.
Работа выполнена при финансовой поддержке Российского научного фонда (грант № 14-23-00096).
Библиографическая ссылка
Горбиков И.А., Казанцев С.О. ЭВОЛЮЦИЯ НАНОЛИСТОВЫХ СТРУКТУР ПСЕВДОБЕМИТА ПРИ ОКИСЛЕНИИ ВОДОЙ НАНОЧАСТИЦ Al И Al/AlN // Успехи современного естествознания. 2015. № 10. С. 15-18;URL: https://natural-sciences.ru/ru/article/view?id=35642 (дата обращения: 21.05.2026).



