Развитие техники и технологий требует постоянного поиска новых функциональных материалов. Вместе с этим появляются новые методы синтеза материалов с различной морфологией. Известно, что макроскопические свойства материалов зависят не только от их химического состава, но и от размера, формы и структуры полученных материалов [2].
Наноразмерные гидроксиды и оксиды алюминия находят широкое применение в качестве адсорбентов и катализаторов для химических процессов [5] в технологиях очистки воды [9]. В последнее время они находят применение в медицинских приложениях [3]. Одними из основных методов синтеза оксидов и гидроксидов алюминия являются методы осаждения из растворов солей, анодное окисление, гидротермальное окисление, золь-гель технологии с использованием как неорганических, так и органических реагентов, окисление нанопорошка алюминия. В зависимости от способа получения возможно синтезировать оксиды и гидроксиды алюминия различной морфологии и фазового состава: наностержни, нанотрубки, наноусы, нанопроволоки, нанопластинки, нановолокна, наноцветки и др. [1, 2, 4, 6, 8, 10].
Перспективным методом синтеза оксидов и гидроксидов алюминия является окисление нанопорошка алюминия водой [7]. Данный метод не требователен к точному контролю параметров процесса, побочным продуктом реакции является водород. В результате реакции происходит полное окисление исходных наночастиц, с образованием нанолистов псевдобемита. Однако рассмотрение механизма образования продуктов реакции и изучение промежуточных продуктов реакции ранее не исследовалось.
На основании этого целью работы является изучение процесса окисления водой наночастиц Al в различных условиях. Исследовать промежуточные продукты окисления и предположить возможные механизмы окисления наночастиц алюминия.
Материалы и методы исследования
В работе использовали нанопорошок алюминия, полученный электрическим взрывом алюминиевой проволоки в атмосфере аргона и пассивированный кислородом воздуха.
Окисление нанопорошка алюминия водой проводили в термоизолированном сосуде. Навеску порошка массой 1,0 г помещали в 100 мл дистиллированной воды и при постоянном перемешивании нагревали до 55–60 °С. Полное окисление порошка происходило в течение часа. После чего отфильтровывали продукты реакции и сушили при 120 °С в течение 2 часов. В процессе окисления отбирали пробы промежуточных продуктов окисления и исследовали их с помощью ПЭМ.
Гидротермальное окисление (ГТО) проводили в автоклаве с тефлоновым вкладышем. Для этого навеску порошка Al массой 1,0 г помещали в автоклав, герметизировали и проводили окисление при 200 °С в течение 6 часов. После чего остужали автоклав, фильтровали продукты реакции и сушили при 120 °С в течение 2 часов. Для ПЭМ-исследований промежуточных продуктов проводили серию параллельных опытов с изменением времени протекания процессов окисления в гидротермальных условиях.
Окисление нанопорошка алюминия во влажном воздухе проводили в климатической камере ТХВ-60 при относительной влажности воздуха 80 % и температуре 60 °С. Навески порошка массой по 1,0 г помещали в открытых стеклянных стаканчиках в камеру и проводили окисление в течение 24 часов. Для исследования промежуточных продуктов через определенные промежутки времени образцы извлекались из камеры.
Формо-размерные характеристики полученных образцов исследовали методом просвечивающей электронной микроскопии (ПЭМ) с помощью JEM 2100 (JEOL, Япония). Удельную поверхность и характер пористой структуры определяли по тепловой десорбции азота с помощью анализатора удельной поверхности Сорбтометр М (Катакон, Россия). Фазовый состав продуктов окисления изучали методом рентгенофазового анализа при помощи рентгеновского дифрактометра XRD-6000 на CuKα – излучении, λ = 1,54056 Å (Shimadzu, Japan).
Результаты исследования и их обсуждение
Наночастицы алюминия, используемые в работе, имеют сферическую форму со средним размером частиц 78 нм (рис. 1, а). Поверхность наночастиц алюминия покрыта оксидной пленкой, толщина которой составляет 4–5 нм (рис. 1, б).
Полное окисление водой наночастиц алюминия происходит за 60 минут (отсутствие признаков реакции: изменение рН, выделение водорода). Во влажном воздухе наночастицы полностью окисляются за 24 часа (не происходит увеличение массы продуктов реакции) Полное ГТО наночастиц Al происходит в течение 6 часов (оценивали по изменению морфологии продуктов окисления). В связи с этим для исследования промежуточных продуктов с помощью ПЭМ, отбирали пробы для исследования: через 15, 30, 40, 60 минут при окислении водой; через 0,5, 1, 3 и 6 часов и температуре 200 °С при ГТО; через 3, 6, 12 и 24 часа при окислении наночастиц алюминия влажным воздухом.
На рис. 2 представлены ПЭМ изображения промежуточных продуктов окисления нанопорошка алюминия в различных условиях. При окислении нанопорошка алюминия в воде и влажном воздухе на начальной стадии образуются идентичные продукты окисления (рис. 2, а, д). Вероятнее всего, на данном этапе происходит гидратация поверхностной оксидной пленки, диффузия реагента через оксидную пленку и формирование на поверхности аморфного оксида алюминия.
При дальнейшем окислении в воде на поверхности оксидной пленки происходит формирование нанолистов оксигидроксида алюминия размером до 50 нм и толщиной от 5 до 8 нм (рис. 2, б). По мере дальнейшего окисления происходит растворение алюминиевого ядра с образованием полости, ограниченной оксидной пленкой (рис. 2, в). При этом происходит диффузия продуктов реакции на поверхность оксидной пленки и увеличение размеров нанолистов до 100–250 нм. По окончании реакции происходит образование полых сфер, покрытых пористой оболочкой, состоящей из смятых нанолистов с планарным размером до 300 нм и толщиной 5–8 нм (рис. 2, г). Диаметр образовавшихся полостей соответствует диаметру прореагировавших частиц алюминия.


а б
Рис. 1. ПЭМ-изображения нанопорошка (а) и частицы, покрытой оксидной пленкой (б)

Рис. 2. Промежуточные продуты окисления в воде через: а –15 мин; б – 30 мин; в – 40 мин; г – 60 мин; во влажном воздухе через: д – 3 ч; е – 6 ч; ж – 12 ч; з – 24 ч; в ГТО: и – 0,5 ч; к – 1 ч; л – 3 ч; м – 6 ч
При окислении алюминиевых наночастиц во влажном воздухе происходит формирование плотных конусовидных структур размером 100–500 нм (рис. 2, е–з), которые увеличиваются в процессе окисления, а исходные частицы уменьшаются до полного исчезновения.
Различия в процессах окисления наночастиц алюминия водой и влажным воздухом можно объяснить тем, что при окислении водой, в избытке реагента, происходит растворение алюминия с образованием аквагидрокомплексов. Избыток воды насыщает координационное число алюминия в составе аквагидрокомплексов, что приводит к образованию димеров, объединенных в цепи, которые и формируют нанолисты.
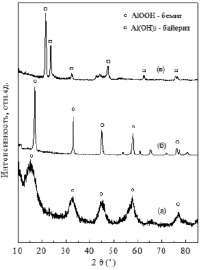
Рис 3. РФА образцов, полученных окислением в воде (а), старением в ГТО (б) и окислением влажным воздухом (в)
Во влажном воздухе скорость реакции значительно меньше, что объясняется низкой скоростью подвода реагента и его недостатком. Рост конусовидных частиц происходит на определенных поверхностных центрах, вероятно, образованных за счет дефектов оксидной пленки.
При гидротермальном окислении наночастиц алюминия (рис. 2, и–л) через 30 минут реакции синтезированные наноструктуры идентичны полым сферам, образовавшимся в воде при 60 °С через 60 минут. При дальнейшей гидротермальной обработке происходит разрушение оболочки полой сферы с образованием нанопластинок размером 40–100 нм и толщиной 4–15 нм (рис. 2, м). Решающим фактором в образовании продуктов ГТО, вероятнее всего, является давление паров воды.
По данным рентгенофазового анализа, продукт окисления наночастиц в воде (рис. 3, а) характеризуется дифракционными максимумами, соответствующими кристаллической фазе бемита, однако линии уширены, что связано с малым размером областей когерентного рассеивания; наличием микронапряжений, возникающих в кристаллической решётке, и наличием межслоевой воды. Такие особенности характерны для фазы псевдобемита. При ГТО наночастиц алюминия, образуются хорошо окристаллизованные частицы бемита (рис. 3, б). Во влажном воздухе происходит образование байерита (рис. 3, в).
Таким образом, показано, что при окислении наночастиц алюминия в зависимости от условий синтеза можно синтезировать наноструктурные частицы с различной морфологией и структурно-фазовыми характеристиками. Значительные отличия при формировании наноструктур из наночастиц алюминия наблюдаются при окислении в воде и во влажном воздухе.
В таблице представлены некоторые физико-химические характеристики синтезированных наноструктур.
Заключение
В работе исследована эволюция наноструктурных частиц при окислении алюминиевых наночастиц в различных условиях. Показано, что окисление наночастиц в воде приводит к образованию полых сфер, ограниченных оксидной пленкой и покрытых нанолистами псевдобемита. При окислении наночастиц алюминия влажным воздухом происходит формирование конусовидных частиц байерита. Рост конусовидных частиц осуществляется на зародышах, расположенных на оксидной пленке, путем уменьшения первоначальных частиц до их полного исчезновения. При ГТО наночастиц алюминия вначале образуются полые сферы, покрытые оболочкой из нанолистов, далее происходит разрушение полых сфер с образованием нанопластинок бемита. Главным фактором, приводящим к образованию нанопластин, является давление паров воды.
Характеристики полученных образцов
|
Образец |
Удельная поверхность, м2/г |
Дзета-потенциал, мВ |
Брутто-формула |
|
Агломераты нанолистов |
285 |
+ 30,3 |
Al2O3×1,9H2O |
|
Нанопластинки |
198 |
+ 33,1 |
Al2O3×1,5 H2O |
|
Конусовидные частицы |
12 |
+ 33,0 |
Al2O3×3H2O |
Все процессы окисления нанопорошка алюминия, рассмотренные в настоящей работе, могут быть использованы для получения наноструктур на основе оксигидроксидов алюминия с заданными характеристиками.
Работа выполнена при финансовой поддержке Российского научного фонда (грант № 14-23-00096).
Библиографическая ссылка
Казанцев С.О., Горбиков И.А. ОСОБЕННОСТИ ОКИСЛЕНИЯ ВОДОЙ НАНОЧАСТИЦ АЛЮМИНИЯ В РАЗЛИЧНЫХ УСЛОВИЯХ // Успехи современного естествознания. 2015. № 10. С. 27-31;URL: https://natural-sciences.ru/ru/article/view?id=35644 (дата обращения: 28.05.2026).



