В последние десятилетия для разделения и очистки различных веществ, в том числе и биологической природы, широко используются водные двухфазные системы на основе водорастворимых полимеров, в частности полиэтиленгликолей различных молекулярных масс и водных растворов неорганических и органических солей [1, 4, 8]. Применение для разделения и очистки веществ на промышленном уровне водных двухфазных систем вода – полимер – неорганические соли, такие как фосфаты, сульфаты и т.д., является нежелательным ибо приводит к загрязнению окружающей среды. Используя так называемые биоразлагаемые соли природных органических кислот, такие как цитраты, тартраты, сукцинаты и т.д., можно избежать этого [15]. Следует отметить, что в последнее время исследованию водных двухфазных систем полиэтиленгликоль – натриевые соли органических кислот и применению их для разделения и очистки биологических объектов посвящается достаточно много работ [5, 10, 12, 16–18, 20]. Однако механизм разделения таких систем на две водные фазы недостаточно изучен. А между тем исследования физико-химических свойств сопряженных фаз водных двухфазных систем, так и водных растворов отдельных компонентов с применением различных методов физико-химического анализа могут оказаться весьма полезными в решении указанной проблемы.
Материалы и методы исследования
Методами рефрактометрии и волюмометрии изучены водные растворы полиэтиленгликоля (ПЭГ-6000) и лимоннокислого натрия (C6H5O7Na3 – в дальнейшем цитрат натрия). В сравнительно широком интервале концентраций изучены показатель преломления (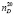 ) и плотность (ρ20) водных растворов ПЭГ-6000 и цитрата натрия. Были использованы полиэтиленгликоли фирмы «Panreac» (Испания), цитрат натрия марки ЧДА, перекристаллизованный из водных растворов, бидистиллированная вода. Показатель преломления определили на рефрактометре марки ИРФ-454Б с точностью ± 0,0001, плотность в пикнометрах около 10 мл, объемы которых предварительно были определены с точностью ± 0,005 мл при 20 ± 0,02 °С.
) и плотность (ρ20) водных растворов ПЭГ-6000 и цитрата натрия. Были использованы полиэтиленгликоли фирмы «Panreac» (Испания), цитрат натрия марки ЧДА, перекристаллизованный из водных растворов, бидистиллированная вода. Показатель преломления определили на рефрактометре марки ИРФ-454Б с точностью ± 0,0001, плотность в пикнометрах около 10 мл, объемы которых предварительно были определены с точностью ± 0,005 мл при 20 ± 0,02 °С.
Были построены фазовые диаграммы двухфазной системы ПЭГ-6000 – цитрат натрия – вода при различных температурах (283,15; 298,15; 313,15 и 333,15 К). Бинодали были построены методами титрования и определения составов сопряженных фаз. Изучено влияние молекулярной массы ПЭГ в системах ПЭГ – цитрат натрия – вода при 298,15 К, а также различных добавок (карбамид, тиокарбамид и этиловый спирт) на фазовую диаграмму водной двухфазной системы ПЭГ-6000 – цитрат натрия. Этиловой спирт был очищен по известной методике, приведенной в работе [2].
Результаты исследования и их обсуждение
В широком интервале концентрацией (Wp = 0÷35 %) определены плотность (ρ20) и показатель преломления (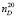 ) водных растворов ПЭГ-6000 при 293,15 К, зависимости которых от концентраций даются следующими соотношениями:
) водных растворов ПЭГ-6000 при 293,15 К, зависимости которых от концентраций даются следующими соотношениями:
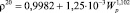 ; (1)
; (1)
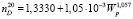 , (2)
, (2)
где Wp – весовой процент ПЭГ в водном растворе.
Эти результаты хорошо согласуются с данными, полученными из единых уравнений для полиэтиленгликолей различной молекулярной массы, предложенной в работе [6]. Некоторые расхождения данных в области высоких концентраций полиэтиленгликоля должны быть связаны с трудностями достижения равновесия в таких вязких системах.
Для водных растворов цитрата натрия получены следующие соотношения зависимости плотности и показателя преломления от концентрации соли в растворе:
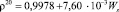 (R2 = 0,9998); (3)
(R2 = 0,9998); (3)
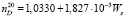 (R2 = 0,9898), (4)
(R2 = 0,9898), (4)
где Ws – весовой процент цитрата натрия в растворе.
Были вычислены мольные объемы водных растворов (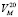 ) указанных компонентов, которые практически являются линейными функциями состава, выраженного в мольных долях. Так, например, для водных растворов ПЭГ-6000 зависимость мольного объема (
) указанных компонентов, которые практически являются линейными функциями состава, выраженного в мольных долях. Так, например, для водных растворов ПЭГ-6000 зависимость мольного объема (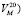 от состава, выраженного в мольных долях (Xp), дается следующим уравнением:
от состава, выраженного в мольных долях (Xp), дается следующим уравнением:
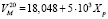 (5)
(5)
Это позволяет принять парциальный мольный объем воды (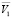 ) в этих растворах равным мольному объему чистой воды (
) в этих растворах равным мольному объему чистой воды (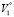 ) и рассчитать через кажущиеся мольные объемы парциальные мольные объемы ПЭГ-6000 (
) и рассчитать через кажущиеся мольные объемы парциальные мольные объемы ПЭГ-6000 (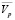 ) и соли (
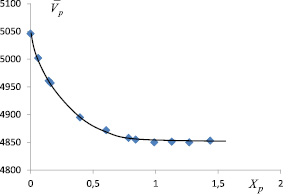
) и соли (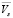 ) в водном растворе [6, 9]. На рис. 1 представлены зависимости парциальных мольных объемов ПЭГ-6000 (а) и цитрата натрия (б) в водных растворах.
) в водном растворе [6, 9]. На рис. 1 представлены зависимости парциальных мольных объемов ПЭГ-6000 (а) и цитрата натрия (б) в водных растворах.
Получены уравнения зависимости парциального мольного объема ПЭГ-6000 (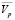 ) и цитрата натрия (
) и цитрата натрия (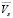 ) от концентрации их в водном растворе (мл/моль):
) от концентрации их в водном растворе (мл/моль):
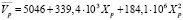 , (R2 = 0,9866), (6)
, (R2 = 0,9866), (6)
где Xp – мольная доля ПЭГ в растворе;
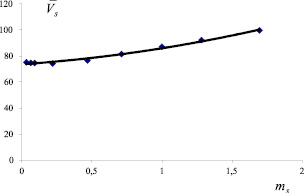
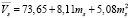 , (7)
, (7)
где ms – моляльность соли в водном растворе.
Следует отметить, что уменьшение и некоторое постоянство значения парциального мольного объема ПЭГ-6000 с увеличением содержания его в растворе, возможно, связано с образованием в растворах относительно стабильной пространственной структуры, где молекулы полимера соединены между собой свободными молекулами воды за счет водородных связей. Образование такой пространственной структуры, сохраняющей в определенной мере кооперативность связей, по всей вероятности, служит причиной некоторого постоянства парциального мольного объема ПЭГ-6000 при повышенных концентрациях его в водном растворе. Увеличение парциального мольного объема цитрата натрия с возрастанием концентрации его в растворе, возможно, связано с наличием поворотной изомерии у цитрат иона с одной стороны и образованием водородных связей между цитрат ионами с увеличением содержания соли в растворе.
На рис. 2 представлены бинодали водных двухфазных систем, образованных ПЭГ различной молекулярной массы и цитратом натрия. Как видно из рисунка, увеличение молекулярной массы ПЭГ смещает бинодальные кривые влево, приводя к увеличению области гетерогенности. Этот экспериментальный факт можно объяснить следующим образом. Хотя при постоянной весовой концентрации полиэтиленгликоля число мономерных звеньев (-CH2CH2O-) на единицу массы водного раствора будет одинаково независимо от молекулярной массы полимера, однако число молекул будет тем больше, чем меньше молекулярная масса ПЭГ. Вследствие того что клубкообразные молекулы ПЭГ с меньшей молекулярной массой имеют большую вероятность к более полному раскрытию и гидратации, то все это делает молекулы полимера со своим водным окружением более совместными с водно-солевым раствором. Эта совместимость должна уменьшаться по мере увеличения молекулярной массы ПЭГ, и расслоение наступит при меньшем содержании полимера в растворе.
Изучено также влияние температуры на фазовую диаграмму водной двухфазной системы ПЭГ-6000 – цитрат натрия. На рис. 3 представлены бинодали указанной системы при различных температурах. Как видно, увеличение температуры также смещает бинодальные кривые влево, увеличивая области гетерогенности системы. Влияние температуры, как и любого другого фактора, влияющего на положение равновесия, должно быть в соответствии с принципом смещения равновесия Ле Шателье – Брауна [7].
a)
б)
Рис. 1. Зависимость парциального мольного объема ПЭГ-6000 (а) и цитрата натрия (б) от концентрации раствора
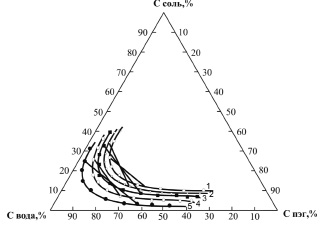
Рис. 2. Бинодальные кривые водных двухфазных систем ПЭГ – С6Н5О7Na3 с различными молекулярными массами полимера (T = 298,15K). 1 – 300, 2 – 600, 3 – 2000, 4 – 6000, 5 – 20000

Рис. 3. Бинодали двухфазной системы ПЭГ – цитрат натрия – вода при различных температурах: 1 – 333,15 К; 2 – 313,15 К; 3 – 298,15 К; 4 – 283,15 К
В работе [3] указано, что в водных растворах полиэтиленгликолей образуются двухфазные системы с двумя критическими температурами растворения – верхней (ВКТР) и нижней (НКТР). Следовательно, тот факт, что увеличение температуры смещает бинодали указанной системы в направлении увеличения области гетерогенности системы, указывает на близость рассматриваемого интервала температур к нижней критической температуре растворения. Кроме того, повышение температуры способствует процессу дегидратации как ионов соли, так и полиэтиленгликоля, изменяя водное окружение молекул последнего, что в итоге также приводит к уменьшению совместимости молекул ПЭГ и ионов соли, способствующее более раннему расслоению системы на две водные фазы с отличающимися структурами.
Нами также изучено влияние карбамида, тиокарбамида и этилового спирта на фазовую диаграмму водной двухфазной системы ПЭГ-6000 – цитрат натрия. Добавление карбамида заметно изменяет положение бинодали указанной системы, увеличивая при этом область гомогенности системы, т.е. фазовое расслоение имеет место при больших концентрациях фазообразующих компонентов, чем в отсутствии мочевины. Ввиду того, что добавление карбамида к воде и водным растворам сопровождается разрушением структуры воды [13, 14, 20], должно быть ясно, что увеличение доли свободных молекул воды в системе должно привести к повышению степени гидратации полиэтиленгликоля и привести к изменению ближайшего водного окружения молекулы ПЭГ, благоприятствующего совместимости полиэтиленгликоля и водно-солевого раствора. Добавление в систему этилового спирта (в интервале концентраций 10–30 вес %) приводит к расслоению исследуемой системы на две фазы при более низких концентрациях фазообразующих компонентов, что находится в согласии с результатами измерения структурной температуры этих растворов [13]. Как было показано ранее [11, 14], этанол в указанном интервале концентраций структурирует воду, что должно отразиться на изменении водного окружения молекулы полиэтиленгликоля и, как следствие, на более раннем расслоении системы на две водные фазы. Добавление тиокарбамида практически не сказывается на положении бинодали водной двухфазной системы ПЭГ-6000 – цитрат натрия. Ранее было показано [13, 14, 20], что тиокарбамид не влияет на состояние воды, чем и объясняется отсутствие влияния его на положение бинодали указанной системы. Полученные данные подтверждают ранее высказанное предположение [5, 20], что фазовое расслоение в водных системах ПЭГ – соль происходит вследствие возникновения в них двух различных водных структур, образующихся за счет разной ориентации молекул воды вблизи молекул фазообразующих компонентов и их ионов. Добавление к таким водным системам веществ, разрушающих структуру воды, будет препятствовать возникновению таких различных водных структур, в то время как добавление веществ, структурирующих воду, должно благоприятствовать образованию двух различных не совместимых друг с другом водных структур, служащих основой водных фаз, на которые распадается система.
Библиографическая ссылка
Масимов Э.А., Оджагвердиева С.Я., Шахвердиев Я.Х., Багиров Т.О. ВЛИЯНИЕ МОЛЕКУЛЯРНОЙ МАССЫ ПОЛИЭТИЛЕНГЛИКОЛЯ, ТЕМПЕРАТУРЫ И НЕКОТОРЫХ ДОБАВОК НА ФАЗОВУЮ ДИАГРАММУ ДВУХФАЗНОЙ СИСТЕМЫ ПЭГ – ЦИТРАТ НАТРИЯ – ВОДА // Успехи современного естествознания. 2015. № 11-1. С. 65-69;URL: https://natural-sciences.ru/ru/article/view?id=35672 (дата обращения: 12.05.2026).



