Пористые углеродные материалы нашли широкое применение в процессах сорбции и катализа [4], что обусловлено рядом их специфических физико-химических свойств (высокие удельная поверхность, механическая прочность, химическая и термическая стабильность, низкие электрическое сопротивление и теплопроводность) [2, 8] и доступностью. По каталитическим свойствам катализаторы на углеродных носителях часто превосходят катализаторы на оксидных носителях. На основе углеродных носителей получают широкий набор катализаторов для крупнотоннажных химических процессов [4].
Темой данного исследования является создание композиционных материалов «металл – углеродный носитель» на основе различных видов углерода (многослойные углеродные нанотрубки (МУНТ), технический углерод (ТУ) и композиционный углерод-углеродный материал «Сибунит») и металлов (Ag, Ni, Co), исследование их физико-химических свойств и возможности использования в качестве катализаторов низкотемпературного процесса окисления кумола.
Материалы и методы исследования
В качестве углеродных носителей в работе использовали: многослойные углеродные нанотрубки (МУНТ) «BaytubesC 150 P» (Bayer MaterialScience AG) с числом слоёв 3–15, диаметром 13–16 нм, длиной 1–10 мкм (НТ (Б)); технический углерод (ТУ) марки П354; углерод-углеродный композиционный материал «Сибунит» (Сибунит). ТУ и Сибунит получены в Институте проблем переработки углеводородов СО РАН (г. Омск). Поверхность Сибунита представлена пиролитическим углеродом [5]. ТУ содержит С 96,4 %, О 2,5 %, S 0,5 %, N и H по 0,3 % [6].
Рентгено-фазовый анализ проводили на рентгеновском дифрактометре Shimadzu XRD 7000.
ИК-спектры регистрировались на ИК-Фурье-спектрометре Nicolet 5700 в матрице KBr в области частот 400–4000 см–1 с разрешением 4 см–1 и количеством сканов 32.
Исследование размера и формы частиц наноструктур проводили с помощью метода просвечивающей электронной микроскопии на электронном микроскопе JEM-100 CX II JEOL в ЦКП «НАНОТЕХ» ИФПМ СО РАН (ЦКП ТНЦ СО РАН).
Изотерма адсорбции молекулярного азота при температуре 77,4 K получена на анализаторе поверхности и пористости Micromeritics ASAP 2020. Расчет удельной поверхности проводился по методу БЭТ.
Процесс низкотемпературного окисления кумола проводили в стеклянном реакторе барботажного типа на газометрической установке при 60 °С и атмосферном давлении. После реакции смесь анализировали методом газовой хроматографии на хроматографе Agilent 7890A.
Результаты исследования и их обсуждение
При создании композиционных материалов использовали 3 вида углеродных носителей – многослойные углеродные нанотрубки (УНТ), технический углерод (ТУ) и углерод-углеродный композиционный материал «Сибунит» (Сибунит).
Есть определенные черты, которые роднят все испытуемые углеродные носители. Они построены из полиароматических слоёв атомов углерода и являются разновидностями семейства углеродных материалов, в которых пространственная ориентация и гибридизация атомов углерода различна. Атомы углерода в углеродных нанотрубках находятся в sр2-гибридизации и имеют 3D размерную пространственную конфигурацию. ТУ также относится к 3D структурам, но атомы углерода в них находятся в sp1- и sp2-гибридных состояниях. Пиролитический углерод находится в sр2-гибридном состоянии и имеет 2D размерную пространственную конфигурацию [7]. Можно отметить и некоторые особенности каждого из углеродных носителей.
К преимуществам углеродных нанотрубок можно отнести необычную электронную структуру их графеновых стенок – при скручивании графеновой плоскости двойные связи -С=С– приобретают повышенную реакционную способность, приближаясь по характеру к двойным связям фуллеренов, и поэтому УНТ могут образовывать поверхностные π-комплексы с металлами.
Характерной особенностью Сибунитов является тип пористой структуры. Они являются преимущественно мезопористыми материалами.
ТУ получен путём термоокислительного пиролиза углеводородов с последующим окислением 20 % раствором пероксида водорода при 100 °С. Особенностью ТУ является наличие на его поверхности протоногенных функциональных групп – центров ионной адсорбции [5]. Методом РФЭС показано, что кислород в составе технического углерода находится в гидроксильных, карбонильных, эфирных и карбоксильных группах.
Для создания композиционного материала «металл-углерод» на поверхность углеродного материала наносили наночастицы металлов (Ag, Ni и Ni совместно с Co). Наночастицы серебра наносили методом ионной адсорбции или пропитки (IMP) материала солью металла (Ag(NO3)) в различных растворителях с последующим выделением, сушкой и прокаливанием при температуре 300–310 °С (Ag-МУНТ, Ag-ТУ, Ag-Сибунит). Для нанесения наночастиц переходных металлов (никеля и никеля совместно с кобальтом) на поверхность углеродных носителей использовали метод химического восстановления металлов из растворов их солей гипофосфитом натрия (Ni–Co-МУНТ, Ni–Co-ТУ). Данный метод используется достаточно широко в гальванотехнике для нанесения никеля (химическое никелирование) на компактные изделия (металлы и сплавы) [1]. К преимуществам метода можно отнести получение дисперсного покрытия и равномерность нанесения металла на подложку. Работ, посвященных нанесению металлов на неметаллы, полимерные и дисперсные покрытия методом химического восстановления на неметаллы, значительно меньше.
Процесс химического никелирования по своему механизму является электрохимическим (хотя и осуществляется без протекания электрического тока в системе). В основе способа лежит окислительно-восстановительная реакция восстановления иона никеля до металла с помощью восстановителя:
NiCl2 + 2NaH2PO2 + 2H2O → Ni + 2NaH2PO3 + H2 + 2HCl. (1)
Происходит восстановление ионов никеля (Ni 2+ ) до металлического никеля и ионов Н+ до газообразного водорода, а также окисление гипофосфит иона 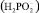 до фосфит-иона
до фосфит-иона 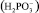 (степень окисления фосфора возрастает от +1 до +3). Таким образом, в системе протекают параллельные электрохимические реакции:
(степень окисления фосфора возрастает от +1 до +3). Таким образом, в системе протекают параллельные электрохимические реакции:
1) катодное восстановление ионов никеля и водорода:
Ni +2 + 2e- → Ni0; (2)
2H+ + 2e- → H2О; (3)
2) анодное окисление гипофосфит-иона:
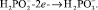 (4)
(4)
Следует отметить, что нанести никель и кобальт на поверхность Сибунита методом химического восстановления не удалось, что, вероятно, может быть связано с почти полным отсутствием функциональных групп на поверхности Сибунита. Полученный композиционный материал имеет развитую поверхность, сравнимую по своим параметрам с поверхностью исходных углеродных материалов (таблица).
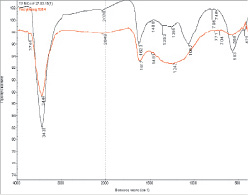
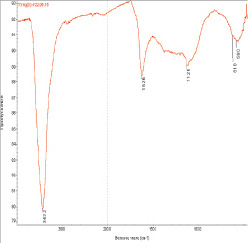
ИК-спектры композиционных материалов на примере композиций «ТУ-металл» представлены на рис. 1.
Удельная поверхность и размер пор композиционных материалов
|
НТ |
ТУ |
Сибунит |
Ni–Co-НТ |
Ni–Co-ТУ |
Ag-ТУ |
Ag-НТ |
Ag-Сибунит |
|
|
Sуд, м2/г |
170 |
110 |
319 |
168,2 |
107,4 |
108,3 |
169,1 |
310,5 |
|
Vпор, см3/г |
0,043 |
0,034 |
0,068 |
0,04 |
0,031 |
0,038 |
0,041 |
0,065 |
|
d, нм |
1,95 |
1,9 |
1,8 |
1,75 |
1,8 |
1,87 |
1,75 |
1,79 |
Наблюдается небольшое смещение полос, отнесенных к колебаниям –С–С– связей на частотах 1057 и 1126 см–1 и увеличивается интенсивность полос на частотах 563 и 580 см–1 (колебания связи –М–С–). Следует отметить, что полосы на частотах 563 и 580 см–1 наблюдались и ранее при нанесении наночастиц никеля, кобальта и серебра на поверхность углеродных нанотрубок [9, 3]. Квантово-химический расчет модельного соединения AgC2 методом B3LYP/DGDZVP дает валентные колебания Ag–C в области 480–500 см–1, деформационные – в области 580 см–1.
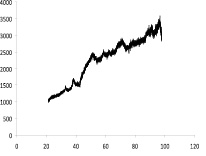
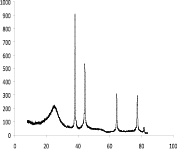
Рентгенограммы композиционных материалов представлены на рис. 2.
На рентгенограмме композиционного материала ТУ-Ni–Co (рис. 2, а) просматриваются уширенные, размытые пики никеля (38,42; 44,555; 58,462; 71,074) и кобальта (43,838; 51,731). Уширение пиков может свидетельствовать об аморфном характере нанесенного покрытия.
Ранее показано, что при восстановлении металлов из растворов их солей гипофосфитом натрия совместно с осаждением никеля соосаждается фосфор по реакции (5), который входит в кристаллическую решетку никеля, образуя аморфное никель-фосфорное покрытие.
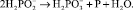 (5)
(5)
На рентгенограмме композиционного материала ТУ-Ag (рис. 2, б) четко просматриваются пики кристаллического серебра (38,087; 44,27; 64,42; 77,39; 81,551) и углерода (25,414).
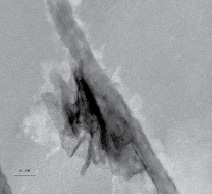
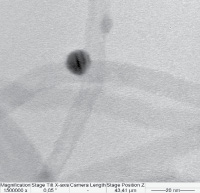
Микрофотографии композиционных материалов на примере углеродных нанотрубок представлены на рис. 3.
Каталитическую активность композиционных материалов изучали в реакции окисления кумола молекулярным кислородом при температуре 40–60 °С кинетическим методом. Скорость процесса окисления оценивали по скорости поглощения кислорода системой кумол - катализатор. Окисление кумола в гидропероксид кумола (ГПК) является одной из стадий в «кумольной» технологии крупнотоннажного производства фенола и ацетона, реализованного в промышленности. Это типичный свободнорадикальный процесс, осуществляемый при температуре 100–130 °С с конверсией 20–30 %. Процесс требует повышенного потребления электроэнергии, кроме этого, уже при температуре 90–100 °С начинается термическое разложение ГПК. Использование в качестве катализатора полученного композиционного материала позволило провести процесс при температуре 60 °С без инициатора и с увеличенной скоростью. Следует отметить, что при температуре 60 °С без инициатора и катализатора процесс окисления кумола фактически не идет.
а
б
Рис. 1. ИК-спектры композиционных материалов ТУ-Ag (а) и ТУ-Ni–Co (б)
а б
Рис. 2. Рентгенограмма композиционного материала ТУ-Ag (а) и ТУ-Ni–Co (б)
а б
Рис. 3. Микрофотографии композиционных материалов: МУНТ-Ni–Co (а); МУНТ-Ag (б)
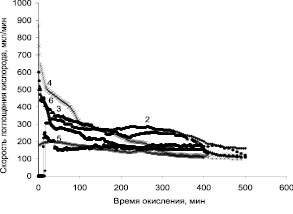
Рис. 4. Зависимость изменения скорости поглощения кислорода от времени при окислении кумола в присутствии композиционных материалов «металл – углеродный носитель»: 1 – Ag-НТ; 2 – Ag-Сибунит; 3 – Ag-ТУ; 4 – Ni–Co-ТУ; 5 – Ni–Co-ТУ (катализатор после восстановления); 6 – Ni–Co-НТ
Согласно изображению на микрофотографиях никель находится на поверхности углеродных нанотрубок в виде очень тонких пластин (рис. 3, а), а серебро имеет кристаллическую структуру (dкр = 1–20 нм) (рис. 3, б).
На рис. 4 представлена зависимость изменения скорости поглощения кислорода от времени при окислении кумола в присутствии композиционных материалов «металл – углеродный носитель».
Согласно рисунку окисление кумола проходит достаточно активно в присутствии всех исследованных катализаторов, но с более постоянной скоростью – при температуре 40 °С на катализаторе ТУ-Ag (рис. 4, кривая 2). Таким образом, композиционные материалы на основе активированных металлами углеродных носителей обладают высоким потенциалом для применения их в качестве гетерогенных катализаторов процесса окисления кумола.
Выводы
1. Созданы композиционные материалы «металл-углерод» на основе различных видов углерода (многослойные углеродные нанотрубки, технический углерод, углерод-углеродный материал Сибунит) и металлов (Ag, Ni, Co) и изучены их физико-химические свойства.
2. Методом РФА и ПЭМВР показано, что серебро находится на поверхности углеродных носителей в кристаллическом состоянии и имеет размеры 10–20 нм, никель в виде аморфизированной пластинчатой структуры.
3. Использование активированных металлами углеродных наноматериалов в качестве катализаторов процесса окисления кумола позволяет существенно снизить температуру и повысить селективность.
Библиографическая ссылка
Коботаева Н.С., Скороходова Т.С., Раздьяконова Г.И., Полещук О.Х. СОЗДАНИЕ И ИССЛЕДОВАНИЕ ФИЗИКО-ХИМИЧЕСКИХ СВОЙСТВ КОМПОЗИЦИОННЫХ МАТЕРИАЛОВ «МЕТАЛЛ ‒ УГЛЕРОДНЫЙ НОСИТЕЛЬ» // Успехи современного естествознания. 2016. № 6. С. 25-30;URL: https://natural-sciences.ru/ru/article/view?id=35960 (дата обращения: 14.04.2026).



