Синдром Смита – Лемли – Опитца (СЛОС) – генетическое заболевание, характеризующееся нарушением биологического синтеза холестерина и симптоматически выражающееся в развитии у пациента пороков сердца, легких, почек, пищеварительного тракта, а также нарушении работы иммунной системы. Частота заболеваемости составляет 1 на 20000–40000 новорожденных [8, 13].
При лечении данного заболевания, как правило, проводят заместительную терапию, посредством включения в диету содержащих холестерин пищевых продуктов. Как правило, в качестве подобных продуктов выступают желтки куриных яиц, молочные и мясные продукты. В данной работе в качестве объектов исследования были выбраны кисломолочные продукты, применяемые в заместительной терапии СЛОС.
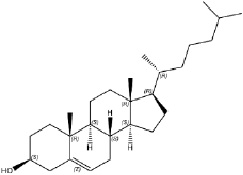
Рис. 1. Структурная формула холестерина (5-холестен-3βола)
Наиболее распространенными в анализе пищевых продуктов являются хроматографические методики, что обусловлено высокой чувствительностью, точностью и простотой устранения мешающего влияния матрицы пробы [4, 6, 9]. Тем не менее данный тип методик имеет также ряд недостатков. Прежде всего, высокая стоимость оборудования, а также необходимая высокая квалификация персонала. Помимо этого, низкая эффективность в поточном лабораторном анализе. Электрохимические методы анализа характеризуются как высокой чувствительностью, так и высокой точностью, а также простотой исполнения и относительной дешевизной оборудования. В связи с чем в данной работе в качестве основной аналитической техники была выбрана электрохимия.
Известно, что электрохимическое определение большинства органических молекул с молярной массой более 100 г/моль требует применения высоких перенапряжений [1]. В связи с чем, большинство вольтамперометрических методик определения органических соединений основано на применении модификаторов электродной поверхности. Известно, что модифицированные электроды, в том числе органическими соединениями [2], можно с успехом применять для определения различных биологически активных веществ [1, 2]. В данной работе в качестве модификатора применялся фталоцианин кобальта (ФК). Поскольку кобальт, являясь металлом переходной группы, способен выступать в качестве медиатора электронного переноса и электрокатализатора [1, 6].
Основной целью данной работы явилась разработка методики вольтамперометрического определения холестерина в продуктах питания (в том числе кисломолочных продуктах) с применением модифицированного платинового электрода. В качестве метода сравнения использовался флюориметрический метод определения холестерина по реакции Златкиса – Зака.
Материалы и методы исследования
В качестве объекта исследования выступал холестерин, полученный из кисломолочных продуктов (сметана, кефир, ряженка) путем жидкофазной экстракции.
В качестве стандартного вещества для сравнения использовали лиофилизированный порошок холестерина (C8667-25G, содержание чистого вещества ≥ 99 % производства Sigma Aldrich, Германия). Фталоцианин кобальта (II) приобретался в виде лиофилизированного порошка (307696, содержание чистого вещества ≥ 95 % производства Sigma Aldrich, Германия).
Поскольку холестерин отличается низкой растворимостью в водных средах, применяли эмульгирующий агент – t-октилфеноксиполиэтоксиэтанол (Triton X-100) (Т8787, содержание чистого вещества ≥ 96 % производства Sigma Aldrich, Германия).
Электрохимические исследования проводили на универсальном вольтамперометрическом анализаторе ТА-Lab (ООО «Томьаналит», г. Томск, Россия).
Флюориметрическое определение холестерина проводили на спектрофлюориметре Hitachi F-7000 (Hitachi Ltd, Япония).
Пробоподготовка образцов продуктов питания
Пробоподготовка осуществлялась жидкостной экстракцией изопропанолом. Образец помещали в пробирку типа Эппендорф, куда также вносился изопропиловый спирт (в соотношении 1:1), после чего проводили центрифугирование при 4000 об/мин в течение 40 минут. Затем полученный супернатант собирали и декантировали. Полученный декантат использовался для дальнейших исследований.
Вольтамперометрическое определение холестерина
В работе использовалась трехэлектродная ячейка, состоящая из модифицированного платинового электрода (ПЭ), как рабочего электрода. В качестве электрода сравнения и вспомогательного электрода применяли хлоридсеребряные электроды.
Декантат в объеме 10 мкл отбирался дозатором со сменным наконечником и вносился в кварцевый стакан объемом 20 мл, в который предварительно наливалось 10 мл рабочего электролита. После чего осуществлялось перемешивание посредством стационарной вибрации рабочего электрода в течение 10 с. Затем проводилось успокоение системы в течение 20 с. После чего, осуществлялась регистрация полученного тока в постояннотоковом режиме с дифференцированием при скорости развертки потенциала υ = 60 мВ/с, рабочий диапазон потенциалов от + 0,5 до + 1,0 В. Накопление аналита в приэлектродном пространстве не проводилось.
Флюориметрическое определение холестерина
Предварительно подготавливался окрашивающий агент, состоящий из растворенного в смеси кислот (ледяной уксусной и концентрированной серной кислот) хлорида железа (III) шестиводного. Концентрация хлорида железа (III) в растворе составила 0,93 моль/дм3.
Затем смешивались равные объемы окрашивающего агента и декантата, переносились в кювету. Проводилась регистрация интенсивности флюоресценции.
Исследования проводились при следующих условиях: время интеграции 1 с, спектральная пропускная способность канала 2 нм, шаг сканирования 0,1 с.
Результаты исследования и их обсуждение
Для определения холестерина вольтамперометрически на модифицированном стеклоуглеродном электроде подобраны следующие рабочие параметры: дифференциальный режим постояннотоковой вольтамперометрии, рН рабочего электролита составил 6,86, скорость развертки потенциала – 60 мВ/с. Полученный аналитический сигнал применялся для количественного определения холестерина в кисломолочных продуктах.
Для построения градуировочного графика приготавливалась серия стандартных растворов холестерина различной концентрации и измерялась высота тока электроокисления холестерина в одинаковых условиях. Затем строился график зависимости высоты аналитического сигнала от его концентрации в растворе. Прямолинейный характер зависимости сохраняется в интервале концентраций от 0,8 до 80 ммоль/дм3 (рис. 2) и описывается уравнением Iп = 10,495•С + 1,5041 (Iп, нА; С, ммоль/дм3) с r = 0,9978. Предел обнаружения, рассчитывали по 3σ критерию [12]. Значение предела обнаружения составило 0,1 ммоль/дм3. Относительное стандартное отклонение Sr не превышает 8,2 % во всем диапазоне исследуемых концентраций.
С помощью предложенной методики было определено содержание холестерина в ряде кисломолочных продуктов. На рис. 3 показана анодная вольтамперограмма окисления холестерина, содержащегося в стандартных растворах холестерина (производства Sigma Aldrich, Германия). Добавка стандартного раствора холестерина известной концентрации приводит к росту тока пика электроокисления холестерина при потенциале + 0,77 В. Следовательно, полученный аналитический сигнал исследуемого образца молока обусловлен электроокислением холестерина. Нахождение концентрации холестерина в исследуемых образцах продуктов питания проводили по градуировочному графику.
Проводились исследования влияния pH среды на получаемый аналитический сигнал с целью подбора рабочих условий измерения содержания холестерина в образцах объектов. Результаты исследования представлены на рис. 4–5.
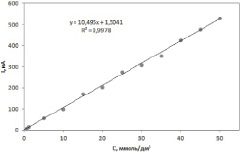
Рис. 2. Зависимость тока электроокисления холестерина от его концентрации в фосфатном буферном растворе (pH = 6,86) на модифицированном ПЭ
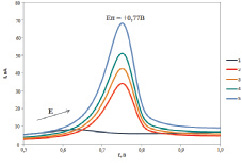
Рис. 3. Вольтамперограммы электроокисления холестерина: 1 – фоновая кривая (Cхол = 0,0 ммоль/дм3); 2 – концентрация холестерина в ячейке составляет 0,8 ммоль/дм3; 3 – концентрация холестерина в ячейке составляет 1,6 ммоль/дм3; 4 – концентрация холестерина в ячейке составляет 3,2 ммоль/дм3; 5 – концентрация холестерина в ячейке составляет 6,4 ммоль/дм3. pH 6,86, υ = 60 мВ/с
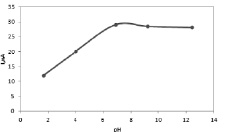
Рис. 4. Влияние pH среды на величину тока окисления холестерина на модифицированном ПЭ
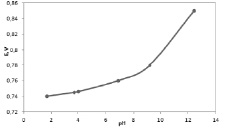
Рис. 5. Влияние pH среды на величину потенциала пика окисления холестерина на модифицированном ПЭ
В качестве метода сравнения применялся флюориметрический метод с применением реакции Златкиса – Зака, заключающийся в измерении оптической плотности раствора, содержащего окрашенный комплекс холестерина с хлорным железом (III) при характеристической длине волны. Для определения длины волны, соответствующей максимуму светопоглощения, были записаны спектры стандартного раствора холестерина и образцов продуктов питания в интервале длин волн 400–650 нм. Установлено, что максимум поглощения как для стандартного раствора, так и для исследуемого кисломолочного продукта соответствует 475,0 нм, что совпадает с литературными данными [5, 7, 15].
На рис. 5–6 представлены результаты построения градуировочной зависимости для определения количественного содержания холестерина методом флюориметрии по Златкису – Заку. Показано, что градуировочная зависимость линейна в широком диапазоне концентраций. Для построения зависимости готовили серию стандартных растворов из стандартного порошка холестерина и записывали спектры поглощения, на основании которых был построен график зависимости величины пика поглощения от концентрации холестерина в кювете (рис. 7).
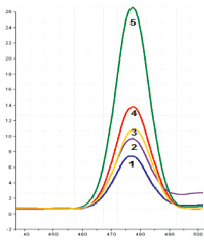
Рис. 6. Спектры поглощения комплекса железа (III) с холестерином в зависимости от концентрации холестерина в объекте исследования, концентрация холестерина составляет: 1 – 10 ммоль/дм3; 2 – 20 ммоль/дм3; 3 – 30 ммоль/дм3; 4 – 40 ммоль/дм3; 5 – 50 ммоль/дм3
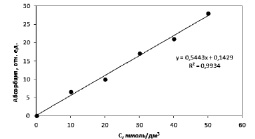
Рис. 7. Зависимость величины пика поглощения холестерина от его концентрации в стандартном растворе
Результаты определения холестерина (ммоль/дм3) в продуктах питания вольтамперометрическим и флюориметрическим методами. n = 6, p = 0,95, tтаб = 2,57
|
Образец |
Производитель |
Вольтамперометрия |
Sr |
Флюориметрия |
Sr |
tэксп |
|
Сметана, жирность 10 % |
«Деревенское молочко» |
58,06 ± 4,65 |
0,08 |
73,21 ± 3,67 |
0,05 |
1,65 |
|
«Простоквашино» |
57,16 ± 2,86 |
0,05 |
64,63 ± 5,17 |
0,08 |
2,08 |
|
|
«Домик в деревне» |
48,18 ± 0,23 |
0,05 |
45,37 ± 1,36 |
0,03 |
1,87 |
|
|
Кефир, жирность 2,5 % |
«Простоквашино» |
18,02 ± 1,44 |
0,03 |
17,47 ± 0,67 |
0,04 |
2,01 |
|
«Деревенское молочко» |
17,56 ± 1,22 |
0,07 |
18,23 ± 0,92 |
0,05 |
1,95 |
|
|
«Домик в деревне» |
15,47 ± 0,62 |
0,04 |
16,26 ± 1,46 |
0,09 |
1,72 |
|
|
Ряженка, жирность 4 % |
«Деревенское молочко» |
16,48 ± 1,32 |
0,08 |
16,35 ± 1,12 |
0,07 |
1,23 |
|
«Простоквашино» |
15,75 ± 0,47 |
0,03 |
16,09 ± 0,96 |
0,06 |
2,12 |
|
|
«Домик в деревне» |
15,84 ± 0,79 |
0,05 |
16,01 ± 1,12 |
0,07 |
1,54 |
Для определения содержания холестерина проводили предварительную пробоподготовку образца продукта питания, согласно описанной выше процедуре.
Затем собранный и декантированный супернатант смешивали с окрашивающим агентом (хлорид железа (III), растворенный в смеси кислот) по методике [12, 15]. Затем проводили регистрацию спектра поглощения и по уравнению регрессии Abs = 0,5443•C + 0,1429 (R = 0,9934) определяли концентрацию холестерина в образце с учетом разбавления. Результаты определения содержания холестерина двумя методами представлены в таблице.
При сопоставлении параметров линейности и относительных стандартных отклонений можно сделать вывод об удовлетворительной сходимости между результатами, полученными по вольтамперометрической и флюориметрической методикам анализа.
Полученные результаты хорошо согласуются с литературными данными [3, 5, 7, 10].
Таким образом, проведённые исследования показывают, что процесс электроокисления холестерина на модифицированном ПЭ сильно зависит от водородного показателя фонового электролита, что соответствует применению эмульгирующего агента амфолитной природы. Причём наибольшая величина аналитического сигнала соответствует рН = 6,86. На основании данных циклической вольтамперометрии и характера зависимостей тока и потенциала от υ1/2 и log(υ1/2) соответственно установлено наличие двух лимитирующих стадий процесса: диффузии вещества в приэлектродное пространство и непосредственно электрохимической реакции. По результатам определения холестерина в модельных средах проведен подбор рабочих условий определения холестерина в продуктах питания методом вольтамперометрии. Проведено сравнительное определение холестерина в ряде продуктов питания с применением вольтамперометрической и флюориметрической методик. Полученные результаты согласуются между собой.
Таким образом, применение фталоцианина кобальта (II) в качестве модификатора электродной поверхности позволило получить стабильный электрохимический отклик при + 0,77 В в анодной области потенциалов. На основе полученного сигнала была разработана методика определения холестерина в кисломолочных продуктах, которая может применяться как для контроля качества пищевой продукции, так и для повышения успешности терапии аутосомальных заболеваний.
Данная работа поддержана Российским фондом фундаментальных исследований (грант РФФИ № 16-33-00319 мол_а «Мой первый грант»).
Библиографическая ссылка
Дёрина К.В. ВОЛЬТАМПЕРОМЕТРИЧЕСКОЕ ОПРЕДЕЛЕНИЕ СОДЕРЖАНИЯ ХОЛЕСТЕРИНА В КИСЛОМОЛОЧНЫХ ПРОДУКТАХ // Успехи современного естествознания. 2016. № 9. С. 14-19;URL: https://natural-sciences.ru/ru/article/view?id=36112 (дата обращения: 10.06.2026).



