Адсорбционные процессы занимают лидирующее положение в вопросах осушки природного газа от влаги и нежелательных компонентов, создана обширная база изотерм адсорбции различных газов, это бутан, этан, пропан, метан и др. Но, к сожалению, исследователи, занимающиеся разработкой теории адсорбции для газов, мало внимания уделили адсорбции растворов, и в этом направлении есть незаполненные моменты.
На сегодняшний день появились модифицированные адсорбенты, которые позволяют осуществлять тонкую осушку спиртов и других растворов на основании избирательной адсорбции на цеолитах. Цеолиты – это алюмосиликаты, содержащие в своем составе оксиды щелочных и щелочноземельных металлов, – отличаются строго регулярной структурой пор, которые при обычных температурных условиях заполнены молекулами воды [6].
Общая химическая формула цеолитов Me2/nO•Al2O3•xSiO2•yH2O. (где Me – катионы щелочного металла, а n – его валентность). В природе в качестве катионов обычно в состав цеолитов входят натрий, калий, кальций, реже барий, стронций и магний [6]. Кристаллическая структура цеолитов образована тетраэдрами SiO4 и AlO4 (атомы Al и Si принято классифицировать как Т атомы), связанные друг с другом общим ионом кислорода.
В природе цеолиты распространены достаточно обширно и часто встречаются. Они образовались в результате изменения вулканических туфов в морских и континентальных бассейнах и таких образом представляют туфогенный – осадочный тип месторождений. Катионы, входящие в состав цеолитов, под действием среды могут замещаться на ионы других металлов. Варьирование условий гидротермального синтеза и протекание реакций катионного обмена [6] в природных условиях предопределило большое разнообразие типов природных цеолитов.
Синтетические цеолиты получаются при нагревании водных щелочных алюмосиликатных смесей, т.е. смесей, содержащих в качестве обязательных компонентов воду, щелочь, SiO4 и AlO4.Таким путем синтетические цеолиты были получены еще в прошлом веке, однако до конца 40-х гг. нашего столетия работы в области синтеза цеолитов были эпизодическими, а полученные кристаллические фазы часто не были чистыми и надежно идентифицированными [5].
Цеолиты являются молекулярными ситами [1, 1]. Их широкое применение объясняется тем, что они могут быть использованы для разделения веществ не только на основе избирательности адсорбции, но и на основе разницы в размерах и форме поглощаемых молекул. Для того чтобы проникнуть в адсорбционную полость, критический диаметр молекул адсорбата должен быть меньше размера входного окна [6]. В России наиболее распространенными являются пять видов цеолитов и их модификации.
Основным фактором, определяющим молекулярноситовые свойства, является размер входных окон цеолитов, который зависит от расположения кислородных колец цеолита и от числа атомов кислорода в кольце. Также на размер входного окна оказывает влияние размер катиона, входящего в состав цеолита. Катионы, расположенные близко к окну, блокируют вход для молекул. Например, при катионном обмене, в котором два катиона натрия замещаются одним катионом кальция, входное окно расширяется; вследствие этого цеолит Na имеет размер входного окна 4 A, а цеолит СаА имеет размер 5 A [6]. Аналогичный обмен в цеолите типа X приводит к некоторому сужению окна. Рассматривая свойства цеолита КА, можно пояснить, что при обычной температуре данный вид цеолита очень хорошо сорбирует воду. Данное свойство предупредило его применение для осушки нестойких веществ, склонных к реакциям полимеризации.
Если рассматривать свойство цеолита NaA, который способен сорбировать большинство компонентов промышленных газов, критический размер молекул которых не превышает 4 A: сероводород, сероуглерод, двуокись углерода, аммиак, низшие диеновые и ацетиленовые углеводороды, этан, этилен, пропилен, органические соединения с одной метильной группой в молекуле, а также метан, неон, аргон, криптон, ксенон, кислород, азот, окись углерода [6]. Последняя группа веществ в значительных количествах поглощается только при низких температурах. Пропан и органические соединения с числом атомов углерода в молекуле более 3 не адсорбируются цеолитом и таким образом при осушке и очистке не подавляют адсорбцию указанных выше примесей.
Цеолиты марки СаА адсорбируют углеводороды и спирты только нормального строения, в связи с чем широко используются в процессах разделения многокомпонентных органических веществ на молекулярноситовой основе. Кроме того, цеолит СаА поглощается метил и этилмеркаптаны, органические соединения с числом атомов углерода в молекуле 2 (этиловый спирт, этиламин), диборан и др. Среди цеолитов общего назначения типа СаА отличается повышенной стойкостью в слабокислой среде и поэтому его используют в процессах сероочистки и декарбонизации газов.
Цеолиты типа Х имеют достаточно широкие входные окна и адсорбируют подавляющее большинство компонентов сложных смесей: все типы углеводородов органические сернистые, азотистые и кислородные соединения (меркаптаны, тиофен, фуран, хинолин, пиридин, диоксан и др.), галоидозамещенные углеводороды (хлороформ, четыреххлористый углеводород, фреоны), пентаборан и дeкаборан [2, 7]. Применение цеолитов СаХ и NаХ основано на избирательности адсорбции, а не на молекулярно-ситовых свойствах. При полном замещении катиона натрия на кальций цеолит СаХ, в отличие от цеолита NaX, не адсорбирует ароматические углеводороды или их производные с разветвленными радикалами, например 1,3,5-триэтилбензол и метадихлорбензол. На этом свойстве основан метод идентификации цеолитов этих двух типов и установление полноты ионного обмена при получении цеолита СаХ.
В случае, если критический диаметр молекулы близок к диаметру входного окна, процесс адсорбции происходит с большой энергией активации и aдcopбируемая молекула должна обладать определенным запасом кинетической энергии для преодоления энергетического барьера. Кинетическая энергия молекул повышается с ростом температуры [7]. Одновременно повышение температуры приводит к усилению термической пульсации решетки цеолита, что облегчает проникание молекулы в адсорбционную полость. Таким образом, изменением температурного режима можно достигнуть такого рубежа, при котором молекулы адсорбтива начнут поглощаться цеолитом.
Цеолит КА сорбирует – Не, Н2, Н2О, цеолит NaA сорбирует – инертные газы СН4, углеводороды С2, С3Н6, СО2, СS2, Н2S, CН3ОН, NH3, CH3CN, CH3NH2,CH3Cl, CH3Br [1]. Цеолит СаА сорбирует – н-алканы С2Н5ОН, С2Н2Сl, С2Н2Br, CH2Br2, (CC3)2NH, CH3I, цеолит СаХ сорбирует – разветвленные алканы и спирты, бензол, цеклогексан и их низшие гомологи [1]; Цеолит NaX – 1,3,5 сорбирует – триэтилбензол, 1,3-дихлорбензол [(н-С4F9)3N].
1. Цеолит КА при обычной температуре в значительных количествах поглощает только воду. Это свойство предопределило широкое применение его для осушки нестойких веществ, склонных к реакциям полимеризации.
2. Цеолит NaA адсорбирует большинство компонентов промышленных газов, критический размер молекул которых не превышает 4 A: сероводород, сероуглерод, диоксид углерода, аммиак, низшие диеновые и ацетиленовые углеводороды, этан, этилен, пропилен, органические соединения с одной метильной группой в молекуле, а также метан, неон, аргон, криптон, ксенон, кислород, азот, оксид углерода.
3. Цеолит СаА адсорбирует углеводороды и спирты только нормального строения (независимо от длины цепи), в связи с чем широко используется в процессах разделения многокомпонентных органических веществ на молекулярноситовой основе. Кроме того, цеолитом СаА поглощаются метил- и этилмеркаптаны, органические соединения с числом атомов углерода в молекуле, равным двум (этиловый спирт, этиламин, диборан и др.). Цеолит СаА среди синтетических цеолитов других типов отличается повышенной стойкостью в слабокислой среде, и поэтому его используют в процессах сероочистки и декарбонизации газов.
Цеолит СаХ при полном замещении катиона натрия на кальций, в отличие от цеолита NаХ, не адсорбирует ароматические углеводороды или их производные с разветвленными радикалами
4. Цеолит NaХ имеет достаточно широкое входное окно и адсорбирует подавляющее большинство компонентов сложных смесей: все типы углеводородов, органические сернистые, азотистые и кислородные соединения (меркаптаны, тиофен, фуран, хинолин, пиридин, диоксан и др.), галогензамещенные углеводороды (хлороформ, четыреххлористый углеводород, фреоны), пентаборан и декаборан [7].
Цеолиты являются наиболее оптимальными адсорбентами для паров воды. Их отличием от других адсорбентов, к примеру от силикагеля, является способность адсорбировать уже при температуре 100 °С пары воды. Их адсорбционная емкость при обычных температурах и давлении порядка 200 Па уникальна. Высокие скорости адсорбции влаги позволяют использовать их короткий слой адсорбента в динамических процессах. Область применения цеолитов очень обширна от осушки воздуха до катализатора в химических реакциях, а также осушки в газовой и нефтеперерабатывающей промышленности [7].
Осушка в газовой промышленности. На газобензиновых заводах использование умеренного и глубокого холода в технологических процессах позволяет увеличить степень извлечения легких фракций углеводородов, решить проблему ожижения природного газа, отделить несконденсированный остаток гелия. На установках сжижения газа происходит охлаждение до –160 °С, а на гелиевых заводах и до –170 °С. Данная технология стала доступной благодаря применению цеолитов, которые обеспечивают продолжительную непрерывную эксплуатацию аппаратуры разделения в этих условиях. Глубокая и надежная осушка транспортируемого наземным транспортом газа в холодном климате возможна при использовании цеолитов.
Осушка природного газа на промыслах. Газ, выходящий из скважины, насыщен водяными парами, и в зимний период эксплуатация скважины и транспортировки продуктов добычи до газосборного пункта сопровождается выпадением гидратов [7]. Во избежании выпадения гидратов необходимо предусмотреть в технологической цепочке стадию осушки природного газа методами адсорбции, в качестве адсорбента используется цеолит, который обеспечивает более высокую осушку по сравнению с силикагелем.
Осушка газа на газобензиновых заводах. На газобензиновых заводах природный газ из большого числа скважин собирается и подготавливается к дальнейшему транспорту по магистральным газопроводам потребителю. Если на газобензиновом заводе предусмотрено относительно неглубокое извлечение этана, точка росы газа не должна быть выше – 40 °C. На таких заводах интенсивно строятся новые и реконструируются на основе синтетических цеолитов старые адсорбционные установки. В некоторых случаях на современных газобензиновых заводах степень извлечения этана предусмотрено довести до 85–90 %, пропана – до 99 %, бутанов – практически до 100 %. Столь глубокое извлечение возможно после охлаждения газа до температуры – 90 °C. На таких заводах осушку газа ведут цеолитами до точки росы – 85 °C, одновременно цеолитами осуществляют осушку и некоторых промежуточных потоков, например верхнего продукта деэтанизатора.
Осушка природного газа, закачиваемого в пласт. После извлечения из природного газа тяжелых углеводородов (конденсата) его для поддержания давления в пласте снова закачивают в пласт. При закачке газа в пласт для уменьшения затрат на компримирование, осушку и отбензинивание целесообразно проводить при высоком давлении.
Осушка природного газа на криогенных установках. Криогенный метод применяют для сжижения природного газа и извлечения из него гелия. Низкие температуры в холодильном цикле (до –170 °C) требуют практически полного удаления паров воды из газа цеолитами. Это соответствует точке росы –100 °C. Глубокая осушка газа цеолитами полностью исключает возможность замерзания оборудования, а следовательно, и нарушения непрерывной эксплуатации криогенных установок.
Осушка в нефтеперерабатывающей промышленности. Продукты нефтепереработки значительно отличаются от природного сырья высоким содержанием непредельных углеводородов, осушка и очистка которых имеет определенные особенности.
Осушка непредельных углеводородов. При осушке непредельных углеводородов необходимо учитывать каталитическую активность цеолитов по отношению к реакции полимеризации. Каталитические свойства цеолитов связаны, с одной стороны, с наличием в кристаллитах активных кислотных центров, а с другой, – с каталитическими свойствами связующего. Кристаллит типа NaA среди цеолитов общего назначения обладает наименьшей каталитической активностью [7].
При осушке непредельных углеводородов цеолитами NaA предпочтительно предусматривать одно и то же направление потока газа на стадиях осушки и регенерации. В этом случае сорбирующиеся в первый период одновременно с водой углеводороды постепенно вытесняются водой из слоя цеолитов и уносятся с потоком осушенного газа. После наступления момента проскока адсорбер переключают на стадию регенерации, осуществляемую горячим газом. окончательное вытеснение углеводородов адсорбирующейся водой из «хвостового» слоя цеолитов заканчивается на стадии регенерации при относительно низких температурах, и таким образом снижается до минимума дезактивация адсорбента. Цеолит KА широко применяется для осушки разнообразных сред, склонных к разложению и полимеризации: этилена, бутилена, бутадиена, стирола и его смеси с н-гексаном, пентиленов, винилацетата, изопрена, дихлорметана, хлороформа, галогенсодержащих хладагентов, газов процесса Вульфа [7].
Осушка изопропилена с одновременной очисткой от изопропилового спирта. В ряде случаев технологический поток необходимо не только осушить, но и глубоко очистить от нежелательных примесей, например пропилен, используемый для получения полипропилена.
Осушка газов риформинга. При осушке циркуляционного водородосодержащего газа риформинга выбор типа адсорбента должен проводиться с учетом того, что в газе присутствуют микропримеси соляной кислоты.
Осушка сырья на установках алкилирования. На заводах алкилирования в качестве катализаторов используют плавиковую или серную кислоту. Эффективность и экономичность алкилирования во многом зависят от влагосодержания перерабатываемого сырья. Содержание влаги в исходном сырье обычно составляет 100–450 ‰. Задача глубокой осушки сырья решается при помощи цеолитов [7].
На установках алкилирования также возможно использовать цеолиты для тонкой очистки сырья от серы и бутадиена.
В данной работе будет исследован цеолит марки КАсо модифицированный на возможность осушки этилового спирта С2Н5ОН. Необходимо установить предельную концентрацию воды, при которой цеолит будет вести себя нестабильно, а также отследить динамику предельной адсорбции.
Исследование адсорбционной емкости выбранного цеолита будем проводить статистическим методом, так как он наиболее доступен в условиях лаборатории.
Результаты исследования по определению предельной адсорбции на цеолите КАсо
|
Конц. Н2О (%) |
10 |
20 |
30 |
35 |
40 |
45 |
50 |
55 |
60 |
70 |
|
Величина предельной адсорбции а (моль/г) |
||||||||||
|
1-й опыт |
0,0136 |
0,01431 |
0,0155 |
0,0157 |
0,0166 |
0,0092 |
0,01185 |
0,0096 |
0,0114 |
0,0175 |
|
2-й опыт |
0,0114 |
0,01143 |
0,01201 |
0,01173 |
0,0128 |
0,0175 |
0,0177 |
0,0178 |
0,0177 |
0,017 |
|
3-й опыт |
0,0108 |
0,01154 |
0,0108 |
0,01172 |
0,0117 |
0,0108 |
0,0104 |
0,0162 |
0,0176 |
0,017 |
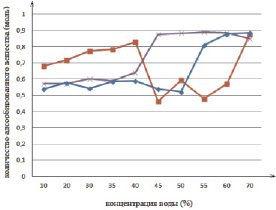
График зависимости концентрации от количества вещества
Масса исследуемого цеолита марки КАСО 50 г, спирт С2Н5ОН 96 %, вода H2О дистиллированная. Для осушки этанола использовали цеолит марки КАСО диаметр гранул 1,6 мм, насыпная плотность 0,85 г/см3, размер пор данного цеолита, заявленный производителем 3 A (0,3 нм). Объем раствора 200 мл при разных концентрациях воды. Диапазон концентрации H2О (от 10 до 70 %). Температура, при которой проводилось данное лабораторное исследование t = 24 °C и давление 0,1 МПа. Плотность смеси определяли ареометрами марки Ареометр АОН-1 (диапазон измерений 700–1840 кг/м3). Массу определяли при помощи лабораторных весов Leki 5002. Величина предельной адсорбции рассчитывается по уравнению
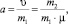
где υ – количество адсорбированного вещества, моль; m1 – масса адсорбента, г; μ – молярная масса адсорбировавшегося вещества, г/моль; m2 – масса навески адсорбента с адсорбированным веществом, г. Результаты, полученные в ходе лабораторных исследований, показаны на рисунке.
Выводы
В результате исследования авторы пришли к выводам, что использование цеолита марки КАсо при больших концентрациях воды нецелесообразно. Также авторы исследовали раствор после адсорбции и пришли к выводам, что, возможно, проходит процесс хемосорбции. Но данное утверждение требует более детального анализа и исследования другими методами. Полученные авторами результаты позволяют использовать данный адсорбент при адсорбции небольших концентраций воды и создавать технологические установки со ступенчатым циклом адсорбции [3, 4]. Полученные данные открывают перспективные технологии адсорбционных фильтров разделения азеотропных растворов методом избирательной адсорбции с использованием молекулярноситовых свойств [5].
Библиографическая ссылка
Паранук А.А., Хрисониди В.А. ИССЛЕДОВАНИЕ АДСОРБЦИОННОЙ ЕМКОСТИ ЦЕОЛИТА КАСО // Успехи современного естествознания. 2016. № 9. С. 29-33;URL: https://natural-sciences.ru/ru/article/view?id=36115 (дата обращения: 23.05.2026).



