Среди различных классов теллурорганических соединений, полученных и изученных в последние 35 лет, винилтеллуриды являются наиболее полезными и наиболее перспективными для использования в органическом синтезе [6] благодаря их легкой трансформации в другие органические соединения с сохранением конфигурации [8]. Полученные теллурорганические соединения использованы как синтоны в органической химии [15], для получения новых электропроводящих материалов [13], в качестве предшественников таких молекулярных фрагментов, как диены и ендиены [5, 15], присутствующих в структуре важнейших классов природных соединений. Наиболее удобным методом получения таких соединений является присоединение галогенидов теллура (IV) к алкинам [1, 2, 3, 4, 7, 12], приводящим как к винилтеллуридам, так и дивинилтеллуридам. Реакции эти высоко стереоспецифичны и протекают исключительно через анти- или син-присоединение, в зависимости от использованного алкина [9]. В частности, этот метод успешно использован в получении биологически активных Te-содержащих соединений, являющихся эффективными ингибиторами катепсина B человека [10] либо демонстрирующими мощные антиоксидантные свойства [14].
В ходе изучения электрофильных реакций тетрахлорида теллура с пропаргилгалогенидами [1, 4] за счет регио- и стереоселективного присоединения тетрахлорида теллура к пропаргилбромиду и последующего восстановления образующегося теллурдихлорида метабисульфитом натрия нами получен Z,Z-бис(3-бром-2-хлорпроп-1-ен-1-ил)теллурид 1, в котором соседствуют два типа нуклеофугов – галоген (хлор) при двойной связи в хлорметилиденовой группе и галоген (бром) при sp3-гибридизованном атоме углерода в бромметиленовой группе. Присутствие в теллуриде 1 двух бромметиленовых групп указывает на возможность функционализации этих соединений как за счет замещения атомов брома в них двумя нуклеофилами, так и потенциально за счет гетероциклизации путем введения бинуклеофила, участвующего в реакции замещения по обоим атомам брома.
Особенности реакций Z,Z-бис(3-бром-2-хлорпроп-1-ен-1-ил)теллурида с сульфидом натрия и натриевыми солями этиленгликоля в этаноле и этиленгликоле и превращения продуктов замещения на этиленгликолат натрия
Мы нашли, что взаимодействие Z,Z-бис(3-бром-2-хлорпроп-1-ен-1-ил)теллурида 1 с сульфидом натрия (Na2S.9H2O) в EtOH, растворителе, успешно использованным при нуклеофильном замещения атомов брома в бромметильных группах E,E-бис(3-бром-1-хлорпроп-1-ен-2-ил)сульфида и селенида на сульфид и селенид натрия с образованием циклических продуктов – бис(хлорметилиденовых) производных 1,4-дитиана, 1,4-тиаселенана и 1,4-диселенана [11], не приводит к замещению атомов брома на сульфидную группу. В реакции превалировал побочный процесс этанолиза атомов брома за счет генерирования в реакционной смеси этилата натрия при действии на EtOH сульфида натрия. В результате единственным выделенным из смеси продуктом был Z,Z-бис(2-хлор-3-этоксипроп-1-ен-1-ил)теллурид 2. Теллурид 2 получен также встречным синтезом при обработке спиртового раствора теллурида 1 избытком Na2CO3 (схема 1). Образование теллурида 2 подтверждено данными ЯМР 1H, 13C, хроматомасс-спектрометрии. В масс-спектре, в частности, идентифицированы помимо молекулярного иона фрагментарные ионы [M–C2H5]+, [M–C2H5O]+, [M–C2H5O – HCl]+.
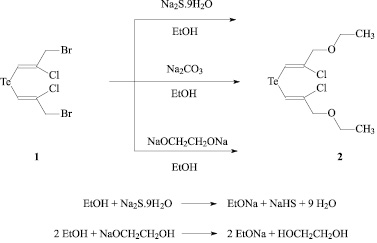
Схема 1
В продолжение исследований нуклеофильного замещения атома брома в бромметильных группах теллурида 1 изучено взаимодействие в этаноле этандиолата динатрия, полученного нейтрализацией 1 эквивалента этиленгликоля двумя эквивалентами NaOH и последующим выпариванием в вакууме образующейся воды. Но и в этом случае в результате реакции получен только Z,Z-бис(2-хлор-3-этоксипроп-1-ен-1-ил)теллурид 2, что прямо указывает на генерирование этилата натрия в этанольном растворе этандиолата динатрия за счет диспропорционирования соли до этандиолата натрия и EtONa (схема 1). Однако замена этанола на этиленгликоль в реакции теллурида 1 с этандиолатом натрия или этандиолатом динатрия, полученными растворением 1 или 2 эквивалентов NaOH соответственно, в 1 эквиваленте HOCH2CH2OH и последующим удалением образующейся воды в вакууме, позволила получить Z,Z-бис[2-хлор-3-(2-гидроксиэтокси)проп-1-ен-1-ил]теллурид 3 – продукт замещения атомов брома бромметильных групп на 2-гидроксиэтокси-группу (схема 2). Образование теллурида 3 подтверждено данными ЯМР 1H, 13C, хроматомасс-спектрометрии. В масс-спектре теллурида 3 зафиксированы помимо молекулярного фрагментарные ионы [M–CH2CH2OH]+, [M–OCH2CH2OH]+, [M–CH2CH2OH–OCH2CH2OH–Cl]+.
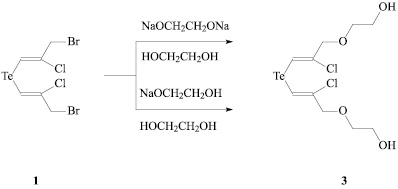
Схема 2
С целью получения производного теллурида 3, в котором гидроксильные группы замещены на атомы хлора, осуществлено его хлорирование тионилхлоридом. Найдено, что параллельно замещению OH-группы на хлор в ходе реакции происходит хлорирование теллура с образованием теллурдихлорида 4 (схема 3).
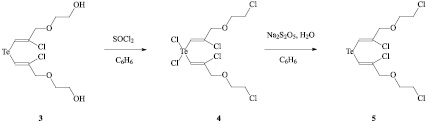
Схема 3
В спектрах ЯМР 1H и 13С на образование теллурдихлорида 4 указывает сильное смещение в слабое поле за счет влияния группы TeCl2 сигналов винильного протона (δ 7,92 м.д.) и дублетного сигнала углерода группы =CH (δ 122,33 м.д.) по сравнению с аналогичными сигналами в теллуриде 3 (δ 7,18 м.д. и 104,40 м.д.).
При восстановлении теллурдихлорида 4 под действием водного раствора Na2S2O5 в бензоле практически количественно получен Z,Z-бис[2-хлор-3-(2-хлорэтокси)проп-1-ен-1-ил]теллурид 5 (схема 3). Строение его подтверждено данными ЯМР 1H, 13C, хроматомасс-спектрометрии. В ИК-спектре теллурида 5 отсутствуют полосы поглощения OH группы. В масс-спектре зафиксированы помимо молекулярного иона фрагментарные ионы [M–OCH2CHCl]+, [M–OCH2CHCl–HCl]+, [TeCH=CClCH2OCH2CH2Cl]+, [CH=CClCH2OCH2CH2Cl]+, [CH2CH2Cl]+. В спектре ЯМР 1H найдены синглетные сигналы винильного и метиленовых протонов, величины которых очень близки сигналам соответствующих групп теллурида 3. Этокси-группы соединений 3, 4, 5 в спектрах ЯМР 1H проявляются в виде двух триплетных сигналов протонов в диапазоне 3,60–3,68 и 3,75–3,84 м.д. Идентичность слабопольных сигналов метиленовых протонов в теллуридах 3 и 5 (δ 3,75 м.д.) и заметное смещение в слабое поле при переходе к теллурдихлориду 4 (δ 3,84 м.д.) позволяет отнести их к группе =CCH2OCH2, так как она наиболее подвержена влиянию теллура при двойной связи. Близкие величины сильнопольных сигналов метиленовых протонов групп CH2X (X = OH, Cl) (3,60 м.д. – теллурид 3, 3,68 м.д. – теллурдихлорид 4, 3,65 м.д. – теллурид 5) согласуются с близкими величинами электроотрицательностей (по Полингу) O (3,44) и C (3,16). Соотнесение сигналов метиленовых углеродов в спектрах ЯМР 13С соединений 2–5 сделано на основании выделения сигнала углерода группы =C–CH2–O (δ 74,09 м.д.) в спектре Z,Z-бис(2-хлор-3-этоксипроп-1-ен-1-ил)теллурида 2 и сравнении спектров соединений 3–5. Слабопольные сигналы в диапазоне 70,62–71,82 м.д. соответствуют группе OCH2, в то время как сильнопольные сигналы при δ 42,74 и 42,95 м.д. указывают на CH2Cl, а при δ 61,82 м.д. – на CH2OH группу.
Экспериментальная часть
Спектры ЯМР 1H (400,13 МГц) и 13C (100,61 МГц) зарегистрированы на приборе Bruker DPX-400 в CDCl3, внутренний стандарт – ТМС. Масс-спектры получены на хромато-масс-спектрометре Agilent 5975 при энергии ионизирующих электронов 70 эВ. ИК-спектр соединения 5 получен на спектрометре IFS 25 Bruker в интервале 4000–400 см–1 в тонком слое. Основные результаты получены с использованием материально-технической базы Байкальского аналитического центра коллективного пользования СО РАН.
Z,Z-бис(3-бром-2-хлорпроп-1-ен-1-ил)теллурид (1) получен согласно методике [1] реакцией четыреххлористого теллура с пропаргилбромидом и восстановлением образующегося промежуточного продукта действием Na2S2O5.
Z,Z-Бис(2-хлор-3-этоксипроп-1-ен-1-ил)теллурид (2). В раствор 0,439 г (1 ммоль) теллурида 1 в 20 мл сухого этанола, дегазированного барботированием аргона, добавляли 0,330 г (3 ммоль) Na2CO3, полученную реакционную смесь перемешивали в атмосфере аргона на водяной бане (60 °С) 4 ч и при комнатной температуре 16 ч. Выпавший осадок отфильтровывали, фильтрат выпаривали, экстрагировали хлороформом. Растворитель удаляли в вакууме. Выход 0,138 г (38 %), темно-коричневое маслообразное вещество. Спектр ЯМР 1Н,δ, м.д.: 1,23 т (6 H, 2 СH3, 3J 7,0 Гц); 3,53 к (4 H, 2 OСH2, 3J 7,0 Гц); 4,12 д (4 H, OCH2–C=, 4J 1,1 Гц); 7,06 т (2 H, 2 =CHCl, 4J 1,1 Гц). Спектр ЯМР 13C, δ, м.д.: 14,98 к (CH3, 1JCH 126,2 Гц); 65,89 т.к (OCH2CH3, 1JCH 141,3, 2JCH 4,3 Гц); 74,09 т (OCH2-C=, 1JCH 145,2 Гц); 103,43 д (=CHTe, 1JCH 171,0 Гц); 137,27–137,40 м (=C). Масс-спектр, m/z (Iотн., %) (35Cl, 130Te): [M]+ 368 (36); 339 (1) [M–C2H5]+, 323 (2) [M–C2H5O]+, 287 (1) [M–C2H5O–HCl]+, 249 (3); 220 (7); 204 (7); 185 (6); 165 (14); 129 (27); 101 (27); 91 (100); 55 (33). Найдено, %: C 33,13; H 4,01; Cl 19,39; Te 34,48, C10H16O2TeCl2, Вычислено, %: C 32,75; H 4,40; Cl 19,33; Te 34,79, M 366,74.
Z,Z-Бис[3-(2-гидроксиэтокси)-2-хлорпроп-1-ен-1-ил]теллурид (3). К раствору 0,229 г (0,52 ммоль) теллурида 1 в 6 мл этиленгликоля добавляли 87 мг (1,04 ммоль) этандиолата натрия, полученного растворением 1 эквивалента NaOH в 1 эквиваленте этиленгликоля, перемешивали в атмосфере аргона при комнатной температуре 6 ч. Реакционную смесь растворяли в 50 мл воды, экстрагировали хлороформом, экстракт сушили MgSO4, Растворители удаляли в вакууме. Выход 0,128 г (62 %); коричневое маслообразное вещество. Спектр ЯМР 1H, δ, м.д.: 3,02 с (2 H, 2 OH); 3,60 т (4 H, 2 OCH2OH, 3J Hz); 3,75 т (4 H, 2 OCH2O, 3J Hz); 4,18 с (4 H, 2 CH2–C=); 7,18 с (2 H, 2 =CHCl). Спектр ЯМР 13C, δ, м.д.: 61,82 т (CH2OH, 1J 123,5 Гц); 71,82 т (OCH2, 1J 143,4 Гц); 74,70 т (OCH2–C=, 1J 147,6 Гц); 104,40 д (=CHTe, 1J 170,6 Гц); 136,93–137,08 м (=C). Масс-спектр, m/z (Iотн, %) (35Cl, 130Te): [M]+400 (4); 355 (1) [M–CH2CH2OH]+, 339 (1) [M–OCH2CH2OH]+, 277 (1) [M–2OCH2CH2OH–H]+, 259 (1); 239 (1); 220 (2); 207 (3); 173 (2); 165 (3); 146 (2); 135 (4); 129 (7); 113 (4); 101 (6); 91 (20); 77 (10); 65 (9); 45 (100) [CH2CH2OH]+, 39 (30) [C3H6]+. Найдено, %: C 30,59; H 4,16; Cl 17,70; Te 32,48, C10H16O4Cl2Te. Вычислено, %: C 30,12; H 4,04; Cl 17,78; Te 32,00, M 398,74.
Z,Z-Бис[2-хлор-3-(2-хлорэтокси)проп-1-ен-1-ил]теллурдихлорид (4). К раствору 0,128 г (0,32 ммоль) Z,Z-бис[3-(2-гидроксиэтокси)-2-хлорпропенил-1]теллурида 3 в 4 мл бензола добавляли за 2 ч в атмосфере аргона 0,680 г (5,7 ммоль) тионилхлорида в 2 мл бензола, перемешивали при комнатной температуре 2 ч. Реакционную смесь обработали водой, экстрагировали хлороформом, сушили MgSO4. Растворитель удаляли в вакууме. Выход 0,098 г (60 %); коричневое маслообразное вещество. Спектр ЯМР 1H, δ, м.д.: 3,68 т (4 H, 2 CH2Cl, 3J 5,5 Гц); 3,84 т (4 H, 2 CH2O, 3J 5,5 Гц); 4,35 д (4 H, 2 CH2, 4J 1 Гц); 7,92 т (2 H, 2 =CHCl, 4J 1 Гц). Спектр ЯМР 13C, δ, м.д.: 42,74 т (CH2Cl, 1J 148,5 Гц); 71,65 т (CH2O, 1J 144,7 Гц); 72,93 т (OCH2–C=, 1J 148,0 Гц); 122,33 д (=CHTe, 1J 189,8 Гц); 145,37 к (=C, 1J 5,5 Гц). Найдено, %: C 27,69; H 3,36; Cl 32,77; Te 29,48, C10H14O2Cl4Te. Вычислено, %: C 27,51; H 3,24; Cl 32,55; Te 29,29.
Z,Z-Бис[2-хлор-3-(2-хлорэтокси)проп-1-ен-1-ил]теллурид (5). К раствору 0,098 г (0,19 ммоль) теллурдихлорида 4 в 5 мл бензола добавляли в течение 1 ч раствор 0,489 г (2,2 ммоль) Na2S2O5 в 2 мл H2O, перемешивали при комнатной температуре 15 ч. Органический слой отделяли, сушили MgSO4. Растворитель удаляли в вакууме. Выход 0,079 г (95 %); светло-коричневое маслообразное вещество. ИК-спектр, cm–1: 3029, 2955 c, 2922 c, 2852 c, 1736, 1604, 1462 c, 1377, 1356, 1299, 1276, 1252, 1171, 1117 c, 1046, Спектр ЯМР 1H, δ, м.д.: 3,65 т (4 H, 2 CH2Cl, 3J 5,5 Гц); 3,75 т (4 H, 2 CH2O3J 5,5 Гц); 4,20 с (4 H, 2 CH2–C=); 7,15 с (2 H, 2 =CHCl). Спектр ЯМР 13C, δ, м.д.: 42,95 т (CH2Cl, 1J 150,2 Гц,); 70,62 т (CH2O, 1J 142,8 Гц,); 74,82 т (OCH2–C=, 1J 148,0 Гц); 104,52 д (=CHTe, 1J 167,7 Гц); 136,80 с (=C). Масс-спектр, m/z (Iотн, %) (35Cl, 130Te): [M]+ 436 (2); 357 (1) [M–OCH2CHCl]+, 321 (1) [M–OCH2CHCl–HCl]+, 283 (1) [TeCH=CClCH2OCH2CH2Cl]+, 217 (1); 191 (3) [HTeCH=CCl]+, 165 (3); 153 (7) [CH=CClCH2OCH2CH2Cl]+, 101 (10); 93 (12) [CH2OCH2CH2Cl]+, 63 (100) [CH2CH2Cl]+. Найдено %: С 32,73; H 3,66; Cl 19,81; Te 34,50, C10H14O2Cl2Te. Вычислено %: C 32,93; H 3,87; Cl 19,44; Te 34,98, M 364,72.
Взаимодействие Z,Z-бис(3-бром-2-хлорпроп-1-ен-1-ил)теллурида 1 с сульфидом натрия в этаноле. К раствору 0,311 г (0,71 ммоль) теллурида 1 в 15 мл этанола медленно добавляли раствор 0,170 г (0,72 ммоль) Na2S.9H2O в 10 мл EtOH, перемешивали 7 ч при 50 °C. Полученную реакционную смесь разбавляли водой, экстрагировали хлороформом, хлороформные вытяжки сушили MgSO4, Растворитель удаляли в вакууме. Получили 0,105 г (40 %) бис(3-этокси-2-хлорпроп-1-ен-1-ил)теллурида 2, ЯМР 1H и 13С спектры соответствуют спектрам теллурида 2.
Взаимодействие Z,Z-бис(3-бром-2-хлорпроп-1-ен-1-ил)теллурида 1 с этандиолатом динатрия в этаноле. К раствору 0,220 г (0,5 ммоль) теллурида 1 в 10 мл сухого этанола добавили 0,106 г (1 ммоль) NaO(CH2)2ONa, перемешивали 4 ч в атмосфере аргона при 60оС. Выпавший осадок NaBr отфильтровывали, фильтрат растворяли в 10 мл хлороформа, промывали водой, сушили K2CO3. Растворители удаляли в вакууме. Получили 0,145 г (79 %) бис(3-этокси-2-хлорпроп-1-ен-1-ил)теллурида 2, ЯМР 1H и 13С спектры соответствуют спектрам теллурида 2.
Заключение
Приведенные в работе экспериментальные данные показывают, что взаимодействие Z,Z-бис(3-бром-2-хлорпроп-1 -ен-1-ил)теллурида с такими нуклеофилами, как сульфид натрия и натриевые соли этиленгликоля, в этаноле приводит к образованию продуктов замещения атомов брома бромметильных групп теллурида на этокси-группы за счет генерирования в реакционных смесях более нуклеофильного этилата натрия. Замещение атомов брома в бромметильных группах теллурида на этиленгликолат натрия удается осуществить при использовании в качестве растворителя этиленгликоля. Полученный в результате реакции Z,Z-бис[2-хлор-3-(2-гидроксиэтокси)проп-1-ен-1-ил]теллурид при хлорировании под действием тионилхлорида приводит к продукту замещения обеих гидроксильных групп на атомы хлора и одновременно хлорирования теллура. Последующее восстановление теллурдихлорида действием водного Na2S2O5 приводит к Z,Z-бис[2-хлор-3-(2-хлорэтокси)проп-1-ен-1-ил]теллуриду, перспективному теллурсодержащему реагенту для построения на его основе новых ациклических и циклических теллурсодержащих соединений.
Работа выполнена при финансовой поддержке Российского фонда фундаментальных исследований (проект № 14-03-00185).
Библиографическая ссылка
Мартынов А.В., Махаева Н.А., Амосова С.В. ФУНКЦИОНАЛИЗАЦИЯ Z,Z-БИС(3-БРОМ-2-ХЛОРПРОП-1-ЕН-1-ИЛ)ТЕЛЛУРИДА ЗА СЧЕТ РЕАКЦИЙ С КИСЛОРОДСОДЕРЖАЩИМИ НУКЛЕОФИЛАМИ // Успехи современного естествознания. 2016. № 12-2. С. 269-274;URL: https://natural-sciences.ru/ru/article/view?id=36298 (дата обращения: 03.06.2026).



