В настоящее время для изучения сорбционно доступной поверхности углеродных материалов применяются адсорбционные, химические и различные физические методы исследования [1, 3, 9]. Однако химические методы ограничиваются кислотно-основным титрованием, не дающим информации об окислительно-восстановительных свойствах поверхности.
В данной работе применен электрохимический метод исследования окислительно-восстановительных свойств поверхности углеродной ткани, показана корреляция зависимости стационарного потенциала от температуры термообработки (ТТО) углеродных тканей с адсорбционной емкостью адсорбентов, получаемых активацией этих тканей.
Для активирования были подготовлены образцы ткани из волокон на основе гидратцеллюлозы (шелковой ткани «Светлогорское волокно»), которые подвергались термической обработке. По структуре элементарного волокна этот материал однороден. Характеристики данного материала представлены в табл. 1.
Таблица 1
Технические характеристики нетермообработанной шелковой ткани (Светлогорское волокно)
|
Показатель |
Единицы измерения |
Значение |
|
Линейная плотность |
текс. |
192 |
|
Поверхностная плотность |
г/м2 |
360 ± 30 |
|
Число нитей на 10 см основы утка |
103 ± 5 80 ± 5 |
|
|
Разрывная нагрузка полоски ткани 5/20 см основы утка |
МПа |
2744 (2800) 2058 (2100) |
|
Переплетение ткани |
cаржа 2/2 |
|
|
Ширина ткани с кромками |
см |
102 ± 3 |
Термическая обработка частично карботизованной промышленно произведенной ткани (при 540 К) проводилась автором в динамических условиях на промышленном агрегате графитации до конечной ТТО 1020–2270 К. То есть лента ткани транспортировалась через камеру нагрева, заполненную инертным газом (расход азота 70– 80 л/час) со скоростью 2 м/час. Общее время пребывания ткани в камере нагрева составило 18 мин, что определялось техническими возможностями установки. При таком нагреве реакции, характерные для разных стадий карбонизации, протекают одновременно и не всегда успевают завершиться за время термообработки. После высокотемпературной обработки ткань подвергалась окислению путем активирования водяным паром в потоке азота (концентрация водяного пара составляла 65 об. %).
При взаимодействии водяного пара с углеродом поглощается тепло, скорость процесса газификации (окисления) углерода умеренная, нет локальных перегревов, продукт однородный по качеству [2].
Более низкая стоимость и доступность водяного пара как активирующего агента, а также более слабый эндоэффект реакции взаимодействия воды с углеродом делают этот реагент предпочтительнее в производстве активированных углеродных тканей по сравнению с углекислым газом [2, 6]. Водяной пар перегревался до температуры активации 1020 К. В результате окисления части углерода сформировалась развитая пористая система углеродных материалов. Масса исходного образца углеродной ткани составляла 0,9 г.
Интегральной характеристикой образцов активированной углеродной ткани служит доля потери массы (обгар) Δm, который можно рассчитать следующим образом:
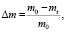 (1)
(1)
где m0, mt – масса ткани в моменты времени t = 0 и t, соответственно.
Опытным путем был подобран расход перегретого водяного пара, и он составил 0,3 л/мин.
Для стандартизации экспериментов и возможности сопоставления свойств адсорбентов, полученных при разных условиях, активирование проводилось до получения обгара 30 %. Этого вполне достаточно для образования развитой пористости и сохранения приемлемых механических характеристик, в частности, прочности на разрыв [5, 7]. Прочность на разрыв при активации снижается, однако, во всех случаях прочность полученных активированных углеродных тканей составляет 400–500 МПа, что вполне приемлемо для работы, как фильтр материала в процессе доочистки воздуха.
Углеродные волокнистые адсорбенты, полученные из рассматриваемых образцов углеродных тканей, исследовались адсорбционными методами. Для получения их характеристик снималась изотерма адсорбции азота объемным методом [4, 8].
Поверхность полученных образцов углеродной ткани при разной ТТО исследовалась химическим и электрохимическим методами.
В табл. 2 приведены данные анализа кислородсодержащих функциональных групп на поверхности углеродной ткани с различной ТТО. Определение количества функциональных групп на поверхности материала проводилось химическим методом кислотно-основного титрования (ГОСТ 8930-79). Из табл. 2 видно, что с увеличением ТТО количество всех кислородсодержащих групп падает. Можно обратить внимание на преобладание хинонных групп на поверхности.
Таблица 2
Количество поверхностных функциональных групп на углеродной ткани с различной ТТО
|
ТТО, К |
Функциональные группы, ммоль/г |
||
|
|
|
|
|
|
1770 |
0,02 |
0,15 |
0,28 |
|
2270 |
0,01 |
0,02 |
0,11 |
Если рассматривать функциональные группы как активные центры, способные к легкому окислению и образованию зародышей микропор при активации углеродных тканей, то можно ожидать, что с увеличением ТТО поверхность становится менее реакционно способной к окислению. Можно также ожидать, что ткань с ТТО 1770 К будет активироваться легче, поскольку имеет гораздо большее количество фенольных групп, способных легко окисляться.
Однако химический метод не дает прямой информации об окислительно-восстановительной способности поверхности углеродного материала. Информация об окислительно-восстановительной способности поверхности углеродного материала важна для понимания процесса активации углеродных материалов. В настоящей работе для анализа окислительно-восстановительных свойств поверхности используются потенциодинамические кривые углеродных тканей. Потенциодинамические кривые снимались с помощью потенциометра. Электродом сравнения служил хлорсеребряный полуэлемент. Все потенциалы в работе приведены относительно нормального водородного электрода. Скорость изменения потенциала задавалась 1 мВ/с. Исследуемый образец представлял собой кусок углеродной ткани размером 10 мм*10 мм, закрепленный на металлическом токопроводе. От контакта с раствором токопровод изолировался заливкой его парафином. Поскольку удельные поверхности всех исследуемых образцов близки, можно сравнивать токи, идущие в цепи, не приводя их к единице поверхности. В этом случае вносимая ошибка измерения плотности тока не превышает 20 %, в то время как токи отличаются на порядки.
На рисунке представлены две потенциодинамические кривые, полученные на образцах углеродной ткани (размером 10 мм*10 мм) в 0,5N растворе NaOH, и для сравнения аналогичная кривая на графите.
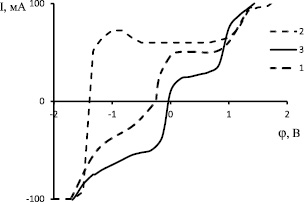
Потенциодинамические кривые, полученные на образцах углеродной ткани с ТТО, равной 2270 К (1), 1770 К (2) и графита (3)
Углеродная ткань, обработанная при 2270 К (кривая 1), имеет более регулярную структуру по сравнению с углеродной тканью, обработанной при 1770 К (кривая 2), и имеет гораздо меньше центров, способных легко окисляться. Об этом свидетельствует тот факт, что стационарный потенциал (φ) этой ткани наиболее близок к потенциалу для графита (кривая 3). Для образца с ТТО 1770 К стационарный потенциал располагается левее почти на 1 В. Это свидетельствует об ускорении анодных процессов, протекающих на этом образце, то есть о способности его поверхности к более легкому окислению. Такая способность может быть обусловлена наличием центров, способных легко окисляться. Это могут быть дефекты поверхности, какие-либо функциональные группы. При потенциалах выше 1 В и ниже – 1,2 В все потенциодинамические кривые практически не имеют различий. В области ниже – 1,2 В идет активное выделение водорода, все образцы работают как инертные электроды. При потенциалах выше 1 В на образце выделяется кислород, и ткань окисляется практически полностью.
Можно ожидать, что при активировании центры, способные к окислению, будут окисляться первыми, образуя поры, и количество пор будет тем больше, чем больше таких центров имеется на поверхности. Исходя из сравнения потенциодинамических кривых, поверхность адсорбента, полученного из углеродной ткани, обработанной при 2270 К, должна быть наименее развитой, поскольку поверхность, имеющая незначительное количество активных центров, при активировании должна окисляться равномерно по всей площади, практически не образуя поры. В то же время наиболее развитая поверхность ожидается у адсорбента, полученного из образца ткани с ТТО 1770 К. Сравнение адсорбционной емкости адсорбентов, полученных из этих образцов углеродной ткани активацией водяным паром при 1200 К и 30 %-м обгаре, дает поверхность по БЭТ 390 (образец 1) и 620 (образец 2) м2/г, что подтверждает вышесказанное предположение.
Данная активированная углеродная ткань на основе гидратцеллюлозы предназначена для доочистки воздуха (газовой фазы) от паров органических веществ: ацетона, изобутилового спирта (ИБС), диметилацетамида (ДМАА). Адсорбционная способность прямо связана не только со структурой адсорбента, но и зависит от свойств адсорбата, его концентрации и параметров проводимого процесса адсорбции. В табл. 3 представлены данные по динамической и предельной емкости полученного адсорбента с поверхностью по БЭТ 620 м2/г, условно называемого АУТ-1. Для сравнения в табл. 3 приведены данные для промышленного активного угля типа АР-В. Предельные емкости определялись эксикаторным методом, а динамические – на полупромышленной установке. Сущность эксикаторного метода состоит в насыщении помещенной в бюкс навески отрегенерированного адсорбента парами органических веществ (ацетона, ИБС и ДМАА), концентрация которых составляла ≈ 1.
Таблица 3
Адсорбция паров органических растворителей
|
Органический растворитель |
Абсолютная концентрация, г/м3 |
Относительная концентрация, С/СS |
Образец |
Статическая емкость, г/г |
Динамическая емкость, г/г |
|
Ацетон |
0,4 |
0,5•10–3 |
АУТ-1 АР-В |
0,36 0,40 |
0,17 0,05 |
|
ИБС |
0,6 |
1,4•10–3 |
АУТ-1 АР-В |
0,40 0,45 |
0,18 0,05 |
|
ДМАА |
0,05 |
2,6•10–3 |
АУТ-1 АР-В |
0,38 0,40 |
0,14 0,05 |
Величина предельной сорбционной емкости (Б) определялась по разности веса бюкса с адсорбентом после насыщения и после регенерации, в соответствии с формулой
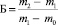 г/г, (2)
г/г, (2)
где m0 – вес высушенного бюкса (г);
m1 – вес бюкса с навеской адсорбента, доведенной до постоянного веса (г);
m2 – вес бюкса с навеской после насыщения (г).
Из табл. 3 видно, что при столь низких относительных концентрациях применение активированной ткани АУТ-1 гораздо эффективнее, чем активного угля. Несмотря на то, что предельная емкость промышленного угля несколько выше, чем у активированной ткани, в динамических условиях благодаря высоким кинетическим параметрам адсорбции, а также свойствам структуры ткань адсорбирует в два-три раза больше, чем активный уголь.
Выводы
Таким образом, в данной работе установлена корреляция окислительно-восстановительных свойств поверхности углеродных тканей, полученных при разных ТТО с адсорбционной емкостью, полученных из них углеволокнистых адсорбентов. Полученная активированная углеродная ткань работает гораздо эффективнее, чем активный уголь в процессе доочистки воздуха от паров органических веществ.
Библиографическая ссылка
Ляшенко С.Е. ОЦЕНКА ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫХ СВОЙСТВ ПОВЕРХНОСТИ УГЛЕРОДНЫХ ТКАНЕЙ ИЗ ГИДРАТЦЕЛЛЮЛОЗНОГО ВОЛОКНА // Успехи современного естествознания. 2017. № 1. С. 13-17;URL: https://natural-sciences.ru/ru/article/view?id=36334 (дата обращения: 14.05.2026).