Интерес к титану и сплавам на его основе объясняется их хорошими конструктивными свойствами, высоким отношением прочности к плотности, большой коррозионной стойкостью, высокой температурой плавления. Все это определило применение титана в самых различных областях: авиации, ракетостроении, машиностроении, судостроении, химическом машиностроении, медицине и т.п.
Изготовлению изделий из титана, особенно нанесению на его поверхность модифицирующих покрытий, препятствует прочная оксидная пленка. Удаление этой пленки производится различными методами [1–3]. Большое распространение получила обработка поверхности титана кислотами [4]. Одним из перспективных растворов для травления титана является смесь плавиковой и соляной кислот. В результате травления титана этим раствором образуется отработанный кислый травильный раствор (ОКТР), содержащий в своем составе фторид титана, плавиковую и соляную кислоты. Этот раствор является достаточно токсичным и перед сбросом должен подвергаться или многократному разбавлению или переработке. Существующие методы переработки ОКТР приводят к получению осадков гидроокиси титана и веществ, содержащих фториды. В результате возникает проблема утилизации этих осадков [5–7].
Цель работы
В статье представлены результаты исследований по переработке ОКТР с получением гидроксида титана и смеси кислот, пригодных для приготовления травильного раствора, используемого в производстве изделий из титана.
Материалы и методы исследования
Исследовалась переработка ОКТР, полученного в процессе травления титана смесью плавиковой и соляной кислот. ОКТР содержал 21,9 г/л фторида титана, 1,7 г/л плавиковой кислоты и 6,2 г/л соляной кислоты.
Процесс переработки состоял из ряда операций. Вначале ОКТР нейтрализовался NaOH и после выпадения осадка Ti(OH)4 фильтровался. Осадок Ti(OH)4 сушили и прокаливали. Фильтрат, содержащий NaF и NaCl, подвергался электрохимической переработке в мембранном электролизере, схема которого приведена на рис. 1.
Электролизер состоял из четырех камер – катодной 1, анодной 4 и двух средних 2, 3. Для разделения камер применяли катионообменную К и анионообменную А мембраны марки МК-40 и МА-40 соответственно. Электродные камеры выполнены в виде углублений размером 5 мм в плитах из оргстекла. Средние камеры изготовлены в виде рамок из поливинилхлоридной пластины толщиной 2 мм. В качестве электродов использовали пластинки из титана, покрытые окисью рутения. Вся конструкция шпильками стягивалась в единый пакет. Для предотвращения контакта между ионообменными мембранами в камеры помещали сетку просечную растянутую из каландрированного винипласта. Рабочая поверхность каждой ионообменной мембраны составляла величину 30 см2.
Через среднюю камеру 2 электролизера прокачивали исследуемый раствор, содержащий фторид и хлорид натрия. Под действием электрического тока ионы натрия переносились в катодную камеру 1 аппарата. В этой камере на катоде происходило разложение воды с выделением водорода и образованием ионов гидроксила. В результате в катодной камере концентрировался раствор щелочи. Катодная камера была непроточной, и щелочь, накапливающаяся в ней, самотеком покидала камеру и собиралась в емкости 10.
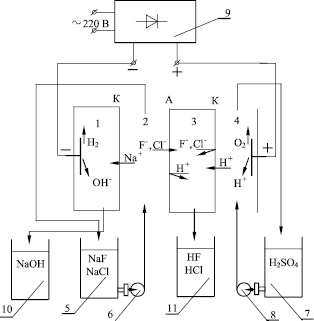
Рис. 1. Схема экспериментальной установки: 1, 2, 3, 4 – камеры электролизера; 5 – емкость с фильтратом; 6, 8 – насосы; 7 – емкость с серной кислотой; 9 – источник постоянного тока; 10 – емкость со щелочью; 11 – емкость с плавиковой и соляной кислотами
Ионы фтора и хлора мигрировали через анионообменную мембрану в камеру 3 аппарата. Дальнейшему продвижению их к аноду препятствовала катионообменная мембрана. Через анодную камеру 4 прокачивали 0,1 н раствор серной кислоты. При этом на аноде разлагалась вода с выделением кислорода и образованием ионов водорода, которые, переносились в камеру 3 электролизера. В этой камере происходило концентрирование плавиковой и соляной кислот, самотеком вытекающих из аппарата по мере их накопления и собирающихся в емкости 5. Для обеспечения необходимой электропроводности электролизера в начальные моменты времени в катодную 1 заливали 0,1 н раствор гидроксида натрия, а в 3 камеру электролизера заливали 0,1 н раствор соляной кислоты. Для питания электролизера использовали регулируемый выпрямитель, позволяющий обеспечивать необходимую токовую нагрузку.
Через каждые 30 мин растворы, собирающиеся в емкостях 10 и 11, анализировались на содержание щелочи, а так же соляной и плавиковой кислот.
Результаты исследования и их обсуждение
В процессе растворения титана в смеси плавиковой и соляной кислот образуется раствор фиолетового цвета. Это указывает на то, что в процессе растворения образуется фторид трехвалентного титана, который окисляется кислородом воздуха до четырехвалентного. Однако этот процесс протекает в течение суток. Для исследования процесса извлечения титана из ОКТР его свежеприготовленный обработкой щелочью к ряду проб, содержащих по 50 мл ОКТР, добавляли различное количество гидроксида натрия. После образования осадка гидроксида титана его отфильтровывали, сушили и прокаливали при температуре 900 °С в течение 1 часа. При этом гидроксид титана переходил в двуокись. Максимальное количество двуокиси титана, которое при этом может быть получено равно 0,835 г. В фильтрате определяли величину рН. Зависимость степени извлечения титана из ОКТР его обработкой щелочью от рН фильтрата представлена в таблице.
Оценка погрешности полученных результатов при осаждении и прокалке с использованием распределения Стьюдента [8] по последним шести результатам показала, что при доверительной вероятности 95 % относительная погрешность не превышает 1 %.
Увеличение рН фильтрата после выделения гидроксида титана до значения, равного 7.6 приводит к росту степени извлечения титана из ОКТР. При рН фильтрата более чем 7,6 степень извлечения титана из ОКТР достигает величины 100 %. Оптимальное значение рН фильтрата после обработки ОКТР гидроксидом натрия находится в пределах 7,6–7,8.
Процесс электрохимической переработки фильтрата, полученного из ОКТР после его обработки щелочью исследовали при мембранных плотностях тока 200 А/м2, 400 А/м2, 600 А/м2 и 800 А/м2, что соответствовало токовой нагрузке на электролизере 0,6 А, 1,2 А, 1,8 А и 2,4 А. Процесс электрохимической обработки вели до тех пор, пока концентрация растворов гидроксида натрия и смеси соляной и плавиковой кислот не перестанет расти. Таким образом, получали максимальную концентрацию продуктов электрохимической переработки фильтрата.
На рис. 2 представлена зависимость концентрации гидроксида натрия от времени электрохимической обработки фильтрата при различной токовой нагрузке на электролизере.
Оценка относительной погрешности результатов полученных при электрохимической обработке ОКТР по описанной ранее методике при доверительной вероятности 95 % не превышает 6,3 %
Скорость образования гидроксида натрия возрастает с увеличением плотности тока. Так при плотности тока 200 А/м2 скорость концентрирования щелочи равна 26,1 г/л·ч, а при плотности тока 800 А/м2 – 179,2 г/л·ч. Максимальная концентрация гидроокиси натрия в катодной камере достигнута при плотности тока 800 А/м2 через 5 часов и составила 374 г/л.
Зависимость степени извлечения титана из ОКТР от рН фильтрата
|
рН |
3,75 |
5,5 |
6,45 |
7,2 |
7,6 |
7,8 |
9,4 |
9,85 |
10,6 |
12,8 |
|
Масса TiO2, г |
0,724 |
0,765 |
0,799 |
0,815 |
0,830 |
0,835 |
0,836 |
0,835 |
0,834 |
0,837 |
|
Степень извлечения, % |
86,7 |
91,6 |
95,7 |
97,6 |
99,4 |
100 |
100 |
100 |
99,9 |
100 |
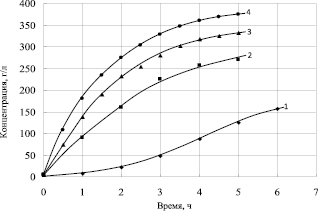
Рис. 2. Зависимость концентрации NaOH от времени, плотность тока, А/м2: 1 – 200; 2 – 400; 3 – 600; 4 – 800
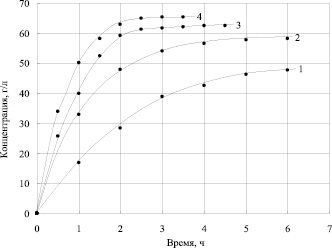
Рис. 3. Зависимость концентрации HF от времени, плотность тока, А/м2: 1 – 200; 2 – 400; 3 – 600; 4 – 800
На рис. 3 приведена зависимость концентрации плавиковой кислоты в камере концентрирования кислот от времени электрохимической обработки фильтрата при различной токовой нагрузке на электролизере. Скорость концентрирования плавиковой кислоты увеличивается с повышением токовой нагрузки на электролизере. При плотности тока 200 А/м2 скорость образования плавиковой кислоты равна 16,8 г/л·ч, а при плотности тока 800 А/м2 – 33,1 г/л·ч. Максимальная концентрация плавиковой кислоты наблюдается при плотности тока 800 А/м2 и составляет величину 65,2 г/л.
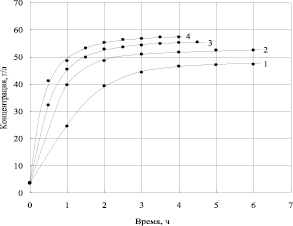
Рис. 4. Зависимость концентрации HCl от времени, плотность тока А/м2: 1 – 200; 2 – 400; 3 – 600; 4 – 800
На рис. 4 представлена зависимость концентрации соляной кислоты в камере концентрирования кислот от времени электрохимической обработки фильтрата при различной токовой нагрузке на электролизере.
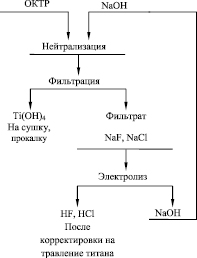
Рис. 5. Технологическая схема переработки ОКТР
Характер изменения концентрации соляной кислоты от времени обработки аналогичен рассмотренным ранее. Скорость концентрирования соляной кислоты выше, чем плавиковой кислоты. При плотности тока 200 А/м2 она равна 24,5 г/л·ч, а при плотности тока 800 А/м2 – 40,9 г/л.·Максимальная концентрация соляной кислоты наблюдается при плотности тока 800 А/м2 и составляет величину 51,1 г/дм3.
На основании результатов, полученных при исследовании процесса переработки ОКТР, предлагается технологическая схема, представленная на рис. 5. ОКТР обрабатывается гидроксидом натрия до рН 7,6–7,8. Осадок гидроксида титана отфильтровывается, сушится и прокаливается. Получающаяся при этом двуокись титана может использоваться в лакокрасочной промышленности. Фильтрат, содержащий фториды и хлориды натрия, перерабатывается в мембранном электролизере. В результате получается гидроксид натрия с концентрацией до 374 г/л и смесь соляной и плавиковой кислот с концентрацией около 51,1 г/л и 65,2 г/л соответственно. Гидроксид натрия может использоваться в процессе нейтрализации ОКТР, а смесь плавиковой и соляной кислот – в процессе травления поверхности титана.
Библиографическая ссылка
Быковский Н.А., Даминев Р.Р., Забиров Т.З., Пучкова Л.Н., Фанакова Н.Н. ПЕРЕРАБОТКА ОТРАБОТАННЫХ ТРАВИЛЬНЫХ РАСТВОРОВ, СОДЕРЖАЩИХ ФТОРИД ТИТАНА, ПЛАВИКОВУЮ И СОЛЯНУЮ КИСЛОТЫ // Успехи современного естествознания. 2017. № 6. С. 7-12;URL: https://natural-sciences.ru/ru/article/view?id=36490 (дата обращения: 17.05.2026).



