Создание электроно- и ионопроводящих сорбционно-активных каталитически активных материалов, которые могут быть использованы как электрохимические мостики в водородпроизводящих матрицах, является актуальной проблемой. В настоящее время известны Н(+) и ОН(-) проводящие полимерные мембраны и ткани, а также электропроводные сорбенты. В работе [1] описывается материал, обладающий протонпроводящими свойствами. Однако такой материал не обладает сорбционными свойствами. Подобный материал описывается и в статье [2], также раскрываются возможности его применения. В [3] производится обработка тканей и придание им свойств ионообменных материалов. Материалы, описанные в статье [4] обладают также свойствами сорбентов, что повышает возможности их применения. В целом такие материалы имеют большой потенциал для использования. Например, в [5] описывается применение полимерного ионпроводящего материала для создания высококачественных гальванических элементов.
Однако ни один из вышеописанных материалов не является одновременно и проводником, и сорбентом, и люминофором. А кроме того сложно создать такой материал, который также будет проводить ионы Н(+) и ОН(-).
В [6, 7] было описано образование комплексов Ni (2+) и Co (2+) с этаноламиновыми производными ПВХ и восстановление ионов до Ni (0) или Co (0) в полостях аминных циклов. В неполяризованных мостиках из материалов из хлопковой марли со слоем из активного угля и этаноламиновых производных ПВХ (далее ЦЭ) с H2SO4 и NaOH, находящихся в газовой или в жидкой средах между растворами H2SO4 или NaOH, движение H+ и OH- происходит по эстафетному механизму через систему водородных связей. В катодно- или анодно-поляризованных мостиках в зоне прививки на микрочастицах угля происходит разложение аквакомплексов с образованием H2 или O2. При этом в регенерации комплексов участвуют H+ или OH-, движущиеся в слое из раствора с анодом или с катодом [6]. Представляло интерес синтезировать материалы, аналогичные ЦЭК и ЦЭГ, не только с соединениями H2SO4 или NaOH, но и с комплексами Ni (0) или Co (0) (далее ЦЭКН, ЦЭКК, ЦЭГН и ЦЭГК соответственно). Можно ожидать, что центральные атомы, дислоцированные в стенках всех указанных пор вместе с углем, будут формировать каналы электронной проводимости. В порах содержание H2SO4 или NaOH может быть больше, чем в ЦЭК и ЦЭГ, за счет координации SO42- или OH. Весьма вероятно, что скорость движения ионов и скорости образования H2 или O2 в мостиках из ЦЭКН, ЦЭКК, ЦЭГН и ЦЭГК будет больше, чем в мостиках из ЦЭК и ЦЭГ.
Цель исследования: на основе хлопковой марли синтезировать ЦЭКН, ЦЭКК, ЦЭГН и ЦЭГК, измерить их электрическое сопротивление и сорбционную емкость при поглощении паров бензола или гексана, а также исследовать их как мостики в электрохимических матрицах.
В литературе интересующие нас данные не описаны.
Материалы и методы исследования
Исходные материалы и реактивы: материал из хлопковой марли со слоем из активного угля и этаноламиновых производных ПВХ (ЦЭ), растворы 0,5 моль/л гексааммиакатов Ni (2+) или Co (2+), содержащие 0,75 моль/л (NH4)2SO4 и 0,8 моль/л NH3, раствор 1 моль/л NaBH4, содержащий 3 моль/л NaOH, кислота серная, гидроокись натрия (квалификация «хч», «чда» или «ч»). ЦЭ был синтезирован по методике [7]. Состав: марля – 86,11 %, в слое производных ПВХ – 49,73 %, угля – 50,27 %, содержание этаноламиновых групп 0,86 ммоль/г.
Измерения сопротивления слоя в отрезках материала длиной 5 см проводили с помощью мультиметра MS8233E.
Измерение сорбционной емкости слоя при поглощении паров бензола и гексана проводили весовым методом [7].
Исследование тканей как мостиков в электрохимических матрицах проводили согласно [6]. При определенном напряжении (Е) измеряли ток (I) с точностью до 0,1 мА в цепи с неполяризованным мостиком из материалов между двумя сосудами с 3 моль/л растворами H2SO4 или с 3 моль/л растворами NaOH с платиновыми электродами в каждом, находящимися на расстоянии 5 см. Затем к участку ткани, находящемуся на воздухе, присоединяли проводник от клеммы (–) или от клеммы (+) и повторяли измерения в катодно и анодно поляризованном мостиках.
Результаты исследования и их обсуждение
Синтез ЦЭКН, ЦЭКК, ЦЭГН и ЦЭГК материалов проводили по следующей методике. Образцы ЦЭ пропитывали в растворе аммиакатов, отжимали фильтровальной бумагой, помещали в раствор боргидрида натрия и выдерживали в условиях выделения водорода до прекращения выделения аммиака, отмывали водой, сушили, выдерживали в 3 моль/л растворе H2SO4 или 3 моль/л растворе NaOH, споласкивали водой и сушили. Содержание металлов было определено по ходу синтеза до восстановления ионов путем титрования Трилоном Б. Содержание H2SO4 и NaOH было определено кислотно-основным титрованием и весовым методом. Параллельно в тех же условиях были синтезированы ЦЭК и ЦЭГ. Данные приведены в табл. 1. В той же таблице приведены значения сопротивления и сорбционной емкости слоев.
Таблица 1
Характеристики слоя в материалах
|
Материал |
Содержание, ммоль/г |
Сопротивление, Ком |
Сорбционная емкость ммоль/г |
||
|
металл |
H2SO4/NaOH |
бензол |
гексан |
||
|
ЦЭКН ЦЭКК ЦЭК ЦЭГН ЦЭГК ЦЭГ |
0,244 0,249 – 0,244 0,249 – |
3,29 3,32 3,00 5,71 5,70 5,18 |
22,4 21,9 28,4 15,3 14,9 22,2 |
0,98 0,84 1,25 2,44 ≈ 0,14 5,14 |
0,85 0,63 1,09 2,36 1,22 4,71 |
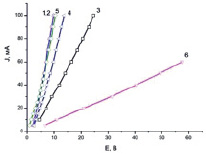
Рис. 1. Вольтамперные кривые для неполяризованных мостиков: 1 – ЦЭКН, 2 – ЦЭКК, 3 – ЦЭК, 4 – ЦЭГН, 5 – ЦЭГК, 6 – ЦЭГ
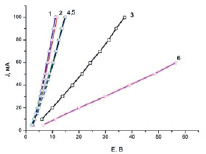
Рис. 2. Вольтамперные кривые для катодно-поляризованных мостиков: 1 – ЦЭКН, 2 – ЦЭКК, 3 – ЦЭК, 4 – ЦЭГН, 5 – ЦЭГК, 6 – ЦЭГ
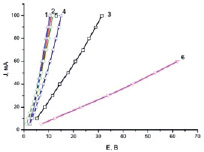
Рис. 3. Вольтамперные кривые для анодно поляризованных мостиков: 1 – ЦЭКН, 2 – ЦЭКК, 3 – ЦЭК, 4 – ЦЭГН, 5 – ЦЭГК, 6 – ЦЭГ
Зависимости тока от напряжения в цепи с мостиками приведены на рис. 1–3. Из кривых (рис. 1) рассчитывали напряжение начала движения ионов в неполяризованном мостике (ЕДв), константы скорости и (К1Дв) и константы ускорения, возникающего вследствие изменения структурной организации водородных связей в поле движущихся зарядов (К2Дв), используя уравнение I/F = К1Дв(Е – ЕДв) + К2Дв(Е – ЕДв)2, где F – число Фарадея, согласно [6]. Из зависимостей (рис. 1 и 2) рассчитывали напряжение начала образования Н2 или O2 (ЕВ и ЕК), констант скорости (К1В и К1К) и констант ускорения этих реакций (К2В и К2К), используя аналогичные уравнения [1]. Данные приведены в табл. 2.
Таблица 2
Характеристики мостиков в электрохимических матрицах
|
Материал |
Неполяризованный мостик |
Катодно-поляризованный мостик |
Анодно-поляризованный мостик |
||||||
|
ЕДв, В |
К1Дв105 г-экв/ В*сек |
К2Дв107 г-экв / В*сек2 |
ЕВ, В |
К1В105 г-экв / В*сек |
К2В107 г-экв / В*сек2 |
Ек, В |
К1К105 г-экв / В*сек |
К2К107 г-экв / В*сек2 |
|
|
ЦЭКН ЦЭКК ЦЭК |
1,87 2,01 2,25 |
12,4 11,6 4,6 |
12,4 34,2 0,24 |
2,25 2,47 2,77 |
11,26 10,04 3,12 |
12,44 14,4 2,84 |
2,19 2,18 2,58 |
11,2 9,98 1,74 |
4,12 4,80 0,44 |
|
ЦЭГН ЦЭГК ЦЭГ |
1,12 1,0 1,36 |
7,04 7,46 1,05 |
29,6 24,3 5,18 |
1,72 1,21 1,80 |
6,6 6,22 1,1 |
27,5 10,3 4,71 |
1,29 1,2 1,56 |
6,72 6,84 0,96 |
24,6 19,6 7,67 |
Заключение
Выше отмечалось, что окружение этаноламиновыми лигандными группами в комплексах Ni (0) или Co (0) такое же, как в комплексах Ni (2+) и Co(2+) до восстановления. В нашем случае отношение содержания этаноламиновых группировок к содержанию металлов для комплексов никеля равно 3,53, а кобальта – 3,45. Это означает, что в слоях имеются примерно одинаковое число сфер, в которых с центральным атомом связаны три или четыре этаноламиновых группы.
Содержание H2SO4 в ЦЭН(H2SO4) и в ЦЭК(H2SO4), как видно из табл. 1, на 0,29 и на 0,32 ммоль/г больше, чем в ЦЭ(H2SO4), а содержание NaOH в ЦЭН(NaOH) и в ЦЭК(NaOH) на 0,53 и на 0,53 ммоль/г больше, чем в ЦЭ(NaOH). Отношение этих разностей к содержанию металлов отвечает числу анионов, координированных к центральным атомам. Следовательно, к Ni (0) или Co(0) координированы примерно один SO42- или два OH-.
Сопротивление ЦЭН(H2SO4) и ЦЭК (H2SO4), как видно из табл. 1, на 21,1 % и на 22,8 % больше, чем ЦЭ(H2SO4), а ЦЭН(NaOH) и ЦЭК(NaOH) на 31,1 % и 32,9 % меньше, чем в ЦЭ(NaOH). Это можно объяснить тем, что Ni (0) или Co (0) в порах переходной зоны контактируют как с углеродными структурами, так и с атомами из других пор. В результате этого в слоях имеется разветвлённая система электронной проводимости.
Сорбционная емкость ЦЭН(H2SO4) и ЦЭК (H2SO4), а также ЦЭН(NaOH) и ЦЭК (NaOH), как видно из табл. 1, меньше чем у ЦЭ(H2SO4) и ЦЭ(NaOH). Это указывает на то, что за счет атомов металлов вместе с координированными анионами уменьшается объем сорбционного пространства, в котором находятся молекулы бензола и гексана.
Напряжение, при котором начинается движение ионов или образование H2 и O2, в мостиках из ЦЭН(H2SO4) и ЦЭК(H2SO4) и в мостиках из ЦЭН(NaOH) и ЦЭК(NaOH), как следует из табл. 2, меньше, чем в мостиках из ЦЭ(H2SO4) и ЦЭ(NaOH). Величины, на которые уменьшается ЕДв, ЕВ и Ек коррелируют со значениями, на которые увеличивается содержание H2SO4 или NaOH. Это можно объяснить тем, что координация анионов приводит к уменьшению энергии перехода H2SO4 или NaOH из раствора в слой, а так энергии активации реакций электрохимического восстановления или окисления аквакомплексов.
Скорость и ускорение движения ионов, а также скорость и ускорение образования H2 и O2 в мостиках из мостиках из ЦЭН(H2SO4), ЦЭК(H2SO4), ЦЭН(NaOH) и ЦЭК(NaOH) в несколько раз больше, чем в мостиках из ЦЭ(H2SO4) и ЦЭ(NaOH). Это подтверждает наше предположение о возможности движения электронов с частиц угля на атомы металлов и наоборот. В этом случае реакций электрохимического восстановления или окисления аквакомплексов происходят не только в зоне прививки производных ПВХ к микрочастицам угля, но и в порах со стенкам из производных ПВХ.
Библиографическая ссылка
Цивадзе А.Ю., Фридман А.Я., Новиков А.К., Титова В.Н., Явич А.А., Морозова Е.М., Полякова И.Я., Шабанов М.П. СЛОИ ИЗ ПРИВИТЫХ К АКТИВНОМУ УГЛЮ ЭТАНОЛАМИНОВЫХ ПРОИЗВОДНЫХ ПВХ С КОМПЛЕКСАМИ CO (0) ИЛИ NI (0) И H2SO4 ИЛИ NAOH НА ТКАНИ // Успехи современного естествознания. 2018. № 12-1. С. 20-24;URL: https://natural-sciences.ru/ru/article/view?id=36968 (дата обращения: 05.05.2026).



