Поиск новейших средств химической защиты здоровья человека, животных и растений и проблема создания новых лекарственных средств продолжают оставаться актуальными задачами, так как ни один из известных лекарственных препаратов однозначно не отвечает современным требованиям медицины, часто из-за высокой токсичности, плохой растворимости, наркотического действия, что препятствует их широкому использованию в медицинской практике.
В этом плане амидные производные по гликозидному центру моно- и олигосахаридов являются интересными модельными объектами при изучении не только молекулярных механизмов кислотно-основного и нуклеофильного катализа реакций сахаров, но и в создании устойчивых, малотоксичных, гидролитически устойчивых лекарственных препаратов. Подходы к синтезу углеводсодержащих соединений могут быть разными. Например, введение углеводных остатков в структуру биологически активных соединений с целью повышения растворимости, понижения их токсичности, изменения спектра биологического действия; или структурно-химическая модификация самого физиологически активного фрагмента [1–4].
Среди многих производных п-амино- бензойной кислоты найден ряд эффективных местных анестетиков, такие ее эфиры, как анестезин, новокаин и дикаин, стали успешно заменять в клинике алкалоид кокаин, не вызывая при этом болезненного привыкания к лекарству. N–углеводные производные (на основе глюкозы и галактозы) этилового эфира п-аминобензойной кислоты относятся к одной из значимых в медицине групп биологически активных соединений.
Целью работы является модификация метода синтеза углеводных производных на основе реакции N-гликозилирования этилового эфира п-аминобензойной кислоты и использование квантово-химических индексов реакционной способности полученных веществ для прогнозирования их биологической активности.
В качестве углеводов в данной работе использовали D-глюкозу, D-галактозу, агликоном выбран этиловый эфир п-аминобензойной кислоты. Выбор агликона обусловлен его биологической активностью. Известно, что п-аминобензойная кислота является структурной основой современных анестетиков [1; 3; 4]. Эфиры п-аминобензойной кислоты находят широкое применение в медицине, фармакологии.
Использование сахаров в качестве гидрофильной матрицы позволяет повысить водную растворимость и понизить токсичность фармакологически активных препаратов.
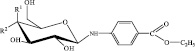
Реакции взаимодействия сахаров с этиловым эфиром п-аминобензойной кислоты в среде этанола приводят к образованию их углеводных производных (схема).
Материалы и методы исследования
ИК-спектры получены на спектрофотометре «Nicolet Avatar 370 GDTS» в диапазоне 4000–400 см-1 (прессование с KBr). Чистота соединений II, IIIa и IIIb определялась методом тонкослойной хроматографии (ТСХ) на пластинах Silufol. Оценку компьютерного прогнозирования биологической активности определяли методом PASS (Prediction of activity Spectra for Substans: Complex and Trainity).
Результаты исследования и их обсуждение
Экспериментальные данные позволяют считать, что с помощью реакции N–гликозилирования можно получить конечные продукты, используя в качестве сахаров глюкозу и галактозу, а агликоном был эфир п-аминобензойной кислоты. Контроль за ходом реакции осуществляли методом ТСХ в системах: бутанол: уксусная кислота: вода = 4:1:5; хлороформ: метанол = 19:1. Некоторые физико-химические характеристики представлены в табл. 1.
Таблица 1
Выход и величина хроматографической подвижности полученных веществ
|
№ соединения |
Выход, % |
Rf (*,**,***) |
|
II |
80 |
0,91*, 0,93*** |
|
IIIa |
85 |
0,63* |
|
IIIb |
76 |
0,7** |
Синтез N-углеводных производных этилового эфира п-аминобензойной кислоты
Смесь 1,8 г моносахарида (0,01 моль), 1,81 г (0,011 моль) этилового эфира п-аминобензойной кислоты, 0,3 мл уксусной кислоты и 15 мл этилового спирта нагревают на водяной бане в течение 30–40 минут. Горячую смесь раствора фильтруют. Выпавший осадок перекристаллизовывают [2]. Ход реакции контролируют методом ТСХ.
Структуры и чистота новых углеводных производных: N–(b–D–глюкопиранозил) этиловый эфир п–аминобензойной кислоты и N–(b–D–галактопиранозил) этиловый эфир п-аминобензойной кислоты были подтверждены данными УФ–спектроскопии и ИК–спектроскопии, методом ТСХ и бумажной хроматографией.
Подлинность этилового эфира п-аминобензойной кислоты также была установлена по УФ-спектру раствора в метаноле в области 190-400 нм на рис. 1.
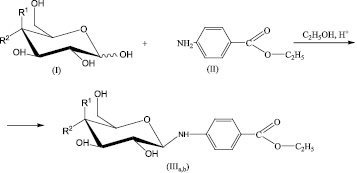
IIIa R1 = H (глюкоза); R2 = OH.
IIIb R1 = OH (галактоза); R2 = H
Способ получения углеводных производных п-аминобензойной кислоты
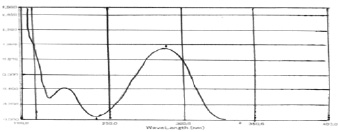
Рис. 1. УФ-спектр этилового эфира п-аминобензойной кислоты
ИК-спектры синтезированных соединений приведены на рис. 2–4. Для анализа и интерпретации полученных данных приведены ИК-спектры чистого этилового эфира п-аминобензойной кислоты и новых углеводных производных на его основе.
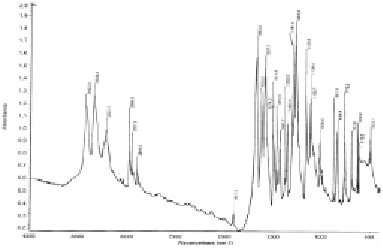
Рис. 2. ИК-спектр этилового эфира п-аминобензойной кислоты
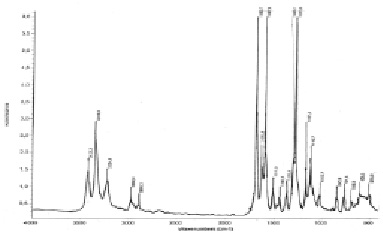
Рис. 3. ИК-спектр N-(β-D-глюкопиранозил) этилового эфира п-аминобензойной кислоты
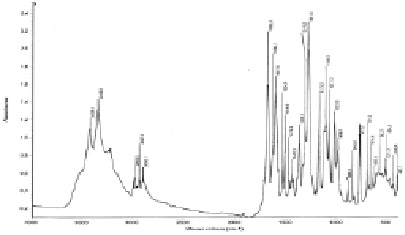
Рис. 4. ИК-спектр N-(β-D-галактопиранозил) этилового эфира п-аминобензойной кислоты
В табл. 2 приведены валентные и деформационные колебания основных частот (n (N-H), см-1; n (O-H), см-1; n (C=O) см-1; d (N-H) см-1; n (C-O-С), см-1) полученных веществ.
Таблица 2
Характеристические полосы поглощения синтезированных соединений
|
№ соединения |
n (N-H), см-1 |
n (O-H), см-1 |
n (C-H), d (C-H), см-1 |
n (C=O), d (N-H), см-1 |
n (аром.), см-1 |
n (C-O-С), см-1 |
|
II |
3423–3343 |
– |
3222–2889 882–701 |
1683 1597 |
1281 |
1280–1125 |
|
IIIa |
3425 |
3346 |
2898–2983 989–640 |
1608–1442 |
1281–1023 |
1281–1024 |
|
IIIb |
3423 |
3343 |
2899–2985 882–616 |
1597–1442 |
1280–1025 |
1273–1022 |
Из данных, приведенных в табл. 2, видно, что характеристические полосы поглощения колебаний ОН группы в области 3345 см-1 в чистых моносахаридах наблюдаются при С1 углеродном атоме. Отсутствие колебаний ОН группы в этой области четко свидетельствует о прохождении реакции N-гликозилирования, т.е. осуществляется взаимодействие по С1 углеродному атому моносахарида через атом азота аминной группы этилового эфира п-аминобензойной кислоты. Изменения в деформационных и валентных колебаниях по аминогруппе свидетельствуют о взаимодействии углеводов с этиловым эфиром п-аминобензойной кислоты.
Компьютерное прогнозирование биологической активности
Биологическую активность химического соединения можно связать с определенным набором химических реакций, происходящих с веществом в организме, в пределах ряда родственных соединений. Степень проявления биологической активности будет определяться способностью членов ряда вступать в химические реакции определенного типа. Принято считать, что молекулы биологически активного вещества претерпевают в организме ряд физико-химических и химических превращений. Это такие процессы, как растворение, сорбция, распределение, связывание, химическая реакция, выделение и т.п. Очевидно, что любой из этих этапов или их сочетание в каждом конкретном случае может определять направленность фармакологического действия вещества или являться лимитирующей стадией суммарного эффекта, определяемого как биологическая активность. Для описания физиологической активности вышеназванных соединений необходимо оценить как минимум четыре физико-химические характеристики соединений, такие как способность вещества распределяться между водной и липидной фазой, объемом молекулы, заряд и «основность» азотсодержащих соединений. Для сравнения реакционной способности в рядах родственных соединений часто применяют методы, основанные на сравнении квантово-химических индексов реакционной способности (ИРС) молекул – величин, получаемых при помощи квантово-химических расчетов (программа PASS) [5–8]. На основании структуры соединения можно количественно оценить вероятность наличия у него активности (Ра) и неактивности (Рi) различных видов биологической активности. Чем больше для конкретной активности величина Ра и чем меньше величина Рi, тем больше шанс обнаружить данную активность у вещества, полученного в эксперименте. Наиболее вероятные виды биологической активности (Pa > 0,5 %) представлены в табл. 3. Базовой структурой для направленного поиска было выбрано соединение: N-(b-D-глюкопиранозил) этилового эфира п-аминобензойной кислоты.
Таблица 3
Данные компьютерного прогноза биологической активности
|
№ соед. |
Структура |
Pa |
Виды активности |
|
IIIa |
|
0,919 0,886 0,801 0,803 0,708 0,697 0,690 0, 680 0,659 0,576 0,375 |
Ингибитор антранилат фосфорибозил трансферазы Антигеморрагическая Антивирусная (грипп) Иммуностимулятор Противодиабетическая Антимикобактериальная Противотуберкулезная Антивирусная (Picornavirus) Антиэкзематическая Противовоспалительная Анестетик (общая) |
Заключение
1. Процесс взаимодействия сахаров (глюкозы и галактозы) с производными п-аминобензойной кислоты происходит с обращением конфигурации при С1 углеродном атоме (трансгликозилирование).
2. Установлена структура и индивидуальность полученных соединений с помощью методов: ИК- и УФ-спектроскопии, ТСХ.
3. Данные по прогнозированию биологической активности (программа PASS) углеводных производных п-аминобензойной кислоты показывают, что они обладают потенциально высокой антигеморрагической, антивирусной, антидиабетической, антимико-бактериальной и другими видами активности.
Библиографическая ссылка
Джаманбаев Ж.А., Абдурашитова Ю.А., Сарымзакова Р.К., Эралиева М.Г. СИНТЕЗ УГЛЕВОДНЫХ ПРОИЗВОДНЫХ П-АМИНОБЕНЗОЙНОЙ КИСЛОТЫ // Успехи современного естествознания. 2019. № 3-2. С. 127-132;URL: https://natural-sciences.ru/ru/article/view?id=37081 (дата обращения: 27.04.2026).