Равновесие между гидроксидом состава Me(OH)n(тв.) (n - степень окисления металла) с насыщенным водным раствором описывается уравнением:
Me(OH)n(тв.) Û Men+ + nOH- (1)
Помимо реакции (1) над осадком гидроксида металла протекают процессы образования гидроксокомплексов в соответствии со следующим уравнением:
iMеn+ + jOH- Û Mеi(OH)j (2)
Количественной характеристикой таких равновесий служат общие константы образования соответствующих комплексов
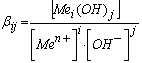 .
.
Растворимость гидроксидов с насыщенным водным раствором S равна суммарной концентрации всех гидроксокомплексов металла в растворе, образованных в результате растворения осадка:
![]() (3)
(3)
Концентрацию иона металла Men+ можно найти из произведения растворимости ПР = [Men+]·[OH-], а концентрации гидроксокомплексов - из общих констант образования.
Если предположить, что в области минимальной растворимости металл находится в растворе в виде нейтрального гидроксокомплекса Ме(ОН)n0 и соседних комплексов Ме(ОН)n-1 и Mе(OH)n+1, то в соответствии с уравнением (3) растворимость гидроксидов Ме(II) и Me (III) будет определяться выражениями:
SII = [Mе(OH)+] + [Mе(OH)20] + [Mе(OH)3-] (4)
SIII = [Mе(OH)2+] + [Mе(OH)30] + [Mе(OH)4-] (5)
С учетом выражений для произведения растворимости и общих констант образования гидроксокомплексов уравнения (4), (5) принимают форму:
SII = ПР∙b11∙[ОH-]-1 + ПР∙b12 + ПР∙b13∙[ОH-] (6)
SIII = ПР∙b12∙[ОH-]-1 + ПР∙b13 + ПР∙b14 ∙[ОH-] (7)
Известно, что для ионов металлов растворимость как функция рН проходит через минимум. Значение Smin определяется из условия ![]() .
.
Продифференцировав уравнения (6), (7) по рН, получаем
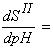 - ПР∙b11∙[ОH-]-2 + ПР∙b13 (8)
- ПР∙b11∙[ОH-]-2 + ПР∙b13 (8)
![]() - ПР∙b12∙[ОH-]-2 + ПР∙b14 (9)
- ПР∙b12∙[ОH-]-2 + ПР∙b14 (9)
Очевидно, что уравнение (8) равно нулю при ![]() , а уравнение (9) при
, а уравнение (9) при ![]() .
.
Приблизительный интервал начальных и конечных значений рН, соответствующих Smin можно найти из предположения, что рНнач. соответствует равенству [Ме(ОН)n0] = [Ме(ОН)n-1], а рНкон. - [Ме(ОН)n0]=[Mе(OH)n+1]. Тогда: для
Ме(ОН)2(тв.) ![]()
![]() (10)
(10)
для
Ме(ОН)3(тв.) ![]()
![]() (11)
(11)
Подставляя в уравнения (4), (5) соответствующие [ОН-], получим выражения для минимальной растворимости гидроксидов Ме(ОН)2(тв.) и Ме(ОН)3(тв.):
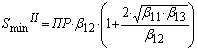 (12)
(12)
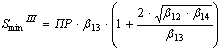 (13)
(13)
Рассчитанные по уравнениям (12) и (13) значения Smin и значения рН, соответствующие им, для гидроксидов Zn (II), Cu(II), Fe (II), Mn (II), Ni (II), Co (II), Cd(II), Pb (II), Fe (III) и Cr(III) приведены в таблице. Из которой видно, что растворимость гидроксидов изменяется в широких пределах от 5,34·10-5 моль/л для Pb(OH)2 до 3,31·10-10 моль/л для Fe(OH)3. Проанализировав полученные цифры, гидроксиды металлов по растворимости можно расположить в следующий ряд: Pb2+ > Zn2+ > Cr3+ > Co2+ > Cd2+ > Mn2+ > Fe2+ > Ni2+ > Cu2+ > Fe3+.
Таблица 1. Метод расчета минимальной растворимости гидроксидов металлов в водной среде, а также значений рН, при которых растворимость минимальна.
|
Men+ |
Упрощенный метод расчета |
Полный метод расчета |
||||
|
Интервал рН |
pHопт. |
Smin, моль/л |
Интервал рН |
pHопт. |
Smin, моль/л |
|
|
Zn2+ |
7,9 - 11,5 |
9,7 |
1,8·10-6 |
9,5-10,5 |
10 |
1,8·10-6 |
|
Cu2+ |
9,3 - 10,5 |
9,9 |
3,1·10-10 |
~10 |
10 |
3,2·10-10 |
|
Fe2+ |
10,4 - 11,1 |
10,8 |
1,0·10-7 |
10,5-11 |
11 |
1,1·10-7 |
|
Ni2+ |
9,1 - 11,0 |
10,1 |
8,2·10-9 |
10-10,5 |
10 |
8,4·10-9 |
|
Mn2+ |
11,6 - 12,6 |
12,1 |
1,6·10-7 |
~13 |
13 |
1,1·10-6 |
|
Pb2+ |
9,4 - 10,9 |
10,2 |
5,3·10-5 |
10-10,5 |
10 |
6,0·10-5 |
|
Co2+ |
9,2 - 12,7 |
10,9 |
3,3·10-7 |
10-11,5 |
11 |
3,3·10-7 |
|
Cd2+ |
10,3 - 12,9 |
11,6 |
2,2·10-7 |
11-12 |
11,5 |
2,2·10-7 |
|
Fe3+ |
6,3 - 9,6 |
8,0 |
3,3·10-10 |
7-9 |
8 |
3,3·10-10 |
|
Cr3+ |
8,3 - 9,4 |
8,9 |
1,6·10-6 |
8,5-9 |
9 |
1,6·10-6 |
Проанализировав таблицу, можно сделать вывод, что значения минимальной растворимости по упрощенному методу, предложенному в данной работе, и полному методу расчета (с учетом всех гидроксокомплексов) практически совпадают для всех металлов, кроме марганца; интервал рН, при котором растворимость минимальна, рассчитанный по упрощенному методу более широкий, чем интервал, рассчитанный по полному методу. Однако по упрощенному методу можно более точно определить рНопт.
Таким образом, полученные данные позволяют оценить эффективность гидроксидного метода очистки сточных вод от ионов тяжелых металлов, а также усовершенствовать процессы очистки природных и промышленных вод.
Библиографическая ссылка
Пестриков С.В., Исаева О.Ю., Сапожникова Е.Н., Легушс Э.Ф., Красногорская Н.Н. РАСЧЕТНЫЙ СПОСОБ ОПРЕДЕЛЕНИЯ УСЛОВИЙ УДАЛЕНИЯ ИОНОВ ТЯЖЕЛЫХ МЕТАЛЛОВ ИЗ СТОЧНЫХ ВОД // Успехи современного естествознания. 2005. № 1. С. 27-28;URL: https://natural-sciences.ru/ru/article/view?id=7740 (дата обращения: 14.05.2026).



