Scientific journal
Advances in current natural sciences
ISSN 1681-7494
"Перечень" ВАК
ИФ РИНЦ = 0,976
KINETIC`S STUDY OF PHENOL AND 3-CHLOROPHENOL OXIDATION IN AQUEOUS SOLUTIONS ON TI ANODES WITH PT AND СЕPT COATINGS
Загрязнение водных экосистем опасными химическими соединениями стало глобальной экологической проблемой современности. Вот почему Генеральная Ассамблея ООН объявила 2005–2015 годы Международным десятилетием действий «Вода для жизни». Фенолы и хлорфенолы – вещества, оказывающие опасное воздействие на живые организмы, включая человека. Их относят к стойким органическим загрязнителям окружающей среды (COЗ) и они включены в список двенадцати СОЗ, полного уничтожения которых требует ратифицированная РФ Стокгольмская конвенция 2011 г. Фенол и хлорфенолы давно используются как антисептики, дезинфектанты, они входят в состав фунгицидов и пестицидов. В условиях медленной биодеградации эти вещества накапливаются в почве. Новой проблемой 21 века стало доказательство образования из хлорфенолов полихлорированных дибензодиоксинов и дибензофуранов [1]. Они токсичнее хлорированных фенолов, поэтому увеличение содержания данных веществ в окружающей среде, в первую очередь в продуктах питания, вызывает большое беспокойство [2].
Химические методы очистки позволяют частично или полностью разлагать фенолы и хлорфенолы или же переводить их в менее токсичные формы, способные к дальнейшей биодеградации. Одним из них является электрохимический метод анодного окисления. Исследования в области удаления фенола и хлорфенолов из водных растворов остаются актуальными, и они важны для разработки комплексных технологий очистки воды, которые могут включать и электрокаталитический метод. Традиционными являются платиновые электроды. Окисление производных хлорфенолов на Pt анодах изучено в диссертации [3]. Введение церия в состав PtTi электрода увеличивает скорость электрохимического окисления 4-хлорфенола и 2,4-дихлорфенола согласно результатам работы [4]. В электроокислении активны и металлоксидные аноды [5]. Оптимизация условий для получения высокой скорости окисления базируется на выборе фонового раствора, состава анода, а также анализе механизма сложного гетерогенного процесса.
Цель данной работы – используя метод циклической вольтамперометрии, определить кинетические характеристики анодного окисления фенола и 3-хлорфенола на платинированных титановых анодах с добавками церия и сурьмы.
Электроды, оборудование
Титановую фольгу (99 %) толщиной 100 мкм после специальных обработок подвергали платинированию в 0,1 М растворе тетранитрито-платината калия квалификации «х.ч.» в течение 1,5 ч при токе 40 мА, напряжении 21 В и рН6. Видимая поверхность анодов – 2 см2 (две стороны). Истинная поверхность анода определялась по пику водорода анодной ветви сернокислотного раствора. Для образца Pt/Ti коэффициент шероховатости поверхности равен 30, и он не изменился при модифицировании платины церием и сурьмой. Процент платины – 2,2 % от массы титана определен весовым методом. По данным энергодисперсионного анализа (рентгенофлуоресцентный спектрометр Clever-С31) в слое толщиной 1 мкм платины 15 % вес, от массы титана. Образцы СePt/Ti и SbPt/Ti были получены добавлением в раствор нитрата церия или нитрата сурьмы при тех условиях электроосаждения.
Потенциодинамические кривые (вольтамперограммы) регистрировали в фоновых растворах 0,5 М H2SO4 и 1 MNaOH при комнатной температуре, скорости развертки потенциала 100 мВ/с и различных начальных концентрациях вещества в интервале 0,01-0,1 мМ с использованием газо-диффузионной (аргон) 3-электродной ячейки с хлорсеребряным электродом сравнения. Для каждого образца результирующую IE кривую фиксировали после 20–30 циклирований на многофункциональном вольтамперметре ЭЛ-02, соединенном с компьютером (ошибка по току не более 5 %).
Результаты исследования и их обсуждение
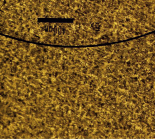
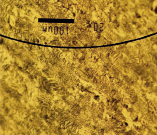
На рис. 1 показаны микрофотографии поверхности модифицированных электродов после электрохимических опытов, полученных с помощью электронного микроскопа Jeol JSM-6490LV.
|
Pt /Ti |
CePt /Ti |
SbPt /Ti |
Рис. 1. Морфология поверхности анодов (данные сканирующей электронной микроскопии)
На поверхности четко видны агрегаты платины, которые достаточно равномерно покрывают поверхность Ti-фольги (светлый фон). Также у Pt/Ti в виде крупных затемненных пятен видны области тонких пленок, по-видимому, углеродистых отложений. Рельеф покрытия анодов CePt/Ti и SbPt/Ti отличается от Pt/Ti: хорошо видно более равномерное распределение частиц платины в присутствии церия и сурьмы, а также отличие покрытия с сурьмой и церием. У образца SbPt/Ti можно рассмотреть вытянутые по форме кристаллы. Большая часть поверхности остается свободной от платины.
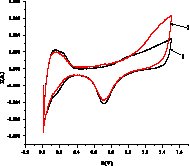
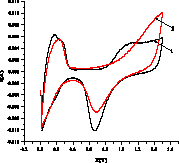
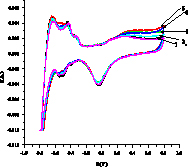
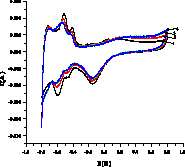
На рис. 2 показаны примеры вольтамперограмм для кислого (а,б) и щелочного (в,г) растворов 3-хлорфенола, из которых определяется ток I, мА в максимуме при 1,4 В в H2SO4 и 0,8 В в NaOH. Ток (скорость) окисления Iox – это разность между током I и током фона. Окисление субстрата Х начинается после окисления платины (образования оксида PtOx) и происходит с его участием Х + PtOx > Pt + Хox или Х + PtOx+1 > PtO + Хox согласно данным [6]. В левой части I-E кривой находятся области адсорбции/десорбции водорода, на катодной области при потенциалах около -0,1В (кислота) и 0,7 В (щелочь) мы видим пик разложения PtOx > Pt + Oадс с восстановлением платины и образованием адатома кислорода.
|
а |
б |
|
в |
г |
Рис. 2. Примеры вольтамперограмм окисления 3-хлорфенола в кислой среде на анодах CePt/Ti (а), SbPt/Ti (б) при концентрации 0,08 мМ (черная линия – фон, 0,5М H2SO4) и в щелочной среде на анодах CePt/Ti (в) и SbPt/Ti (г) при концентрациях 0,0164 (2), 0,032 (3), 0,0476 (4), 0,0625 (5), 0,0769 мМ, черная линия 1 – фон 1М NaOH
Из вольтамперограмм следует, что при окислении органического вещества ток увеличивается, значения Iox возрастают с ростом концентрации. Пики водородной области (Н1 и Н2 – две формы адсорбированного водорода) уменьшаются. Также уменьшается катодный пик кислорода. Это связано с блокировкой центров анода адсорбированными Х и продуктами окисления, способными к полимеризации. Аналогичный результат для фенола.
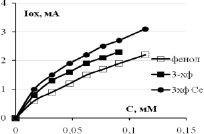
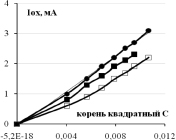
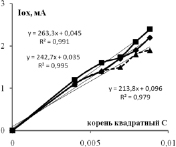
Зависимости тока (скорости) окисления от концентрации фенола и 3-хлорфенола показаны на рис. 3. Видно, что они нелинейные и порядок электроокисления меньше единицы. В координатах дробного порядка n = ½ получаются хорошие прямые линии с регрессионным коэффициентом R2 не хуже 0,95. Тангенс угла наклона прямой Iox = KC½ – это константа скорости электроокисления K1/2. Значения констант K1/2 для трех электродов и двух веществ приведены в табл. 1. Из данных таблицы видно, что K1/2 возрастают в ряду Pt /Ti < СеPt /Ti < SbPt /Ti. Значения K1/2 фенола и 3-хлорфенола отличаются: у 3ХФ они, как правило, больше по сравнению с фенолом, так в щелочной среде для анодов Pt/Ti на 18 % и для SbPt /Ti на 27 %, а в кислой среде у СеPt /Ti на 14 % и у SbPt /Ti на 90 %. Активность сурьмяно-платино-титанового анода воспроизводится, как видно из нижней строчки табл. 1.
|
а |
б |
|
в |
г |
Рис. 3. Концентрационные зависимости тока окисления фенола и 3-хлорфенола в кислой и щелочной среде для анодов, модифицированных церием и сурьмой
Таблица 1
Константы скорости K1/2 [мА*(л/моль)1/2] электроокисления фенола и 3-хлорфенола при комнатной температуре и скорости развертки потенциала 100 мВ/с
|
Среда |
Кислая среда |
Щелочная среда |
||
|
Электрод |
фенол |
3-ХФ |
фенол |
3-ХФ |
|
Pt /Ti |
190 |
195 |
198 |
233 |
|
СеPt /Ti |
209 |
238 |
241 |
246 |
|
SbPt /Ti |
245 |
275 |
203 |
258 |
|
SbPt /Ti* |
242 |
– |
214 |
263 |
Примечание: образец * проверен на воспроизводимость активности через 1 год.
Концентрационные зависимости скорости электроокисления с дробным кинетическим порядком можно объяснить адсорбцией из раствора ассоциированных форм субстрата (димеров и тримеров). Перед стадией электроокисления нужна диссоциация комплекса на поверхности электрода с образованием мономерной формы вещества. Эта стадия, по-видимому, и является лимитирующей стадией электроокисления в целом. Двухстадийную адсорбцию с диссоциацией комплекса, которая предшествует окислению, можно записать схемой Хm(раствор) - Хm(электрод) > mХадс > электроокисление. Учитывая распад молекулярных комплексов на электроде, мы получаем формальный порядок меньше единицы n = 1/m, где m – число молекул и нелинейные зависимости Iox–C.
Теперь рассмотрим влияние начальной концентрации 3-хлорфенола на суммарные количества окисленного 3-хлорфенола (ОХ), адсорбцию/десорбцию водорода (Н), адсорбцию атомарного кислорода после разложения оксида платины (О). Промотирующий эффект добавок на примере церия проявляется и в этих характеристиках. Изменение адсорбции Н и О в условиях окисления показывает наличие на поверхности анода свободных центров для реакций Надс – е > Н+раствор в условиях кислой среды и PtO + e > Pt + Oадс. Площади пиков S определяются интегрированием соответствующих трех областей I–E кривых. Для корректного сравнения можно рассчитать относительное изменение площади пиков с учетом площади пиков фонового раствора по формуле S % = 100 (S-Sфон)/Sфон.
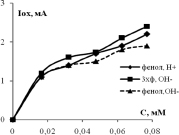
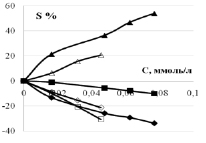
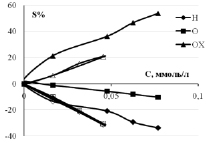
Как видно из рис. 4, для окисляемого вещества значения S % увеличивается с ростом концентрации (S % > 0), выше значения S % у образца с добавкой Ce (аналогично и для Sb). Значения S % водородной и кислородной областей отрицательные (S % < 0): уменьшение площади пиков связано с хемосорбцией субстрата, как уже мы писали выше, из-за которой активные центры поверхности блокированы. Концентрационные зависимости S % можно аппроксимировать прямыми линиями и рассчитать линейный градиент DS/DC как изменение площади соответствующих пиков. Эти значения приводятся в табл. 2. У анода СеPt/Ti линейный положительный градиент окисления DS/DC существенно больше, чем у Pt/Ti: в 663/437~2 раза в кислой среде и в 662/469 ~1,4 раза в щелочной среде.
|
а. 0,5 M H2SO4 |
б. 1M NaOH |
Рис. 4. Относительное изменение площади пиков I–E кривых в водородной, кислородной областях и области окисления 3-хлорфенола на анодах Pt/Ti (незакрашенные) и CePt/Ti (закрашенные значки) в кислом и щелочном фоновом растворе
Таблица 2
Линейный градиент площади пиков (DS/DC) окисления 3-хлорфенола, десорбции/адсорбции водорода и кислорода
|
Среда |
3ХФ, Н+ |
3ХФ, ОН- |
||
|
Анод |
Pt/Ti |
CePt/Ti |
Pt/Ti |
CePt/Ti |
|
ОХ |
+337 |
+663 |
+ 469 |
+ 662 |
|
Дес./Адс. Н |
– 320 |
– 413 |
– 686 |
– 409 |
|
Дес.О |
– 266 |
– 181 |
– 675 |
– 135 |
Отрицательный градиент кислорода уменьшается в присутствии церия, также как и для водорода в щелочной среде. Наибольшее изменение у кислорода в щелочном растворе 3ХФ: 675/135 = 5 раз, а у водорода только в 1,7 раза. Только в кислом растворе 3-ХФ у СеPt/Ti значение DS/DC для адсорбированного Н по модулю больше. Итак, введение церия и сурьмы увеличивает окислительную способность анода за счет снижения дезактивации центров адсорбции кислорода и/или облегчения распада оксида платины.
Ассоциаты фенола и 3-хлорфенола
Квантово-химические расчеты индивидуальных молекул и их молекулярных комплексов были проведены с использованием программы HyperChem 8.0.8. Хотелось понять, каково изменение межъядерных расстояний при ассоциации? Как влияет растворитель на длины связей O-C, С-Cl, водородной связи при помещении Х и их димеров в «водяной бокс» (метод AMBER с параметрами по умолчанию)? Некоторые комплексы оптимизированной геометрии показаны на рис. 5.
|
ассоциат 3ХФ с молекулой воды |
димер 3-ХФ |
тример фенола |
тример 3-ХФ |
Рис. 5. Комплексы оптимизированной геометрии
В табл. 3 приведены дипольные моменты μ, энергия нижней вакантной МО (знак «+» означает, что молекула нуклеофил, « – » электрофил), энергии связи фенольных молекул с водой ЕХ+Н2О, энергии водородной связи в димере ЕХ+Х и тримере Е`Х+Х+Х (` – на одну связь). В присутствии атома хлора энергия водородной связи в димере и тримере увеличивается. Энергия водородной связи димера 3ХФ (ЕХ+Х = 3,9 ккал/моль) в 2 раза больше, чем в ассоциате с водой (ЕХ+Н2О = 1,71 ккал/моль). Длина водородной связи у димеров и тримеров такая же, как и между фенольной молекулой и водой (1,83 A). Ассоциация наблюдается и с «растворенными молекулами»: рис. 6 демонстрирует димер 3ХФ в «боксе» с 48 молекулами воды. При «растворении» увеличение длин связей С-О и С-Cl небольшое (не более 1,6 и 5,2 % соответственно). Но для водородной связи О…Н в димере это увеличение существенное, оно составляет 10 % для фенола и 45 % для 3-ХФ.
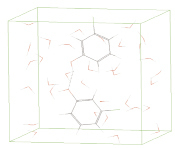
Рис. 6. Димер 3ХФ в «боксе»
Таблица 3
Данные квантово-химических расчетов
|
Характеристика |
фенол |
3-ХФ |
|
Дипольный момент μ, Дб |
1,165 |
2,814 |
|
ЕНВМО , ккал/моль |
+ 0,246 |
– 0,246 |
|
ЕХ+Н2О , ккал/моль |
2,01 |
1,71 |
|
ЕХ+Х , ккал/моль |
2,1 |
3,9 |
|
Е`Х+Х+Х , ккал/моль |
3,5 |
4,6 |
Таким образом, ассоциаты фенола и 3-хлорфенола – это устойчивые структуры, и их присутствие в растворе влияет на процесс анодного окисления, кинетические параметры которого зависят от состава анода и среды. Церий и сурьма увеличивают активность платинированного титанового анода, снижая эффект блокировки поверхности прочно адсорбированным органическим веществом или продуктами его превращения.
Библиографическая ссылка
Салех М.М., Заев Д.А., Михаленко И.И. КИНЕТИКА ОКИСЛЕНИЯ ФЕНОЛА И 3-ХЛОРФЕНОЛА В ВОДНЫХ РАСТВОРАХ НА TI АНОДАХ С PT, СЕPT, SBPT ПОКРЫТИЯМИ // Успехи современного естествознания. 2017. № 5. С. 17-23;URL: https://natural-sciences.ru/en/article/view?id=36448 (дата обращения: 17.05.2026).